微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中
(1)______是还原剂,______是还原产物.
(2)该反应的离子方程式为:______.
(3)用双线桥法分析此氧化还原反应 2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O______
(4)NA表示阿伏伽德罗常数,若产生标准状况下的气体的体积为2.24L,则反应过程中转移电子的数目为______,被氧化的HCl的质量为______g.
参考答案:在2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O反应中,Mn元素的化合价降低,Cl元素的化合价升高,
(1)该反应中HCl为还原剂,KMnO4为氧化剂,则MnCl2为还原产物,故答案为:HCl;MnCl2;
(2)在离子反应中,气体和水应保留化学式,该反应的离子反应为MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O,故答案为:MnO4-+16H++10Cl-=2Mn2++5Cl2↑+8H2O;
(3)该反应中Mn得到2×5e-,Cl失去10×e-,则双线桥法表示反应转移的电子的方向和数目为
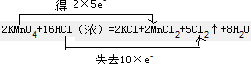
,
故答案为:

;
(4)若产生标准状况下的气体的体积为2.24L,n(Cl2)=2.24L22.4L/mol=0.1mol,反应过程中转移电子的数目为0.1mol×2×1×NA=0.2NA,被氧化的HCl的物质的量为0.2mol,则被氧化的HCl的质量为0.2mol×36.5g/mol=7.3g,故答案为:0.2NA;7.3.
本题解析:
本题难度:简单
2、选择题 在下列反应中,反应物中的含硫物质被还原的是( )
A.稀硫酸与锌反应
B.铜片与浓硫酸共热
C.二氧化硫与氧气反应
D.三氧化硫与水反应
参考答案:A.稀硫酸与锌反应生成硫酸锌和氢气,Zn和H元素化合价发生变化,故A错误;
B.铜片与浓硫酸共热,反应生成硫酸铜、二氧化硫和水,Cu和S元素化合价变化,浓硫酸起到氧化剂的作用,S元素化合价由+6价降低到+4价,故B正确;
C.二氧化硫与氧气反应生成三氧化硫,S元素化合价升高,被氧化,故C错误;
D.三氧化硫与水反应生成硫酸,S元素化合价没有发生变化,故D错误.
故选B.
本题解析:
本题难度:简单
3、选择题 下列反应中必须加入还原剂才能进行的是( )
A.Fe3+→Fe2+
B.Zn→Zn2+
C.H2→H2O
D.CuO→CuCl2
参考答案:A.Fe3+→Fe2+,铁离子得电子化合价降低,所以铁离子作氧化剂,故A选;
B.Zn→Zn2+,锌失电子化合价升高,所以锌作还原剂,故B不选;
C.H2→H2O,氢气失电子化合价升高,所以氢气是还原剂,故C不选;
D.CuO→CuCl2,铜元素化合价不变,所以氧化铜既不是氧化剂又不是还原剂,故D不选;
故选A.
本题解析:
本题难度:简单
4、选择题 下列单、双线桥的表示方法不正确的是( )
A.

B.
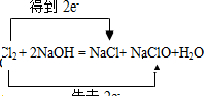
C.

D.
参考答案:A、钠元素的化合价升高,氯元素的化合价降低,则钠失去电子,转移的电子数为2e-,故A正确;
B、该反应中Cl元素的化合价既升高又降低,转移的电子数为e-,正确的表示为
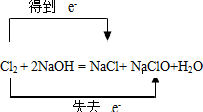
,故B错误;
C、该反应中钠失去电子,氢得到电子,转移的电子数为2e-,故C正确;
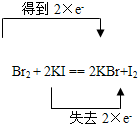
D、该反应中碘失去电子,溴得到电子,转移的电子数为2e-,故D正确;
故选B.
本题解析:
本题难度:简单
5、选择题 某同学为探究黄瓜汁长期放置后维生素C含量的变化,分别向盛有等体积淀粉-碘溶液的两烧杯中滴加新鲜黄瓜汁和久置黄瓜汁,并记录使淀粉-碘溶液蓝色刚好褪去时所滴加的黄瓜汁的滴数,结果如下表(维生素C能使淀粉-碘溶液褪色).该实验说明
( )
A.黄瓜汁中的维生素C具有氧化性
B.新鲜黄瓜汁中维生素C含量较高
C.久置黄瓜汁中维生素C含量较高
D.两者的维生素C含量一样高
参考答案:A、黄瓜汁中的维生素C具有还原性,不具有氧化性,故A错误;
B、新鲜黄瓜汁使淀粉-碘溶液蓝色刚好褪去时所滴加的黄瓜汁的滴数较少,而久置黄瓜汁中的维生素C能够被空气中的氧气氧化,使淀粉-碘溶液蓝色刚好褪去时所滴加的黄瓜汁的滴数较多,说明新鲜黄瓜汁中维生素C含量较高,故B正确;
C、久置黄瓜汁中的维生素C能够被空气中的氧气氧化,使淀粉-碘溶液蓝色刚好褪去时所滴加的黄瓜汁的滴数较多,说明久置黄瓜汁中维生素C含量较低,故C错误;
D、新鲜黄瓜汁使淀粉-碘溶液蓝色刚好褪去时所滴加的黄瓜汁的滴数较少,而久置黄瓜汁中的维生素C能够被空气中的氧气氧化,使淀粉-碘溶液蓝色刚好褪去时所滴加的黄瓜汁的滴数较多,说明新鲜黄瓜汁中维生素C含量较高,久置黄瓜汁中维生素C含量较低,故D错误;
故选B.
本题解析:
本题难度:一般