| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《常见的化学电源》高频试题特训(2017年最新版)(六)
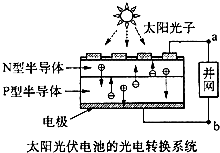 参考答案:通过图片分析知, 本题解析: 本题难度:一般 2、选择题 在碱性锌锰干电池中,已知氢氧化钾为电解质,发生的电池总反应为:Zn+2MnO2+2H2O===2MnOOH+Zn(OH)2。下列该电池的电极反应,正确的是 |
参考答案:C
本题解析:该电池中,Zn元素化合价由0价变为+2价,所以Zn作负极,Mn元素化合价由+4价变为+3价,所以二氧化锰作正极,根据电池反应式知,负极反应式为Zn-2e-+2OH-=Zn(OH)2,正极反应式为2MnO2+2H2O+2e-
本题难度:一般
3、选择题 铅蓄电池是一种典型的可充电电池(如图所示),电池总反应式为PbSO4+2H2O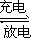 Pb+PbO2+4H++
Pb+PbO2+4H++
2SO42-。则下列说法正确的是 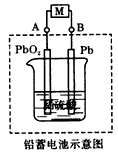
[? ]
A.放电时,电流方向由B过M到A
B.充电时,铅蓄电池的正极应与充电器电源的负极相连
C.放电时,正极反应是Pb-2e-+SO42-= PbSO4
D.充电时,阳极反应是PbSO4-2e-+2H2O=PbO2+SO42-+4H+
参考答案:D
本题解析:
本题难度:一般
4、实验题 锂离子电池的广泛应用使回收利用锂资源成为重要课题:某研究性学习小组对废旧锂离子电池正极材料(LiMn2O4、碳粉等涂覆在铝箔上)进行资源回收研究,设计实验流程如下: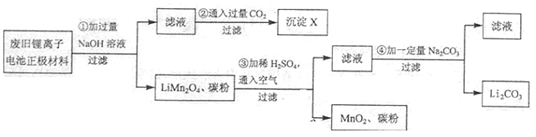
(1)第②步反应得到的沉淀X的化学式为 。
(2)第③步反应的离子方程式是 。
(3)第④步反应后,过滤Li2CO3所需的玻璃仪器有 。
若过滤时发现滤液中有少量浑浊,从实验操作的角度给出两种可能的原因:
、 。
(4)若废旧锂离子电池正极材料含LiMn2O4的质量为18.1 g,第③步反应中加入20.0mL 2.5mol・L-1的H2SO4溶液。正极材料中的锂经反应③和④完全转化为Li2CO3,至少有 g Na2CO3参加了反应。
参考答案:(1)Al(OH)3(2分)
(2)4 LiMn2O4+O2+4H+=4Li++8MnO2+2H2O (2分)
(3) 漏斗玻璃棒烧杯(3分); 滤纸破损、滤液超过滤纸边缘等(2分)
(4)5.3(2分)
本题解析:正极材料包括LiMn2O4、碳粉、铝箔,其中的铝箔可溶合地碱液:①2Al+2NaOH+2H2O=2NaAlO2+3H2↑
过滤后,向滤液中通入过量的CO2:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3-,故沉淀X为Al(OH)3;滤渣为LiMn2O4、碳粉,向加稀硫酸并通入空气LiMn2O4溶解:4 LiMn2O4+O2+4H+=4Li++8MnO2+2H2O,过滤得到滤渣MnO2及碳粉;滤液加入碳酸钠:2Li++CO32-=Li2CO3↓,过滤可得到Li2CO3
过滤过程中所需要的玻璃仪器包括漏斗玻璃棒烧杯;若过滤时发现滤液中有少量浑浊,可能是由于滤纸破损、滤液超过滤纸边缘等原因造成
本题难度:一般
5、选择题 查处酒后驾驶采用的“便携式乙醇测量仪”以燃料电池为工作原理,在酸性环境中,理论上乙醇可以被完全氧化为CO2,但实际乙醇被氧化为X,其中一个电极的反应式为:CH3CH2OH-2e-→X+2H+.下列说法中正确的是( )
A.电池内部H+由正极向负极移动
B.另一极的电极反应式为:O2+4e-+2H2O=4OH-
C.乙醇在正极发生反应,电子经过外电路流向负极
D.电池总反应为:2CH3CH2OH+O2→2CH3CHO+2H2O
参考答案:A.原电池工作时,阳离子向正极移动,故A错误;
B.电解质溶液呈酸性,正极反应式为O2+4e-+4H+=2H2O,故B错误;
C.原电池工作时,电子由负极经外电路流向正极,故C错误;
D.电池总反应与乙醇燃烧的方程式相同,应为2CH3CH2OH+O2→2CH3CHO+2H2O,故D正确.
故选D.
本题解析:
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《胶体》高频.. | |