��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
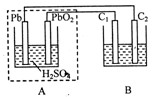
1��ѡ���� ��ͼװ���У�AΪǦ���أ�C1��C2Ϊʯī�缫��B�ձ�����Ũ�Ⱦ�Ϊ0.1mol/L��H2SO3��KI�Ļ����Һ100mL������˵����ȷ����?
A��Ǧ���ع���һ��ʱ���A����Һ��PH��С
B����B�ձ���I-��Ũ�Ƚ�Ϊ0.05mol/Lʱ��A�����ĵ�
H2SO3�����ʵ���Ϊ0.025mol
C����C1��C2��������ʼ��������ʱ����������3.6��1022�����Ӵӵ�·������
D��Ǧ���ع���ʱ�������缫��ӦʽΪ��PbO2��2e -+ H2SO3 ��PbSO4+2H2O +SO42-
�ο��𰸣�B
�����������
�����Ѷȣ���
2������� ȼ�ϵ��������ȼ�ϣ���CO��H2��CH4�ȣ���������Ӧ������Ӧ�����Ļ�ѧ��ת��Ϊ���ܵ�װ�ã�ͨ��������������Ϊ�������Һ��
��1��������й��ڼ��飨CH4��ȼ�ϵ�ص���գ�
�ټ�����������Ӧ�Ļ�ѧ����ʽΪ��
����֪ȼ�ϵ�ص��ܷ�ӦʽΪCH4+2O2+2KOH==K2CO3+3H2O���������һ���ĵ缫��ӦΪCH4+10OH--8e-="=" CO32-+7H2O������缫��ȼ�ϵ�ص� ���������������������һ���缫�ϵĵ缫��ӦʽΪ��
�����ŵ�ز��Ϸŵ磬�������Һ�ļ��� �����������С�����䡱��
��ͨ������£�����ȼ�ϵ�ص����������� ������ڡ�����С�ڡ����ڡ�������ȼ�յ����������ʡ�
��2���ݱ��������Ħ��������MOTOROLA����˾�з���һ���ɼ״��������Լ�ǿ�����������Һ�������ֻ���أ����������������غ�﮵�ص�10����������ʹ��1���³��һ�Ρ��ٶ��ŵ�����У��״���ȫ����������CO2�������������CO32����
�ٸõ�ط�Ӧ�������ӷ���ʽΪ____________________________
�ڼ״���____��������Ӧ��������������ڷŵ��������Һ��pH��____����ͻ����������䣩��
�ο��𰸣���11�֣���1����CH4+O2 CO2+2H2O ��2�֣� ��
CO2+2H2O ��2�֣� ��
�ڸ��� ��1�֣��� 2O2+4H2O+8e-==8OH- ��2�֣�
�ۼ�С ��1�֣� �� �ܴ��ڣ�1�֣�
��2����2CH3OH+3O2+4OH��=2CO32��+6H2O ��2�֣���
�ڸ� ��1�֣��� �½���1�֣�
�����������1���ټ�����������Ӧ���ɶ������Ѻ�ˮ���ʷ���ʽΪCH4+O2 CO2+2H2O��
CO2+2H2O��
��CH4ʧȥ���ӣ�����������Ӧ���Ǹ�����O2���������õ����ӣ�������ԭ��Ӧ���缫��ӦʽΪ2O2+4H2O+8e-==8OH-��
�۸��ݷ�Ӧʽ��֪��KOH������Ӧ���ʵ������Һ�ļ��Լ�С��
�ܼ���ȼ�ջ��˷Ѵ������������ʼ���ȼ�ϵ�ص����������ʴ��ڼ���ȼ�յ����������ʡ�
��2���ٸ������и����ķ�Ӧ���������õ�ط�Ӧ�������ӷ���ʽΪ2CH3OH+3O2+4OH��=2CO32��+6H2O��
�ڼ״�ʧȥ���ӣ���ѧ�����ߣ�����������Ӧ���ʼ״��ڸ���������Ӧ��ǿ������˷�Ӧ���ʵ���ڷŵ��������Һ��pH�����͡�
���㣺ȼ�ϵ�� ���͵�Դ
���������⿼�����ȼ�ϵ�غ����͵�Դ�����֪ʶ����Ŀ�Ѷȴ���Ϥԭ��صĹ���ԭ���ǽ���Ĺؼ���ע�����֪ʶ��ѧϰ�����ռ�Ӧ�á�
�����Ѷȣ�һ��
3������� (7��)ijͬѧ��Ǧ��������Դ����ʯī���缫���500mLijŨ�ȵ�AgNO3��Һ���۲쵽A�缫�����н������ɣ�B�缫������ɫ�������������Һ��ԭ��������ȫ����ֹͣͨ�磬ȡ��A����ϴ�ӡ�����������缫����5.4g����֪Ǧ���صĹ���ԭ��Ϊ��Pb+PbO2+2H2SO4=2PbSO4+2H2O��
�밴Ҫ��ش��������⣺
��1��A�缫Ϊ���ص�_____����B�缫�ϲ���������Ϊ_________��
��2�����ǰAgNO3��Һ�����ʵ���Ũ��Ϊ____________��
��3������Ӧ������ת�Ƶĵ���Ϊ0.01molʱ��Ǧ������������������ʵ��� Ϊ
?mol��
��4��Ǧ���طŵ�ʱ����������______����������_________�����Һ��pH_____(���������С�����䡱)��
�ο��𰸣�����7�֣�ÿ��1�֣���1��������������O2����2��0.1mol��L-1?��3��0.01
��4��������������
�������������绯ѧ��Ӧ�á�
��1���������������������õ�����������A�缫�����н������ɣ�����A����������B������������������Һ�е�OH���ŵ磬����������
��2��A������������5.4g�����ʵ�����5.4g��108g/mol��0.05mol������ԭ���غ��֪��������Ҳ��0.05mol������Ũ����0.05mol��0.5L��0.1mol/L��
��3���������صķ�Ӧʽ��֪��ÿ����2mol���ᣬ��Ӧ�о�ת��2mol���ӣ����Ե���Ӧ������ת�Ƶĵ���Ϊ0.01molʱ������������0.01mol��
��4�����طŵ�ʱ������Ǧ��������Ǧ������������ǦҲ����������Ǧ�����������������������ӵġ����طŵ�����������ģ�����pH����
�����Ѷȣ�һ��
4��ѡ���� ��ѧ��ؿ���ֱ�ӽ���ѧ��ת��Ϊ���ܣ���ѧ��صı����� �� ��
A�����ϼ۵�����
B�����Ϸ�Ӧ
C��������ԭ��Ӧ
D�����ܵĴ���