微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 元素的原子结构决定其性质和在周期表中的位置,下列说法中正确的是
A.元素周期表中位于金属和非金属分界线附近的元素属于过渡元素
B.某微粒的结构示意简图为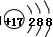 ,则该元素在周期表中位于第三周期、ⅥA族
,则该元素在周期表中位于第三周期、ⅥA族
C.过氧化氢电子式: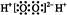
D.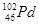 和
和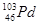 互为同位素
互为同位素
参考答案:D
本题解析:金属和非金属分界线附近的元素全部是主族元素,过渡元素在副族中,故A错误;C选项,过氧化氢是共价化合物,错误。
本题难度:一般
2、填空题 有机物A~F之间的转化关系如下图所示(部分产物已略去),其中B的相对分子质量是D的2倍。

提示: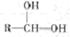 会自动脱水形成R―CHO
会自动脱水形成R―CHO
根据以上信息回答下列问题:
(1)B的分子式是?
(2)检验D中官能团可使用的试剂名称是?,写出D的相邻同系物与该试剂反应的化学方程式_______________________________。
(3)C遇FeCl3溶液显紫色,核磁共振氢谱中有四个峰,其峰面积比为1:2:2:1。写出C的结构简式_______________________。
(4)写出符合下列条件的C的同分异构体的结构简式_______、______、______、________。
①苯环上存在对位取代基;②遇FeCl3溶液显紫色;
③能与银氨溶液反应。
(5)写出A的结构简式__________________________。
(6)若1molA 和足量NaOH反应,最多能消耗___________mol NaOH。
和足量NaOH反应,最多能消耗___________mol NaOH。
参考答案: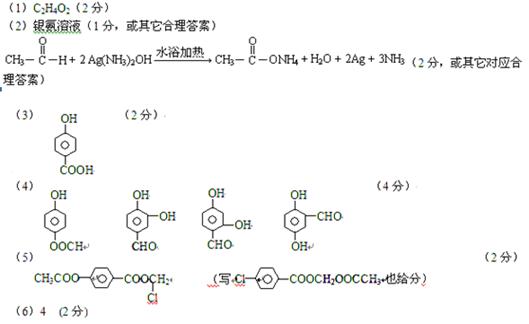
本题解析:略
本题难度:一般
3、选择题 下列说法正确的是(?)
A.不同的核素一定是不同的原子
B.H2和D2互为同位素
C.所有主族元素的最高正化合价都等于其价电子数
D.所有的过渡元素都是金属元素,所有的金属元素也都是过渡元素
参考答案:A
本题解析:H2和D2是单质;同位素是同种元素不同原子间的互称;主族元素中的O、F的最高正价不等于其价电子数;所有的过渡元素都是金属元素,但金属元素不一定都是过渡元素,如Na、K、Pb、Al等。
本题难度:简单
4、选择题 A的原子结构示意图为: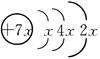 ,其基态原子的价电子层电子排布式正确的是
,其基态原子的价电子层电子排布式正确的是
A.3s23p2
B.3d24s2
C.4s24p2
D.3s23p4
参考答案:A
本题解析:根据核外电子排布规律可知,最内层K层只能容纳2个电子,则x=2,所以A原子的原子序数是14,属于第三周期ⅣA族的硅元素,则其基态原子的价电子层电子排布为3s23p2,答案选C。
本题难度:一般
5、填空题 (7分)短周期元素Q、R、T、W在元素周期表中的位置如右图所示,其中T所处的周期序数与主族序数相等,请回答下列问题:
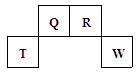
(1)T的原子结构示意图为?;
(2)Q的最高价氧化物水化物的酸性?W的最高价氧化物水化物的酸性,则元素的非金属性:Q ??W(填“>”或“<”);
(3)W的单质与其最高价氧化物的水化物浓溶液共热能发生反应,生成两种物质,一种是液体,另一种是气体,该气体能使品红溶液褪色,则反应的化学方程式为?;
(4)R有多种氧化物,其中甲的相对分子质量最小。在一定条件下,2L的甲气体与0.5L的氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的R的含氧酸盐的化学式是?;
参考答案:(1) ? (1分)?(2)<? (1分)?<? (1分)
? (1分)?(2)<? (1分)?<? (1分)
(3)S+2H2SO4(浓)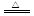 3SO2↑+2H2O? (2分)
3SO2↑+2H2O? (2分)
(4)NaNO2;(2分)
本题解析:“T所处的周期序数与主族序数相等”,同时结合图的结构可知:T处于第三周期IIIA族,所以,T为铝元素;则Q为碳元素、R为氮元素,W为硫元素;
(2)碳酸是弱酸,硫酸是强酸,故Q的最高价氧化物水化物的酸性<W的最高价氧化物水化物的酸性;而最高价氧化物对应水化物的酸性越强,则原子的得电子能力越强,元素的非金属性越强;
(3)“该气体能使品红溶液褪色”,所以该气体为SO2,再利用原子守恒得:另一液体产物为水;根据题目的叙述即可得出反应的方程式:S+2H2SO4(浓)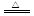 3SO2↑+2H2O(S与浓H2SO4发生了氧化还原反应,故应利用化合价升降相等配平方程式)
3SO2↑+2H2O(S与浓H2SO4发生了氧化还原反应,故应利用化合价升降相等配平方程式)
(4)R的+1、+2、+3、+4、+5价都有氧化物,其中NO的相对分子质量最小,则甲为NO;
“2L的甲气体与0.5L的氧气相混合”
2NO + O2 = 2NO2,
2? 1? 2
1L? 0.5L? 1L
则反应后变为1LNO与1LNO2(即在同温同压下,两者等物质的量)的混合物,再“该混合气体被足量的NaOH溶液完全吸收后没有气体残留”说明反应为:NO+NO2+2NaOH=2NaNO2+H2O(发生了氧化还原反应,NO中N为+2价,NO2中N为+4价,故两者发生归中反应,生成+3价,故为NaNO2)
本题难度:一般