| �߿�ʡ������ | |
|
|
| �߿�ʡ������ | |
|
|
|
�߿���ѧ֪ʶ����ɡ������Ļ�ѧ��Դ������Ԥ�⣨2017��ǿ���棩(��)
�ο��𰸣�B ������������淴Ӧ������ͬ������¿������߽��еķ�Ӧ���ʴ˵���ܷ�Ӧ���ǿ��淴Ӧ���ŵ�ʱ��ԭ��أ���ѧ��ת��Ϊ���ܣ����ʱ����ת��Ϊ��ѧ�� �����Ѷȣ��� 2������� ��6�֣���������ȼ�ϵ����һ�ָ�Ч�������Ѻõ����͵�أ��ں��պ��졢DZͧ������������õ��˹㷺��Ӧ�á� �ο��𰸣� ����������� �����Ѷȣ�һ�� 3��ѡ���� ��ͼΪһ�����͵�����ȼ�ϵ�أ���������Ϳ����ø�ĵ缫�����ڳ������������������IJ������У�����������Ի�ϴӶ�ʡȥ�˰����ȼ�ϸ���Ĥ�����ж��乤��ԭ��������ȷ���ǣ� �� |
�ο��𰸣�C
���������������Ϣ�õ�ط�Ӧ����ʽΪ2H2��O2=2H2O�����������У�H2OΪ�ȶ������������ӦʽΪO2��2H2O��4e��=4OH����������ӦʽΪ2H2��4e��=4H����H������������������ͬ����Ӧ�����У�H��Ũ�Ȳ��䣻����ø�����������ԣ���ʧȥ��Ч����
�����Ѷȣ�һ��
4��ѡ���� ��29����˻��ڼ䣬��Ϊ���������ܳ��͵������㳵��������װ�š���ɫ���ࡱ�������ӽ���Ĥȼ�ϵ�أ��乤��ԭ����ͼ��ʾ��������������ȷ����

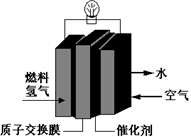
A��ͨ������ĵ缫����������Ӧ
B��ͨ�������ĵ缫Ϊ����
C�������ĵ缫��ӦʽΪ��O2+4H+-4e-==2H2O
D���ܷ�ӦʽΪ��O2+2H2==2H2O
�ο��𰸣�D
���������
ר�⣺�绯ѧר�⣮
��������ȼ�ϵ���У�ͨ��ȼ�ϵĵ缫�Ǹ������ü��Ϸ���ʧ���ӵ�������Ӧ��ͨ�������ĵ缫���������ü��Ϸ����õ��ӵĻ�ԭ��Ӧ���ܷ�Ӧ��Ϊȼ��ȼ�յĻ�ѧ����ʽ��
��𣺽⣺A������ȼ�ϵ�صĵ缫��Ӧ���ɣ�ͨ������������������ĵ缫��������������ԭ��Ӧ����A���� B������ȼ�ϵ�صĵ缫��Ӧ���ɣ�ͨ��ȼ�������ĵ缫�Ǹ�������B����C��ͨ�������ĵ缫���������ü��Ϸ����õ��ӵĻ�ԭ��Ӧ�������Ի����£��缫��ӦΪ��O2+4H++4e-�T2H2O����C���� D����ȼ�ϵ���У�����ȼ�ϵ�صĵ缫��Ӧ���ɣ��ܷ�Ӧ��Ϊȼ��ȼ�յĻ�ѧ����ʽ����O2+2H2�T2H2O����D��ȷ��ѡD��
���������⿼��ѧ��ȼ�ϵ�صĹ���ԭ��֪ʶ�����Ը�����ѧ֪ʶ���лش��ѶȲ���
�����Ѷȣ���
5������� ��6�֣�Ǧ�����ǵ��͵Ŀɳ��͵�أ��������������Ƕ��Բ��ϣ�����ܷ�ӦʽΪ��Pb+PbO2+4H++2SO42- 2PbSO4+2H2O�ش��������⣨�������⡢����������ԭ��
2PbSO4+2H2O�ش��������⣨�������⡢����������ԭ��
��1���ŵ�ʱ�������ĵ缫��Ӧʽ��?�������·ͨ��1mol����ʱ�����Һ������H2SO4?mol��
��2�����ʱ��Pb �͵�Դ��?����������ʱ�����ĵ缫��ӦʽΪ?��
�ο��𰸣���1��PbO2��2e����4H����SO42����PbSO4��2H2O? 1
��2����? PbSO4��2e����Pb��SO42��
�����������1���ŵ��൱��ԭ��أ���ԭ����������õ����ӣ����ݷ�Ӧʽ��֪��������Ǧ�õ����ӣ�����������ӦʽΪPbO2��2e����4H����SO42����PbSO4��2H2O�������ܷ�Ӧʽ��֪��ÿ����2mol���ᣬ��Ӧ�о�ת��2mol���ӣ��������ͨ��1mol���ӣ�������1mol���ᡣ
��2������൱�ڷŵ���淴Ӧ���ŵ���Ǧ�Ǹ���ʧȥ���ӣ����Գ��ʱǦ�͵�Դ�ĸ������������������õ����ӣ����Է�ӦʽΪPbSO4��2e����Pb��SO42����
�����Ѷȣ�һ��
| ���� �� С������ӡ�� �������� ���ر��� �����ض����� | |
| ��һƪ���߿���ѧ�ؿ�֪ʶ�㡶���ۺ���.. | |
| �����Ŀ |