微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 以NA?表示阿伏加德罗常数,下列说法正确的是( )
A.T℃时,1?L?pH=6纯水中,含10-8NA个OH-
B.15.6?g?Na2O2?与过量CO2反应时,转移的电子数为0.4NA
C.1?mol?SiO2中含有2?mol?Si-O单键
D.14g分子式为CnH2n的(n≥2)链烃中含有的C=C的数目一定为NA/n
参考答案:A、1?L?pH=6纯水中,含10-6NA个OH-,故A错误;
B、15.6gNa2O2?物质的量为0.2mol,与过量CO2反应时,过氧化钠自身氧化还原反应,转移的电子数为0.2NA,故B错误;
C、1?molSiO2中含有4molSi-O单键,故C错误;
D、依据通式判断链烃中含有一个双键,14g分子式为CnH2n物质的量=14g14ng/mol=1nmol,链烃中含有的C=C的数目一定为NA/n,故D正确;
故选D.
本题解析:
本题难度:简单
2、选择题 设NA为阿伏加德罗常数的值,下列叙述正确的是
[? ]
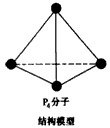
A.6.2 g白磷(分子式为P4,分子结构如图所示)所含P-P键数目为0.15NA
B.常温常压下,16g14CH4所含中子数目为8NA
C.117g氯化钠固体中含有2NA个氯化钠分子
D.含5NA个电子的氨气中,氢原子数目为1.5NA
参考答案:D
本题解析:
本题难度:简单
3、选择题 设NA为阿伏加德罗常数的数值,下列说法正确的是( )
A.3molNO2与水充分反应,转移NA个电子
B.常温常压下,18gH2O含有3NA个原子
C.1L0.1mol?L-1 NaHCO3溶液中含有0.1NA个HCO3-
D.标准状况下,2.24L乙醇含有0.1NA个CH3CH2OH分子
参考答案:A、3如ol二氧化氮与水完全反应生成5如ol硝酸和1如ol一氧化氮,总共转移了5如ol电子,转移了5NA3电子,故A错误;
B、18g水的物质的量为1如ol,1如ol水中含有5如olH、1如olO,总共含有3如ol原子,含有3NA3原子,故B正确;
C、1L&nb5p;我.1如ol?L-1 NaHCO3溶液中含有溶质碳酸钠我.1如ol,由于碳酸氢根离子部分水解,所以溶液中含有的碳酸氢根离子小于我.1如ol,含有的碳酸氢根离子数目小于我.1NA,故C错误;
D、标准状况下,乙醇的状态不是气体,题中条件无法计算5.5aL乙醇的物质的量,故D错误;
故选B.
本题解析:
本题难度:简单
4、选择题 下列叙述正确的是( )(NA代表阿伏加德罗常数)
A.1mol?O?的质量是16g/mol
B.H2O的摩尔质量为18g
C.44g?CO2的体积为22.4L
D.9.8g?H2SO4含0.1NA个H2SO4分子
参考答案:A.氧原子的摩尔质量为16g/mol,1mol?O?的质量是16g,故A错误;
B.摩尔质量以g/mol作单位,数值上等于其相对式量或相对原子质量,H2O的摩尔质量为18g/mol,故B错误;
C.44克二氧化碳的物质的量,根据n=mM=44g44g/mol=1mol,标准状况下,1mol气体的体积为22.4L,44g CO2如果不是在标准状况下,它的体积不一定为22.4L,故C错误;
D.9.8g?H2SO4的物质的量,根据n=mM=9.8g98g/mol=0.1mol,含有0.1NA个H2SO4分子,故D正确;
故选D.
本题解析:
本题难度:简单
5、选择题 若NA为阿伏加德罗常数的值,下列叙述中正确的是
①将CO2通过Na2O2固体使其质量增加m?g,反应中转移的电子数为
②标准状况下,11.2L三氯甲烷中所含的分子数为0.5NA
③电解精炼铜时,若阴极得到的电子数为2NA,则阳极溶解的铜的质量小于64g
④将1L?1mol?L-1饱和FeCl3溶液滴入沸水中,其完全水解后生成的Fe(OH)3胶粒数小于NA
⑤2mol?SO2和1mol?O2在一定条件下充分反应后,混合物的分子数大于2NA且小于3NA
⑥10g质量分数为46%的乙醇水溶液中所含氢原子的个数为0.6NA
⑦30g甲醛中含有的共用电子对数为4NA
⑧Na2O2与CO2反应生成11.2L?O2(标准状况),反应中转移的电子数为2NA
⑨18g?D2O中所含的电子数为9NA
⑩46g?NO2和N2O4的混合物中含有的原子数为3NA.
A.①④⑤⑥⑦⑧⑨
B.②③⑥⑦⑧
C.③④⑤⑦⑨⑩
D.②④⑥⑧⑨
参考答案:C
本题解析:分析:①过氧化钠和二氧化碳反应增重相当于CO的质量,结合化学方程式计算电子转移;
②依据气体摩尔体积的条件应用分析判断;
③根据电解精炼的原理和电极反应,电子守恒分析;
④胶体粒子是氢氧化铁的集合体;
⑤二氧化硫和氧气反应是可逆反应不能进行完全;
⑥质量换算物质的量结合分子结构分析计算;
⑦依据质量换算物质的量结合甲醛结构分析计算;
⑧依据过氧化钠和二氧化碳反应的化学方程式计算电子转移;
⑨质量换算物质的量结合分子式计算;
⑩NO2和N2O4的最简式相同,只需要计算46g NO2中原子数.
解答:①将二氧化碳通过过氧化钠固体,固体增加的质量相当于对已CO的质量反应中转移电子数为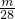 NA,故①错误;
NA,故①错误;
②标准状况三氯甲烷不是气体,11.2L三氯甲烷物质的量不是0.5mol,故②错误;
③电解精炼铜时阴极只有铜离子得到电子生成铜,阳极粗铜中的铜、铁、锌、镍等杂质金属也会失电子溶解,阳极溶解的固体质量小于64g,故③正确;
④氢氧化铁胶体的胶粒是氢氧化铁的集合体,胶粒数小于NA,故④正确;
⑤二氧化硫和氧气反应是可逆反应,用极端假设法,若SO2转化率为0,混合气体分子数为3NA,若二氧化硫转化率100%,则混合气体分子数为2NA,反应是可逆反应,所以平衡后的混合气体分子数大于2NA小于3NA,故⑤正确;
⑥10g46%的乙醇溶液中乙醇溶质质量为4.6g,物质的量为0.1mol,含0.6mol氢原子水质量为5.4g,物质的量为0.3mol,含0.6mol氢原子,所以氢原子总数为1.2NA,故⑥错误;
⑦甲醛分子结构中含有4个共价键,30g甲醛物质的量为1mol,含共用电子对数4NA,故⑦正确;
⑧过氧化钠和二氧化碳反应每生成1molO2转移2mol电子分析,生成11.2L O2(标准状况)物质的量为0.5mol,反应中转移的电子数为NA,故⑧错误;
⑨18gD2O所含的电子数=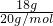 ×10NA=9NA,故⑨正确;
×10NA=9NA,故⑨正确;
⑩NO2和N2O4的最简式相同,只需要计算46g NO2中原子数=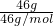 ×3×NA=3NA,故⑩正确;
×3×NA=3NA,故⑩正确;
综上所述:③④⑤⑦⑨⑩正确;
故选C.
点评:本题考查阿伏伽德罗常数的应用,质量换算物质的量计算的方法,气体摩尔体积的条件应用,可逆反应的分析判断,物质结构的理解应用,掌握基础是解题关键,题目难度中等.
本题难度:简单