微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 某同学欲探究SO2的还原性和酸性氧化物的性质,设计了如图所示的实验:
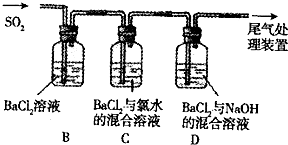
先通N2,将装置中的空气排净,然后通入SO2.请回答:
(1)B中的现象是______.
(2)C中的现象是______,出现该现象的原因是______,______(用离子方程式表示).
(3)D中的现象是______,出现该现象的原因是______,______(用离子方程式表示).
(4)通过上述实验得出的结论是:SO2与BaCl2溶液在______或______条件下会生成沉淀.
参考答案:(1)二氧化硫在碱性条件下可以和钡离子之间发生反应生成白色沉淀,在中性环境下不会发生该反应,故答案为:无明显现象;
(2)氯气具有氧化性,可以将二氧化硫在水溶液中氧化,即SO2+Cl2+2H2O=4H++2Cl-+SO42-,然后是SO42-+Ba2+=BaSO4↓,故答案为:SO2+Cl2+2H2O=4H++2Cl-+SO42;SO42-+Ba2+=BaSO4↓;
(3)在碱性环境下,二氧化硫可以和氢氧根之间发生反应生成亚硫酸根离子,SO2+2OH-=SO32-+H2O,亚硫酸根离子可以和钡离子之间发生反应,即SO32-+Ba2+=BaSO3↓,故答案为:产生白色沉淀;SO2+2OH-=SO32-+H2O;SO32-+Ba2+=BaSO3↓;
(4)根据上述实验的现象得出结论:SO2与BaCl2溶液在强氧化剂存在或是碱性条件下会生成沉淀,故答案为:强氧化剂存在;碱性.
本题解析:
本题难度:简单
2、选择题 下列各组物质中,使有色物质褪色的反应机理相同的是( )
A.二氧化硫和过氧化钠
B.过氧化氢和次氯酸
C.二氧化硫和漂白粉
D.活性炭和二氧化硫
参考答案:B
本题解析:
本题难度:一般
3、选择题 下列情况会对人体健康造成较大危害的是
[? ]
A.自来水中通入少量Cl2进行消毒杀菌
B.用SO2漂白食品
C.用食醋清洗热水瓶胆内壁附着的水垢[主要成分为CaCO3和Mg(OH)2]
D.用小苏打(NaHCO3)发酵面团制作馒头
参考答案:B
本题解析:
本题难度:简单
4、选择题 在通常情况下能大量共存,并且可以用浓硫酸干燥的一组气体是( )
A.SO2、H2S、Cl2
B.NO、O2、Cl2
C.SO2、H2、O2
D.HCl、CO、NH3
参考答案:C
本题解析:
本题难度:简单
5、简答题 用如图1实验装置探究铜丝与过量浓硫酸的反应及S02的部分化学性质.
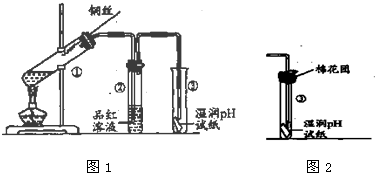
(1)试管①中发生反应的化学反应方程式为______.
(2)装置③证明S02溶液显______性,同时证明S02______(填“能”或“不能”)漂白pH试纸.
(3)实验完毕,取下试管②并加热,可观察的现象是______;该实验可以达到的目的是______.
(4)实验初期发现大试管内有白色沉淀生成,该沉淀的化学式为______.
(5)终止试管①中反应的方法是______.
(6)基于环境保护的考虑,如图2是某学生提出的实验改进方法,其中棉花团上应浸取试剂为______任填一种).
参考答案:(1)铜与浓硫酸反应加热条件下生成硫酸铜、二氧化硫、水,依据氧化还原反应写出化学方程式;Cu+2H2SO4?△?.?CuSO4+SO2↑+2H2O,
故答案为:Cu+2H2SO4?△?.?CuSO4+SO2↑+2H2O;
(2)二氧化硫是酸性氧化物溶于水生成亚硫酸显酸性,装置3湿润的PH试纸变红色,证明二氧化硫溶液显酸性;同时证明二氧化硫的漂白性具有选择性,不能漂白变色的pH试纸,
故答案为:酸;不能;
(3)试管2二氧化硫通入后品红变无色,加热恢复原来的颜色红色,说明二氧化硫的漂白性不稳定,二氧化硫和水生成的亚硫酸和有色物质结合成不稳定的无色物质,加热恢复原来的颜色,
故答案为:溶液由无色恢复为红色;说明二氧化硫与有色物质生成的无色物质不稳定;
(4),浓硫酸溶液中水是水合分子形式,开始反应生成水少,与铜反应开始生成的硫酸铜不能溶解;实验初期发现大试管内有白色沉淀生成,
故答案为:CuSO4 ;
(5)终止试管①中反应的方法是,停止加热 或把铜丝抽离浓硫酸溶液,故答案为:停止加热或把铜丝抽离浓硫酸溶液;
(6)装置中 生成的二氧化硫气体是污染性气体,不能排放到空气中,改进装置中的棉花是吸收二氧化硫的作用,可以用氢氧化钠溶液或高锰酸钾溶液等,
故答案为:NaOH溶液或高锰酸钾溶液;
本题解析:
本题难度:一般