��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��֪A��B��C��D��E�Ƕ������е�5��Ԫ�أ����ǵ�ԭ��������������A�����ڱ���ԭ�Ӱ뾶��С��Bԭ�ӵ��������������ڲ��������2����DԪ����AԪ��ͬ���壮EԪ����CԪ��ͬ���壻E�ĵ���Ϊ��ɫ���壬�����ڶ���̼��
�ٻ���A�������ӵĽṹʾ��ͼ______��
��C�ĵ��ʺ�D�ĵ����ڵ�ȼ�����·�Ӧ���ɻ�����X���÷�Ӧ�Ļ�ѧ����ʽΪ______�������������з�̪��ˮ�У��۲쵽������Ϊ______��
�۽�9gB������������C������ȼ�գ���������ͨ��1L1.0mol?L-1NaOH��Һ�У���ȫ���պ���Һ�д��ڵ����Ӱ�Ũ���ɴ�С������˳����______��
�ܽ�E�ĵ�����������C�ĵ�����ȼ�գ�������Ҫ����ΪY����Yͨ��X�У�X��Y���ܷ����ķ�Ӧ�Ļ�ѧ����ʽ��______��
�ο��𰸣�A��B��C��D��E�Ƕ������е�5��Ԫ�أ����ǵ�ԭ��������������A�����ڱ���ԭ�Ӱ뾶��С����AΪ��Ԫ�أ�Bԭ�ӵ��������������ڲ��������2������B��2�����Ӳ㣬����������Ϊ4����BΪ̼Ԫ�أ�DԪ����AԪ��ͬ���壬ԭ����������̼Ԫ�أ���DΪ��Ԫ�أ�E�ĵ���Ϊ��ɫ���壬�����ڶ���̼����EΪ��Ԫ�أ�EԪ����CԪ��ͬ���壬��CΪ��Ԫ�أ�
��AΪ��Ԫ�أ�A��������ΪH-��H-�Ľṹʾ��ͼΪ
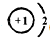
���ʴ�Ϊ��
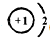
��
������������ȼ�����ɹ������ƣ���Ӧ����ʽΪ2Na+O2?��ȼ?.?Na2O2���������Ƽ�����з�̪��ˮ�У�����������ˮ��Ӧ�����������ƺ�����������ɫ����ų�����Һ��죬�������ƾ���ǿ�����ԣ���ɫ��ȥ��
�ʴ�Ϊ��2Na+O2?��ȼ?.?Na2O2������ɫ����ų�����Һ�ȱ�죬����ɫ��
�۽�9g̼������������������ȼ�գ����ɶ�����̼9g12g/mol=0.75mol���������������̼ͨ��1L1.0mol?L-1NaOH��Һ�У�������̼�������������ʵ���֮��Ϊ0.75��1����������̼������̼�����ƣ���̼������̼�����Ƶ����ʵ����ֱ�Ϊx��y����x+y=0.75mol��2x+y=1mol�����x=0.25mol��y=0.5mol�����ڳʼ���c��OH-����c��H+����̼�����̼�������ˮ��̶ȶ���������c��HCO3-����c��CO32-��������Һ������Ũ���ɴ�С������˳����c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+����
�ʴ�Ϊ��c��Na+����c��HCO3-����c��CO32-����c��OH-����c��H+����
�ܽ�E�ĵ�����������C�ĵ�����ȼ�գ�������Ҫ����ΪY��YΪSO2��XΪNa2O2����SO2ͨ��Na2O2�У����ܷ����ķ�Ӧ�Ļ�ѧ����ʽ��2Na2O2+2SO2�T2Na2SO3+O2����Na2O2+SO2�TNa2SO4��
�ʴ�Ϊ��2Na2O2+2SO2�T2Na2SO3+O2����Na2O2+SO2�TNa2SO4��
���������
�����Ѷȣ�һ��
2��ѡ���� ������Ԫ��A��B��Cԭ���������ε��������ǵ�ԭ�ӵ�����������֮��Ϊ10��A��C�����ڱ���ͬ���壬Bԭ����������������Aԭ�Ӵ���������������������ȷ���ǣ�������
A��ԭ�Ӱ뾶A��B��C
B��A���⻯����ȶ���С��C���⻯��
C��B����������۵��A���������
D��A��C���γ����ӻ�����
�ο��𰸣�Bԭ����������������Aԭ�Ӵ�������������B������������Ϊ2���������ǵ�ԭ�ӵ�����������֮��Ϊ10��A��C�����ڱ���ͬ���壬��֪A��C������������λ4���ֱ�ΪCԪ�ء�SiԪ�أ�A��B��Cԭ���������ε�������BΪMgԪ�أ�
A��AΪCԪ�أ�BΪMgԪ�أ�CΪSiԪ��ԭ�Ӱ뾶Ϊ��Mg��Si��C����A����
B��ͬ����Ԫ�طǽ�����Խǿ���⻯���Խǿ��A���⻯����ȶ��Դ���C���⻯���B����
C��B��������Ϊԭ�Ӿ��壬A��������Ϊ���Ӿ��壬B����������۵��A��������ߣ���C��ȷ��
D��A��C�γɵĻ�����ΪSiC��Ϊ���ۻ������D����
��ѡC��
���������
�����Ѷȣ�һ��
3��ѡ���� X��Y��Ԫ�ص�������֮��Ϊ22��X��ԭ�Ӻ����������Y��ԭ�Ӻ����������6��������˵������ȷ���ǣ�������
A��X�ĵ��ʹ�̬ʱΪ���Ӿ���
B��Y�ĵ�����ԭ�Ӿ���
C��X��Y�γɵĻ������̬ʱΪ���Ӿ���
D��X��̼�γɵĻ������ڹ�̬ʱΪ���Ӿ���
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪X��Y��ZΪ��������Ԫ�أ��ֱ��γ�Xn+��Ym+��Zn-�������ӣ���֪m��n��X��Y������ԭ�ӵ�M���������Ϊ����������˵���в���ȷ���ǣ�������
A�����������У�Ym+���ӵİ뾶��С
B��Z������������ˮ����ķ���ʽΪHnZO4
C��X��Y��Zһ����ͬһ���ڣ���ԭ�Ӱ뾶Z��X��Y
D������Ԫ����Ӧ������������ˮ����֮����ܻ�����������Ӧ
�ο��𰸣�X��Y��ZΪ��������Ԫ�أ��ֱ��γ�Xn+��Ym+��Zn-�������ӣ���X��Y��Z����ԭ�ӵ�M���Ӳ��еĵ�������Ϊ��������X��Y��Z һ�����ڵ�3���ڣ����γɼ�����ΪXn+��Ym+��Zn-������ֵm��n������XΪ��Ԫ�أ�YΪ��Ԫ�أ�ZΪ��Ԫ�أ�
A��������������ͬ�����Ӳ�Խ�����Ӱ뾶Խ���������Ӱ뾶Cl-��Na+�����Ӳ��Ų���ͬ���˵����Խ�����Ӱ뾶ԽС�����Ӱ뾶Na+��Al3+������Al3+���Ӱ뾶��С����A��ȷ��
B��Z������������ˮ����HClO4������n=1��HClO4����HnZO4����B��ȷ��
C��ͬ����ԭ�Ӱ뾶��ԭ�����������Ӷ���С��X��Y��Z�뾶���μ�С����C����
D��X��Y��Z������������Ӧˮ����ֱ�ΪNaOH��Al��OH��3��HClO4��Al��OH��3�����������������NaOH��
HClO4��Ӧ��NaOH��HClO4����������кͷ�Ӧ����D��ȷ��
��ѡ��C��
���������
�����Ѷȣ���
5������� ����������Ԫ��A��B��C��D��ԭ��������������A��Dͬ���壬B��C��ͬһ���ڣ�Bԭ��������������Cԭ����2����A��C�����ڳ����¾�Ϊ���壬������һ���������������2��1��ȫ��Ӧ���������ڳ�������Һ�壮��Һ����D�����ڳ������ܾ��ҷ�Ӧ����A�ĵ��ʣ�������Һ�����̪�Ժ�ɫ���ش��������⣺
��1��д��Ԫ�ط���A______��B______��C______��D______��
��2��д��B��C���ֵ�����ȫ��Ӧ������������ĵ���ʽ______���÷��ӿռ乹��Ϊ______��
��3��C��D���ֵ����ڵ�ȼ�������γɵĻ�����ĵ���ʽ
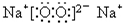
���ж����еĻ�ѧ��������______��
��4��д��������A��B��C��D����Ԫ����ɵĻ�����Ļ�ѧʽ______��______��
�ο��𰸣�����A��C�����ڳ����¾�Ϊ���壬������һ���������������2��1��ȫ��Ӧ���������ڳ�������Һ�壮��֪Һ����ˮ��AΪ������CΪ����������ˮ��D�����ڳ������ܾ��ҷ�Ӧ����A�ĵ��ʣ�������Һ�����̪�Ժ�ɫ����A��Dͬ���壬����������Ԫ�أ���֪DΪ�ƣ�����B��C��ͬһ���ڣ�Bԭ��������������Cԭ����2������֪BΪ̼��
��1����AΪ������BΪ̼��CΪ������DΪ�ƣ�����Ԫ�ص�Ԫ�ط��ŷֱ��ǣ�H��C��O��Na���ʴ�Ϊ��H��C��O��Na��
��2����̼��������ȫ��Ӧ�����ɶ�����̼���ʴ�Ϊ��

�� ֱ���Σ�
��3������������м��������Ӻ���������֮������Ӽ�������ԭ�Ӻ���ԭ��֮��Ĺ��ۼ����ʴ�Ϊ�����Ӽ����Ǽ��Լ���
��4��Na��H��C��O����Ԫ������Ԫ����ɵĻ�������NaHCO3��CH3COONa���ʴ�Ϊ��NaHCO3��CH3COONa��
���������
�����Ѷȣ�һ��