微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列关于化学反应速率的说法正确的是
[ ? ]
A.增大反应物浓度,可增大单位体积内活化分子百分数,从而使有效碰撞次数增大
B.有气体参加的化学反应,若增大压强(即缩小反应容器的体积),可增加活化分子的百分数,从而使反应速率增大
C.升高温度能使化学反应速率增大,主要原因是增加了反应物分子中活化分子的百分数
D.催化剂不影响反应活化能但能增大单位体积内活化分子百分数,从而增大反应速率
参考答案:C
本题解析:
本题难度:一般
2、填空题 对于在密闭容器中进行的反应2SO2+O2
2SO3,其他条件不变,只改变一个反应条件,将生成SO3的反应速率的变化填入由表中空格里.(选填增大、减小或不变) | 改变条件 | 速率变化
①
降低温度
______
②
增加O2浓度
______
③
使用V2O5做催化剂
______
④
压缩气体
______
参考答案:①温度对化学反应速率的影响是:温度越高,反应速率越大,温度越低,反应速率越小,故答案为:减小.
①浓度对化学反应速率的影响是:浓度越大,反应速率越大,浓度越小,反应速率越小,故答案为:增大.
③催化剂对化学反应速率的影响是:加入正催化剂,反应速率加快,V2O5是其正催化剂,所以反应速率加快,故答案为:增大.
③压强对化学反应速率的影响是:增大压强,反应速率加快,减小压强,反应速率减慢,压缩体积,增大体系压强,故答案为:增大.
本题解析:
本题难度:简单
3、选择题 在一密闭容器中加入A、B、C三种气体,保持一定温度,在t1~t4(s)时刻测得各物质的浓度如下表。据此下列结论正确的是( )。
测定时刻/s
| t1
| t2
| t3
| t4
| c(A)/(mol・L-1)
| 6
| 3
| 2
| 2
| c(B)/(mol・L-1)
| 5
| 3.5
| 3
| 3
| c(C)/(mol・L-1)
| 1
| 2.5
| 3
| 3
|
A.在t3时刻反应已经停止
B.A的转化率比B的转化率高
C.在容器中发生的反应为:A+2B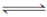 C C
D.在t2~t3内A的平均反应速率为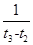 mol・(L・s)-1 mol・(L・s)-1
参考答案:BD
本题解析:在t3时刻各种物质的浓度不再发生变化,说明反应达到平衡状态,A不正确;平衡时A和B的转化率分别是2/3、2/5,所以A的转化率高,B正确;平衡时ABC的变化量分别是4mol、2mol、2mol,则反应的化学方程式应该是2A+B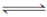 C,C不正确;根据表中数据和反应速率的概念可知,选项D正确,答案选BD。 C,C不正确;根据表中数据和反应速率的概念可知,选项D正确,答案选BD。
点评:该题是高考中的常见题型,属于中等难度的试题。试题综合性强,侧重对学生解题方法与技巧的培养与训练,有利于培养学生的逻辑推理能力,提高学生的应试能力和学习效率。
本题难度:简单
4、简答题 科学研究表明,不少化学反应都具有可逆性,即正向反应和逆向反应都能同时进行.
(1)一定条件下,当可逆反应的正反应速率与逆反应速率______时,反应物与生成物的浓度______,达到表面上静止的一种“平衡状态”,这种状态叫化学平衡状态.
(2)外界条件的变化有可能破坏原有的平衡状态,并在新的条件下建立新平衡,可逆反应中旧平衡破坏和新平衡建立的过程叫化学平衡的移动.化学平衡移动的方向由条件改变时正反应速率[v(正)]和逆反应速率[v(逆)]的相对大小决定.当v(正)>v(逆)时,平衡向右(正反应方向)移动,当v(正)<v(逆)时,平衡向左(逆反应方向)移动,当v(正)=v(逆)时,平衡不移动.勒夏特列从大量实验事实中总结出平衡移动的规律(勒夏特列原理):如果改变影响平衡的一个条件,平衡就向着能够减弱这种改变的方向移动.一定条件下可逆反应2A(g)+B(s)?

2C(g);△H<0达到平衡.现只改变下列一个条件时,试依据勒夏特列原理,判断平衡移动的方向.(填向左移动、向右移动、不移动)
1增大C的浓度______?②减小A的浓度______③增大压强______
(3)已知使用催化剂不能使化学平衡发生移动,试从反应速率的角度说明催化剂不能使化学平衡发生移动的原因______.
参考答案:(1)一定条件下,当可逆反应的正反应速率与逆反应速率相等时,反应物与生成物的浓度保持不变,达到表面上静止的一种“平衡状态”,这种状态叫化学平衡状态,故答案为:相等;保持不变;
(2)根据影响化学平衡移动的因素,减小反应物的浓度,化学平衡逆向移动,增大反应物的浓度,化学平衡正向移动,增大生成物的浓度,化学平衡逆向进行,减小生成物的浓度,化学平衡正向进行,可逆反应2A(g)+B(s)?

2C(g)是一个反应前后气体体积不变的反应,对于反应前后气体体积不变的反应,压强变化不影响平衡的移动,故答案为:向左;向左;不移动;
(3)使用催化剂不能使化学平衡发生移动,因为催化剂同时等幅改变正逆反应速率,故答案为:催化剂同时等幅改变正逆反应速率,条件变化后正逆反应速率依然相等.
本题解析:
本题难度:一般
5、选择题 在化工生产中,如果再加快反应速率,应该优先考虑的科研方向是( )
A.提高设备强度,以便加压
B.选择适宜的催化剂
C.采用高温
D.用块状反应物代替粉末状反应物
参考答案:B
本题解析:由于催化剂可以成千上万倍的加快反应速率,因此优先考虑的科研方向是催化剂。所以答案选B。
本题难度:一般
|