微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列说法中正确的是( )
A.物质发生化学反应时不一定都伴随着能量变化
B.伴有能量变化的变化都是化学变化
C.在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量
D.反应热只与反应体系的始态和终态有关,而与反应的途径无关
参考答案:D
本题解析:
本题难度:简单
2、填空题 在容积为2.0L的密闭容器内,物质D在T℃时发生反应,其反应物和生成物的物质的量随时间t的变化关系如图,据图回答下列问题:
(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为______mol?(L?min)-1.
(2)根据上图写出该反应的化学方程式______,该反应的平衡常数表达式为K=______.
(3)第5min时,升高温度,A、B、D的物质的量变化如上图,则该反应的正反应是______(填“放热”或“吸热”)反应,反应的平衡常数______(填“增大”“减小”或“不变”,下同),B的反应速率______.
(4)若在第7min时增加D的物质的量,A的物质的量变化正确的是______(用图中a、b、c的编号回答).
(5)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总压强为原来的
,则N2的转化率α(N2)=______.
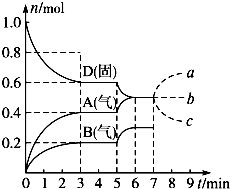
参考答案:(1)从反应开始到第一次达到平衡时,A物质的平均反应速率为0.4mol2.0L3min=0.067mol/L?min,
故答案为:0.067;
(2)根据图象知,随着反应的进行,D的物质的量减少,A、B的物质的量增加,所以D是反应物,A、B是生成物;同一反应、同一时间段内,各物质的浓度变化量之比等于其计量数之比,0-3min时,△D=0.4mol,
△A=0.4mol,△B=0.2mol,△D:△A:△B=0.4mol:0.4mol:0.2mol=4:4:2来源:91考试网 www.91exAm.org,方程式为:2D(s)?2A(g)+B(g);
故答案为:2D(s)?2A(g)+B(g)
因D为固体,所以化学平衡常数K=C2(A)×C(B),
故答案为:K=C2(A)×C(B);
(3)温度升高,D的物质的量减少,A、B的物质的量增大,平衡正向移动,而温度升高,平衡向吸热的方向移动,说明正反应为吸热反应,
平衡常数只有与温度有关,温度升高,平衡正向移动,平衡常数增大;
温度升高化学反应B的反应速率加快;
故答案为:吸热;增大;增大;
(4)D为固体,增加D的物质的量,浓度不变,平衡不移动,故选:b;
(5)一定温度下,在1L密闭容器中充入1molN2和3molH2并发生反应.若容器容积恒定,10min达到平衡时,气体的总压强为原来的910,依据化学平衡三段式列式计算,设氮气消耗物质的量为x;
N2+3H2=2NH3
起始量(mol) 1 3 0
变化量(mol) x 3x 2x
平衡量(mol) 1-x 3-3x 2x
气体的总压强为原来的910,则1-x+3-3x+2x=910×(1+3)
x=0.2mol
则N2的转化率α(N2)=0.2mol1mol×100%=20%;
故答案为:20%.
本题解析:
本题难度:一般
3、选择题 在一密闭容器中有如下反应:aX(g)+bY(g)?nW(g);△H=Q.某化学兴趣小组的同学根据此反应在不同条件下的实验数据,作出了如下曲线图:
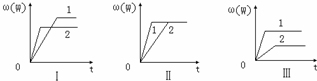
其中,ω(W)表示W在反应混合物中的百分含量,t表示反应时间.其它条?件不变时,下列分析正确的是( )
(1)图Ⅰ可能是不同压强对反应的影响,且P2>P1,a+b<n
(2)图Ⅲ可能是不同温度对反应的影响,且T1>T2,△H<0
(3)图Ⅱ可能是不同压强对反应的影响,且P1>P2,n<a+b
(4)图Ⅱ可能是在同温同压下催化剂对反应的影响,且1中使用的催化剂效果好.
A.(1)(2)
B.(1)(3)
C.(2)(4)
D.(1)(4)
参考答案:D
本题解析:
本题难度:一般
4、选择题 将固体NH4I置于密闭容器中,在一定温度下发生下列反应: ①NH4I(s)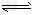 NH3(g)+HI(g);②2HI(g)
NH3(g)+HI(g);②2HI(g)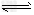 H2(g)+I2(g) 达到平衡时,c(H2)=0.5?mol/L,c(HI)=4?mol/L,则此温度下反应①的平衡常数为
H2(g)+I2(g) 达到平衡时,c(H2)=0.5?mol/L,c(HI)=4?mol/L,则此温度下反应①的平衡常数为
A.9?
B.16
C.20?
D.25
参考答案:C
本题解析:
本题难度:一般
5、简答题 甲醇是一种可再生能源,具有广泛的开发和应用前景,因此甲醇被称为21世纪的新型燃料.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)?CH3OH(g).图l表示反应中能量的变化;图2表示一定温度下,在体积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间变化图.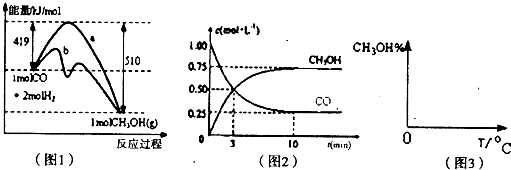
请回答下列问题:
(1)在“图1”中,曲线______(填“a”或“b”)表示使用了催化剂;该反应属于______(填“吸热”或“放热”)反应.
(2)根据“图2”判断,下列说法正确的是______
a.起始充入的CO为1mol
b.增加CO浓度,可使H2的转化率增大
c.容器中压强恒定时,反应已达平衡状态
d.保持温度和密闭容器容积不变,再充入1molCO和2molH2,再次达到平衡时n(CH3OH)/n(CO)会增大
(3)从反应开始到建立平衡,v(H2)=______;该温度下CO(g)+2H2(g)?CH3OH(g)的化学平衡常数为______.若保持其它条件不变,将反应体系升温,则该反应的化学平衡常数将______(填“增大”、“减小”或“不变”).
(4)请在“图3”中画出平衡时甲醇蒸气百分含量(纵坐标)随温度(横坐标)变化的曲线,要求画压强不同的2条曲线(在曲线上标出P1、P2,且P1>P2).
参考答案:(1)加入催化剂,可降低反应的活化能,由图象可知b活化能较低,应加入催化剂,反应物的总能量大于生成物的总能量,则反应为放热反应,
故答案为:b;放热;
(2)A.CO的起始浓度为1moL/L,体积为2L,则起始充入的CO为2mol,故a错误;
B.增加CO浓度,平衡向正方向移动,H2的转化率增大,故b正确;
C.由于反应前后气体的体积不等,则容器中压强恒定时,反应已达到平衡状态,故c正确;
D.保持温度和密闭容器容积不变,再充入1mol CO和2mol H2,相当于在原来的基础上缩小体积,压强增大,平衡向正反应方向移动,则平衡时n(CH3OH)n(CO)会增大,故d正确.
故答案为:bcd;
(3)从反应开始到建立平衡,v(CO)=1mol/L-0.25mol/L10min=0.075moL/(L?min),
则v(H2)=2v(CO)=0.15moL/(L?min),
平衡时:c(CO)=0.25mol/L,c(CH3OH)=0.75mol/L,
则消耗n(CO)=0.75mol/L×2L=1.5mol,消耗的n(H2)=3mol,
平衡时c(H2)=4mol-3mol2L=0.5mol/L,
k=0.750.25×0.52=12,
故答案为:0.15moL/(L?min);12;
(4)增大压强,平衡向正反应方向移动,则甲醇的百分含量增大,温度升高,平衡向逆反应方向移动,甲醇的百分含量降低,则图象可为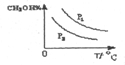 ,
,
故答案为: .
.
本题解析:
本题难度:一般