|
|
|
�߿���ѧ�ؿ�֪ʶ�㡶��ѧƽ�ⳣ������Ƶ����̣�2017�����°棩(һ)
2017-08-06 09:42:01
��Դ:91������
����:www.91exam.org �� �� �� ��
|
��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��֪��Ӧ��2CH3COCH3��l��?CH3COCH2COH��CH3��2��l����ȡ����CH3COCH3���ֱ���0���20���£������ת��������ʱ��仯�Ĺ�ϵ���ߣ�Y-t����ͼ��ʾ������˵����ȷ���ǣ�������
A��b����0����CH3COCH3��Y-t����
B����Ӧ���е�20minĩ��CH3COCH3��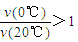
C�������¶ȿ����̷�Ӧ��ƽ���ʱ�䲢�����ƽ��ת����
D����Y=0��Y=0.113��CH3COCH2COH��CH3��2��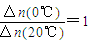
| 
2������� ��ѧ����Դ����������������ʮ�ֹؼ������á�
��1���̲��ں��Ŀ�ȼ���Ǹ�ѹ���γɵ��������ļ���ˮ������壬����֮Ϊ��δ����Դ������25?�桢101?kPa�£�1?g������ȫȼ������CO2��Һ̬ˮʱ����55.6?kJ������ȼ�յ��Ȼ�ѧ����ʽΪ_________________________________����ͬ�����£�356?g��ȼ��(����ʽΪCH4 9H2O)�ͷŵļ���������ȫȼ������CO2��Һ̬ˮ���ų�������Ϊ___________?kJ�� 9H2O)�ͷŵļ���������ȫȼ������CO2��Һ̬ˮ���ų�������Ϊ___________?kJ��
��2�������ѣ�CH3OCH3������Ϊ21���͵�����ȼ�ϣ�������ࡢ��Ч���������ܡ�
��?д��һ�����������Է������������Ԫ��������ͬ���л���Ľṹ��ʽ________��
��?�����ѿ��ɺϳ�����CO��H2����һ���������Ƶá��úϳ����ƶ�����ʱ����������һ�ֿɲ������ѭ������������÷�Ӧ�Ļ�ѧ����ʽ�����ǣ�?_____________________________________________��
��?�Զ����ѡ�����������������ҺΪԭ�ϣ�ʯīΪ�缫�ɹ���ȼ�ϵ�ء��õ���и����ϵĵ缫��Ӧʽ�ǣ�______________________________________________��
��?���ݻ��̶����ܱ������н��л�ѧ��Ӧ��CO(g)?+?H2O(g) CO2(g)?+?H2(g)���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±� CO2(g)?+?H2(g)���仯ѧƽ�ⳣ��K���¶�T�Ĺ�ϵ���±�
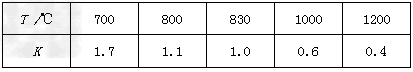
�÷�Ӧ�Ļ�ѧƽ�ⳣ������ʽΪK��____________________���÷�Ӧ������Ӧ��__________��Ӧ������ȡ����ȡ�����
3��ѡ���� ��������������ʱ���ı�ijһ������A����g��+3B��g���T2AB3����g��?��ѧƽ��״̬��Ӱ�죬�õ���ͼ��ʾ�ı仯���ɣ�ͼ��T��ʾ�¶ȣ������н�����ȷ���ǣ�������
A��a��c����A2��ת�������
B������Ӧһ�������ȷ�Ӧ����T2��T1
C��b��ʱ��ƽ����ϵ��A��Bԭ����֮����ӽ���1��3
D����a���ƽ����ϵ�м���A2���ɴﵽb���ƽ��״̬
|

4������� ���Ż�����ʶ����ǿ�������ԴԽ��Խ�����ǹ�ע��
(1)������һ�ֽྻ��Դ����֪��CH4(g)+2O2(g)=CO2(g)+2H2O(g);��H= -802.3kJ/mol H2O(l)=H2O(g)����H= +44 kJ/mol����4.8 g��������ȼ������Һ̬ˮ�ų�����Ϊ��_____________��
(2)���ü�����ˮ��Ӧ�Ʊ���������ԭ�ϼ��������ʸߣ�����ʵ���ƹ��ֵ���÷�Ӧ��
CH4(g) +H2O(g)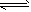 CO(g)+3H2(g);��H= +206.1 kJ/mol
CO(g)+3H2(g);��H= +206.1 kJ/mol
����800��ʱ����Ӧ��ƽ�ⳣ��K1=1.0��ijʱ�̲�ø��¶��£��ܱ������и����ʵ����ʵ���Ũ�ȷֱ�Ϊ��c(CH4) =3. 0mol/L��c(H2O)=8.5 mol/L��c(CO)= 2.0 mol/L��c(H2) =2.0 mol/L�����ʱ���淴Ӧ������ ��ϵ�ǣ�__________������ţ���
A. v��>v�� B. v��<v�� C.v��=v�� D�����ж�
�������¶Ƚ���600��ʱ����ʱƽ�ⳣ��ΪK2���� K1____���>����<����=����K2��
(3)����MnFe2O4��������ͨ��������Ӧ�ɽ�ˮ�ֽ��Ƶ�H2����һ����ӦΪ��
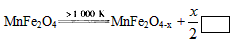 ?����ڵ�����Ϊ��________�� �ڶ�����Ӧ����ʽΪ��
?����ڵ�����Ϊ��________�� �ڶ�����Ӧ����ʽΪ��
______________________��
5��ѡ���� ���ȷ�ӦCO(g)+H2O(g)?CO2(g)+H2(g)��H��0���¶�t1ʱ�ﵽƽ�⣬c1(CO)=c1(H2O)=1.0mol/L����ƽ�ⳣ��ΪK1�����߷�Ӧ��ϵ���¶���t2ʱ����Ӧ���ƽ��Ũ�ȷֱ�Ϊc2(CO)��c2(H2O)��ƽ�ⳣ��ΪK2����( ? )
A��K2=K1
B��c2(CO)=c2(H2O)
C��K2��K1
D��c1(CO)��c2(CO)


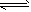 CO(g)+3H2(g);��H= +206.1 kJ/mol
CO(g)+3H2(g);��H= +206.1 kJ/mol 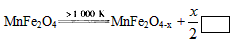 ?����ڵ�����Ϊ��________�� �ڶ�����Ӧ����ʽΪ��
?����ڵ�����Ϊ��________�� �ڶ�����Ӧ����ʽΪ��