��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1�������� ��ͼA��B����װ�ã��ش��������⣺
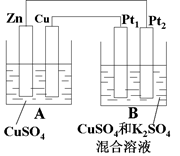
��1��AΪ_________�أ�Pt1Ϊ______����
��2������·��ͨ��0.02mol����ʱ��A��Һ�����仯Ϊ_______________g��
ͬʱB���ռ�����״���µ�����224mL����ӦǰB����ԭ�����Һ��Cu2+��Ũ����__?______����B��ԭ���Һ�����Ϊ200mL����
�ο��𰸣���1��ԭ�� ������1�֣� ��2��0.01��2�֣�?��3��0.025mol/L ��2�֣�
�����������1��п�ܺ�����ͭ�����û���Ӧ������A��ԭ��ء�����п�Ǹ�����ͭ��������B�ǵ��أ���Pt1���Դ��������������������Pt2Ϊ������
��2��п�缫�ĵ缫��Ӧʽ��Zn��2e��=Zn2������·��ͨ��0.02mol����ʱ������п��������0.65g����ͭ�缫��������0.64gͭ������A����Һ����0.65g��0.64g��0.01g��B������ʼ����OH-�ŵ������������缫��Ӧʽ��4OH����4e��=2H2O��O2�������ݵ��ӵ�ʧ�غ��֪�����������������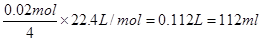 ����B���ռ�����״���µ�����224mL����˵��B�л����������ɣ����������������224ml��112ml��112ml�����ʵ�����0.005mol������B������������ͭ���ӷŵ磬Ȼ���������ӷŵ磬�缫��Ӧʽ�ֱ���Cu2����2e��=Cu��2H����2e��=H2�������Ը��ݵ��ӵĵ�ʧ�غ��֪��������ͭ��
����B���ռ�����״���µ�����224mL����˵��B�л����������ɣ����������������224ml��112ml��112ml�����ʵ�����0.005mol������B������������ͭ���ӷŵ磬Ȼ���������ӷŵ磬�缫��Ӧʽ�ֱ���Cu2����2e��=Cu��2H����2e��=H2�������Ը��ݵ��ӵĵ�ʧ�غ��֪��������ͭ��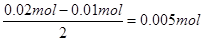 ������ԭ��Һ��Cu2+��Ũ����0.005mol��0.2L��0.025mol/L��
������ԭ��Һ��Cu2+��Ũ����0.005mol��0.2L��0.025mol/L��
�������������е��Ѷȵ����⣬Ҳ�Ǹ߿��еij������㡣���������ǿ�����ض������������ͽ��ⷽ����ѵ����ָ��������������ѧ������˼ά������Ӧ������������Ĺؼ������úõ��ӵ�ʧ�غ㣬���Ҫ�����������ӵķŵ�˳��
�����Ѷȣ�һ��
2������� ij��ȤС��������·�����������ȼ�ϵ�ء�

��1����ͼA��ʾ��a��b��Ϊ���ʯī�������ʯī�������������������ɵ����壩������a��ֱ����Դ����������b��ֱ����Դ�����������������ҺΪNaOH��Һ����a�缫�Ϸ����ĵ缫��ӦʽΪ_________________��������Һ��pH____________�����������С�����䡱����������������
��2��Ȼ����ͼB��ʾ������ֱ����Դ����a��b��������һ����������ܣ����Կ��������ܷ��⡣��ʱ�ĵ���������______________���a��b����b��a������b���ĵ缫��ӦʽΪ______________________________������������������ _��
��3������a������22��4L(��״��)���壬����ת����Ϊ60%����ͨ�������ܵĵ��ӵ����ʵ���Ϊ______________��
�ο��𰸣�(1)4OH����4e����2H2O + O2����3�֣�?����(2��)
(2)a��b?(2��) ?H2+2OH����2e����2H2O��3�֣�? (3)2.4mol(2��)
�����������1��a��ֱ����Դ������������a�缫��������������Һ�е�OH���ŵ������������缫��Ӧʽ��4OH����4e����2H2O + O2�������Ե缫�������������Һ���൱���ǵ��ˮ����������������Һ��Ũ������pH���ߡ�
��2������a�缫����������b�缫�������������Դ�ʱ������ȼ�ϵ�أ�����a��������b�Ǹ�������˵����ķ�����a��b�������������������Һ�����Ը����缫��Ӧʽ��?H2+2OH����2e����2H2O��
��3�����������ʵ�����1mol���ڷ�Ӧ�еõ�4mol���ӣ�����������ת������60�������ͨ�������ܵĵ��ӵ����ʵ�����4mol��60����2.4mol��
��������ԭ����нϻ��õĽ�����������ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ��������õ����ӣ�������ԭ��Ӧ�����ڵ���������ʧȥ�������õ����ӣ�����Ƕ��Ե缫������������Һ�е�������ʧȥ���ӣ���������Һ�е������ӵõ����ӣ��ݴ˿����жϡ�
�����Ѷȣ�һ��
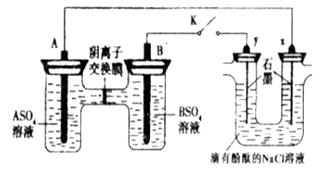
3��ѡ���� ijͬѧ����ͼ��ʾ��װ�ý���ʵ�飬A��BΪ�������������ǵ������ο�����ˮ����K�պ�ʱ�������ӽ���Ĥ����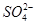 ���������ƶ������з�����ȷ����
���������ƶ������з�����ȷ����
A��A�Ľ����������B
B��Na+��y�缫����x�缫
C��Y�缫������Һ�ȱ��
D��B�ĵ缫��Ӧ��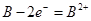
�ο��𰸣�B
�����������������֪����װ�����ұ�װ��Ϊ���أ����װ����ԭ��أ�A����K�պ�ʱ�������ӽ���Ĥ��SO42-���������ƶ���˵��AΪ������BΪ��������A�Ľ������ǿ��B������ B���ұ�װ��������B��y��Ϊ����������A��x��Ϊ���������ع���ʱ��Na+��y�缫����x�缫����ȷ�� C���ұ�װ����y���Ϸ����ĵ缫��ӦʽΪ2Cl--2e-=Cl2����x���Ϸ����ĵ缫��ӦʽΪ2H++2e-=H2�������������ӷŵ�����������Ӳ��ŵ絼����Һ�ʼ��ԣ�X�缫������Һ�ȱ��,����D����K�պ�ʱ���� ���ӽ���Ĥ��SO42һ���������ƶ���˵��AΪ������BΪ������B������Һ�еĽ��������ӵõ������ɽ������ʣ��缫��ӦʽΪB2++2e���TB������
�����Ѷȣ�һ��
4��ѡ���� �����������������IJ�����ߣ��ϵ�ر�����м��д��������ⱻ�ᵽ�����ճ̣�����Ҫԭ���ǣ�������
A�����õ����ǵĽ�������
B����ֹ����й����Ӻ�Ǧ���ؽ������Ӷ�������ˮԴ�����Ⱦ
C����ʹ��������ĵ��Һ��ʴ������Ʒ
D����������ʯī�缫
�ο��𰸣�B
���������
�����Ѷȣ���
5��ѡ���� ����Ƭ���缫a����ͭƬ���缫b����CuSO4��Һ���Թ���ԭ��ػ���أ���ͼ��ʾ��������˵����ȷ����
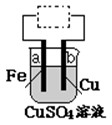
A������ԭ���ʱb����ӦΪ�� Cu��2e-��Cu2+
B�����ɵ�ԭ��ػ���ع�����Ϳ��ܲ�����������
C�����ɵ���ʱb �������ȿ��ܼ���Ҳ��������
D�����ɵ���ʱa������һ�������
�ο��𰸣�
�����ۺ��Ծ�����1ҳ����16ҳ��
?C
���������ԭ����нϻ��õĽ���������������ͭ���ã����Ǹ�����ʧȥ���ӣ�A����ȷ������ǵ��أ����ܲ����������壬B����ȷ��C�����b�����������������٣����������������������C��ȷ��D����ȷ�����a�����������������ӡ���ѡC��
�����Ѷȣ�һ��