��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ��6�֣���ˮ�к��ж��ֳɷ֣�������ж�����ʣ�������ˮ�ֱ�����ͼ�������ʷ����ķ�Ӧ��գ�a��b��c��d�غϲ��ִ������ʼ䷴Ӧ������ˮ����������֤����ˮ����Ư���Ե���??(�a������b������c����d��)��C�����е������� ?��b�����е����ӷ���ʽΪ??��a�����еĻ�ѧ����ʽΪ ?��

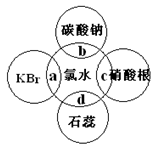
�ο��𰸣�d�� �а�ɫ�������� 2H����CO32����H2O��CO2��2Br����Cl 2��2Cl�� �� Br2
�����������ˮ�е�HClO��ǿ�����ԣ�һ����Ӧ����Ư��ʱ��HClO��ǿ�����Խ���ɫ������������ɫ���ʣ���������ˮ��ʹʯ����Һ�ȱ�죬����ɫ���ʴ�Ϊ��d����ˮ����Cl-������AgNO3��Һ�а�ɫ�������ɣ�����AgCl�������ʴ�Ϊ���а�ɫ�������ɣ���ˮ�к���HCl��HClO���������ԣ���CO32-��Ӧ���ɶ�����̼���壬��Ӧ�����ӷ���ʽΪCO32-+2H+=CO2��+H2O��Cl2��������ˮ����Ҫ�ɷ֣�����ǿ�����ԣ���KBr����������ԭ��Ӧ����Ӧ�Ļ�ѧ����ʽΪ2KBr+Cl2 �T2KCl+Br2���ʴ�Ϊ��CO32-+2H+=CO2��+H2O�� 2KBr+Cl2 �T2KCl+Br2��
���������⿼�����������ʣ���Ŀ�ѶȲ���ע����ˮ�ijɷֺ����ʣ�ע�ػ���֪ʶ�Ļ��ۡ�
�����Ѷȣ�һ��
2��ѡ���� ��Cl2��SO2��Ͼ��Ⱥֱ�ͨ�뵽����������Һ�У���Һ��ɫһ������ȥ����
A��I2����ۻ����Һ
B��KMnO4��Һ
C��Ʒ����Һ
D����ɫʯ���Լ�
�ο��𰸣�C
�����������Cl2��SO2 1:1��Ϻ�ͨ����Һ�ܹ�������Ӧ��Cl2+SO2+2H2O=H2SO4+2HCl����Cl2����������Һ���ܹ���ˮ������Ӧ����������ʹ����ᣬ��������������ԣ���SO2����ʱ���ܹ���ˮ��Ӧ���������ᣬ���������Ư���ԡ�Aѡ�I2����ۻ����Һ����ɫ����SO2������I2��SO2����������ԭ��Ӧ����ɫ��ȥ����Cl2�������ܷ�����Bѡ���SO2������KMnO4�����䷢��������ԭ��Ӧ����Cl2�������ܷ�����Cѡ����ȷ����Cl2�����������Ĵ������ܹ�ʹƷ����ɫ����SO2������������������ͬ����ʹƷ����ɫ��Dѡ�Cl2������ɫʯ���Լ�Ϊ��ɫ���ʱ���ѡ��Cѡ�
�����Ѷȣ�һ��
3������� ���ֹ�������ˮ������ɱ����Ϊ���ƴ��ģ��Ⱦ�Լ�����������Ч����֮һ��Ư���dz��õ�������֮һ��
��1����ҵ�Ͻ�����ͨ��ʯ����[Ca(OH)2]��ȡƯ�ۣ���ѧ��Ӧ����ʽΪ?����Ӧ�٣���
��2��Ư������ˮ���ܿ����е�CO2���ã���������Ư�ס�ɱ�����õĴ����ᣬ��Ӧ��ѧ����ʽΪ?����Ӧ�ڣ���
��3��������ȶ������ֽ⣬��ѧ��Ӧ����ʽΪ?����Ӧ�ۣ���
��4����Ӧ�١���Ӧ�ڡ���Ӧ���У�����������ԭ��Ӧ���ǣ��Ӧ��ţ�?��
�ο��𰸣���1��2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
��2��Ca(ClO)2+CO2+H2O=CaCO3+2HClO
��3��2HClO=2HCl+O2��
��4����,��
�����������1�����������绯��Ӧ�������Ȼ��ƺʹ�����ƣ�Ȼ����ݵ�ʧ�����غ���ƽ���ɡ���д����ʽʱҲ���Կ�����������ˮ��Ӧ��������ʹ����ᣬȻ�����ٺͼ���кͷ�Ӧ��
��2������ǿ���������ԭ����̼������Դ��ڴ����ᣬ����Ca(ClO)2+CO2+H2O=CaCO3+2HClO
��3��������ȶ�������ֽ�ΪHCl��O2��
��4����Ԫ�ػ��ϼ������ķ�Ӧ��������ԭ��Ӧ����Ӧ����Ԫ�ػ��ϼ�û�з����仯��
�����Ѷȣ�һ��
4��ѡ���� ������һ�ֻ�ѧ���ʺܻ��õķǽ������ʣ������н�ǿ�������ԣ����������в���ȷ���ǣ�?��
A�����ȵ�ͭ˿�����������ȼ�գ������ػ�ɫ����
B������������ȼ�գ����ɰ�ɫ����
C����������ˮ��Ӧ���ɴ���������ᣬ������ˮ���ձ�Ϊϡ����
D�����廯�ƺ͵⻯�صĻ����Һ��ͨ�������������Ȼ����Һ���ɲ�����������µ��������Ȼ��ƺ��廯�ء�
�ο��𰸣�D
���������A������ȵ�ͭ˿�����������ȼ�����ɹ����Ȼ�ͭ�����۲쵽�ػ�ɫ���̶���������A��ѡ��B������������ȼ�գ����ɰ�ɫ���̣���NaCl���壬B��ѡ��C��Cl2��H2O=HCl��HClO��2HClO 2HCl��O2��,?C��ѡ��D��2NaBr��Cl2=2NaCl��Br2��2KI��Cl2=2KCl��I2��Ȼ����Һ���ɲ�����������µ��������Ȼ��ƺ��Ȼ��ء�ѡD��
2HCl��O2��,?C��ѡ��D��2NaBr��Cl2=2NaCl��Br2��2KI��Cl2=2KCl��I2��Ȼ����Һ���ɲ�����������µ��������Ȼ��ƺ��Ȼ��ء�ѡD��
�����Ѷȣ�һ��
5��ѡ����  ������ͨ���廯������Һ���ټ������Ȼ�̼�������á�����ʵ������п϶��ܹ۲쵽��������(����)
������ͨ���廯������Һ���ټ������Ȼ�̼�������á�����ʵ������п϶��ܹ۲쵽��������(����)

A���ϲ��Ի���ɫ
B���²��Ժ���ɫ

C���²�����ɫ
D���ڳ�ʪ�������γɰ���
�ο��𰸣�A
�������������Fe2���Ļ�ԭ��ǿ��Br�������ͨ�������ȷ�����2Fe2����Cl2===2Fe3����2Cl����������2Br����Cl2===2Cl����Br2�����ʵ������п϶��ܹ۲쵽������Ϊ�ϲ��Ի���ɫ����Br��û�� ��ʼ��Ӧ�����²�����ɫ����Br���Ѿ���ʼ��Ӧ�����²��Ժ���ɫ�����⿼�����������ʣ��е��⡣
�����Ѷȣ�һ��