微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 利用下图电解装置进行实验。
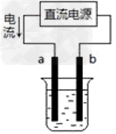
(1)若a、b是惰性电极,电解质溶液是氯化钠溶液,a极是_______极,总反应的离子方程式是_____________________。
(2)若a、b是惰性电极,电解质溶液是硝酸银溶液,b极上的现象是________________,总反应的离子方程式是___________________。
(3)若a、b是惰性电极,电解质溶液是硫酸钾溶液,a极上的电极反应是________,若两极附近分别加入石蕊试液,两极附近的现象是__________________。
参考答案:(1)阳;2Cl-+2H2O Cl2↑+H2↑+2OH-
Cl2↑+H2↑+2OH-
(2)有银白色固体析出;4Ag++2H2O 4Ag+O2↑+4H+
4Ag+O2↑+4H+
(3)4OH--4e-=?2H2O+O2↑;a极附近溶液变红,b极附近溶液变蓝
本题解析:
本题难度:一般
2、选择题 用铂作电极电解500mL含KNO3和Cu(NO3)2的混合溶液一段时间后,在两极均生成11.2L标准状况下的气体,原溶液中Cu2+的物质的量浓度为( )
A.0.5?mol/L
B.2?mol/L
C.1?mol/L
D.无法确定
参考答案:阳极溶液中离子放电顺序书写电极反应,溶液中阴离子氢氧根离子失电子生成氧气,阳离子放电顺序Cu2+>H+,阳极电极反应为:4OH--4e-=2H2O+O2↑,阴极电极反应为:Cu2++2e-=Cu 2H++2e-=H2↑,在两极均生成11.2L标准状况下的气体物质的量为0.5mol,依据电子守恒电极主要电子为4×0.5mol=2mol,生成氢气转移电子1mol,铜离子得到电子1mol,反应的铜离子物质的量0.5mol,所以Cu2+的物质的量浓度=0.5mol0.5L=1mol/L,
故选C.
本题解析:
本题难度:一般
3、选择题 如图所示,U形管中装入含有紫色石蕊的 溶液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:(?)
溶液,通直流电,一段时间后U形管内会形成三色“彩虹”的现象,它从左到右颜色的次序是:(?)
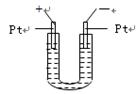
A.蓝、紫、红
B.红、蓝、紫
C.红、紫、蓝
D.蓝、红、紫
参考答案:C
本题解析:根据电解原理,和电源的正极相连的是阳极,和电源的负极相连的是阴极,电解硫酸钠的实质是电解水,阳极生成氧气,阴极生成氢气,阴极氢离子放电,碱性增强,该极附近呈蓝色,阳极氢氧根离子放电,酸性增强,该极附近呈红色,中间溶液是石蕊的紫色,即从左到右颜色的次序是:红、紫、蓝。
本题难度:一般
4、选择题 把等物质的量的Na2SO4、NaCl、AgNO3混合物放入足量水中,经充分搅拌后,将所得溶液用石墨做电极进行电解,阳极生成的物质是:
A.H2
B.Ag
C.Cl2
D.O2
参考答案:D
本题解析:略
本题难度:简单
5、选择题 (2014届山东省日照市高三3月模拟考试理综化学试卷)
电化学在日常生活中用途广泛,图甲是镁一次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2 ,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是
,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是

A.图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2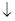
B.图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
C.图乙电解池中,若有0.084 g阳极材料参与反应,则阴极会有336 mL的气体产生
D.若图甲燃料电池消耗3.6 g镁产生的电量用以图乙废水处理,理论上可产生10.7 g氢氧化铁沉淀
参考答案:A
本题解析:
A、根据图甲镁一次氯酸钠燃料电池的结构,ClO?在正极得电子,发生还原反应:Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2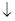 ,正确;B、电解池中阴离子向阳极移动,所以图乙中Cr2O72-金属铁电极移动,错误;C、图乙电解池阳极反应为Fe―2e?=Fe2+,阴极反应为2H++2e?=H2↑所以若有0.084 g阳极材料参与反应,则阴极产生氢气的体积为:0.084g÷56g/mol×22.4L/mol=0.0336L=33.6ml,错误;D、图甲燃料电池消耗3.6 g镁时,失去的电子式0.3mol,图乙中阳极反应为:Fe―2e?=Fe2+,根据电子守恒,生成的Fe2+为0.15mol,所以最后生成的Fe(OH)3也是0.15mol,质量为16.05g,错误。
,正确;B、电解池中阴离子向阳极移动,所以图乙中Cr2O72-金属铁电极移动,错误;C、图乙电解池阳极反应为Fe―2e?=Fe2+,阴极反应为2H++2e?=H2↑所以若有0.084 g阳极材料参与反应,则阴极产生氢气的体积为:0.084g÷56g/mol×22.4L/mol=0.0336L=33.6ml,错误;D、图甲燃料电池消耗3.6 g镁时,失去的电子式0.3mol,图乙中阳极反应为:Fe―2e?=Fe2+,根据电子守恒,生成的Fe2+为0.15mol,所以最后生成的Fe(OH)3也是0.15mol,质量为16.05g,错误。
本题难度:一般