��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ���и����У�ǰ����ܼ���������ӵ���
��3d��4s����4p��5s��?��5s��4d��?��5p��4d
A���٢�
B���ڢ�
C���ڢ�
D���ۢ�
�ο��𰸣�B
���������ԭ�Ӻ����������ռ�������͵Ĺ������������ĸߵ����ܲ���ܼ����������е�3d>4s�����е�4p<5s�����е�5s<4d�����е�5p>4d������ǰ���ܼ���������ӵ��Ǣڢۡ���ȷ�Ĵ�ѡB��
�������ӹ���ԭ��ͼ�п��Կ����ܼ��������ߵͳ��˷���E(ns)<E(np)<E(nd)<E(nf)��E(1s)<E(2s)<E(3s)<E(4s)�ȹ���֮�⣬������һЩ��ͬ�ܲ���ܼ��Ľ����������磬E(3d)>E(4s)��E(4d)>E(5s)��E(5d)>E(6s)��E(6d)>E(7s)��E(4f)>E(5p)��E(4f)>E(6s)�ȡ����ڳ����ܼ���������Kԭ��������һ��͵ڶ�������ŵ�����ʱ��������3s�ܼ���3p�ܼ������һ�����ӽ���4s�ܼ�������3d�ܼ�����������ԭ�ӽṹʾ��ͼΪ��
�����Ѷȣ�һ��
2������� �������ֶ�����Ԫ��A��B��C��D��E����ԭ��������������A��Eͬ���壬AԪ��ԭ�Ӱ뾶��С��BԪ��ԭ�ӵ��������������ڲ��������2����CԪ������������ˮ����X�����⻯��Y��Ӧ����һ���Ρ�A��B��C��E����Ԫ�ض�����DԪ���γ�ԭ�Ӹ����Ȳ���ͬ�ij���������Իش��������⣺
(1)д��X��Y��Ӧ���������εĻ�ѧ����ʽ?��
(2)A��B��D��E����Ԫ����ɵ�ij���������ֽ⡣д�������û�������������? Ba(OH)2��Һ��Ӧ�����ӷ���ʽ?��
(3)��B��ij�ֵ��������缫�����EԪ�ص����������ˮ�������Һʱ�������ĵ缫��ӦʽΪ?��
(4)��һ�ܱ�������ע��A2��C2�������壬�����ˡ� ���Ļ�ѧ��Ӧ����ij�¶��´ﵽƽ��ʱ�������ʵ�Ũ�ȷֱ��ǣ�c(A2)="9.00" mol��L-1��c(C2) ="3.00" mol��L-1��c(CA3) ="4.00" mol��L-1�����ʱ�÷�Ӧ��ƽ�ⳣ��K=?��C2�ij�ʼŨ��Ϊmol��L-1��A2��ת������?����
���Ļ�ѧ��Ӧ����ij�¶��´ﵽƽ��ʱ�������ʵ�Ũ�ȷֱ��ǣ�c(A2)="9.00" mol��L-1��c(C2) ="3.00" mol��L-1��c(CA3) ="4.00" mol��L-1�����ʱ�÷�Ӧ��ƽ�ⳣ��K=?��C2�ij�ʼŨ��Ϊmol��L-1��A2��ת������?����
�ο��𰸣�


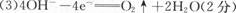

������������ֶ�����Ԫ��A��B��C��D��E����ԭ��������������BԪ��ԭ�ӵ��������������ڲ��������2������֪BԪ��Ϊ̼����֪A��Eͬ���壬AԪ��ԭ�Ӱ뾶��С����֪A��E����һ���ڣ�ԭ��������̼С��AΪ�⣬EΪ�ƣ�CԪ������������ˮ����X�����⻯��Y��Ӧ����һ���Ρ���֪C��Ԫ�أ�
A��B��C��E����Ԫ�ض�����DԪ���γ�ԭ�Ӹ����Ȳ���ͬ�ij����������֪DΪ����
�����Ѷȣ�һ��
3��ѡ���� ����ѡ���У���ʾ��A��ijԪ��ԭ�ӽṹʾ��ͼ����?
�ο��𰸣�A
����������ڢ�A��Ԫ�ص�ԭ���������϶��·ֱ���7��15��33��51��83�ȣ�A�ǵ�Ԫ�أ�B��OԪ�أ�C����Ԫ�أ�D��þԪ�أ���˴�ѡA��
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ����Ԫ�����ڱ��ṹ����Ϥ���ճ̶ȣ���ס���ɣ��ѶȲ���ѧ�����ѵ÷֡�
�����Ѷȣ�һ��
4��ѡ���� ±�ؼ��γɵĻ������硰IF5��BrCl��IBr���ȳ�Ϊ±�ػ������ѧ������±�ص������ƣ������й���±�ػ���������ʵ���������������ط�Ӧ����ȷ����(? )?
A��IF5 + 3H2O = HIO3 +5HF
B��3IBr +2Fe = FeI3 + FeBr3
C��BrCl��������ǿ��I2
D��IBr������NaOH��Һ��Ӧ����2����
�ο��𰸣�B
���������A��IF5����ˮ�⣬����HIO3��HF������ʽΪIF5+3H2O�THIO3+5HF����A��ȷ��B������������Fe3+��I2��IBr������Ӧ����FeI2����B����C��Cl��Br�ķǽ����Ա�Iǿ��BrCl��������ǿ��I2��������������֮�䣬��C��ȷ��D��IBr������NaOH��Һ����NaIO��NaBr����D��ȷ����ѡB��
�����Ѷȣ�һ��
5��ѡ���� Ԫ��X��������ۺ��۵ľ���ֵ֮��Ϊ6��Ԫ��Yԭ�Ӵ������Ԫ��Xԭ�Ӵ�����Ϊ8�����ӣ�X��Y�����Ӿ�����ͬ�ĵ����Ų���X��Y�γɵĻ������ǣ�?��
A��MgF2
B��MgCl2
C��CaCl2
D��CaBr2
�ο��𰸣�C
���������Ԫ��X��������ۺ��۵ľ���ֵ֮��Ϊ6����XΪCl, Ԫ��Yԭ�Ӵ������Ԫ��Xԭ�Ӵ�����Ϊ8�����ӣ�X��Y�����Ӿ�����ͬ�ĵ����Ų�,��YΪK��Ca����ôK��Cl��Ԫ�ؿ����γ�KCl��Ca��Cl��Ԫ�ؿ����γ�CaCl2������ѡ���ȷ����ΪCaCl2����ȷѡ��ΪC��
�����Ѷȣ�һ��