微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一密闭容器中发生反应:2X(g)+Y(g) aZ(g) ΔH=Q kJ・mol-1,开始按体积比2∶1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图象,下列有关说法正确的是( )
aZ(g) ΔH=Q kJ・mol-1,开始按体积比2∶1将X、Y充入反应器中,一定条件下发生反应。图甲和图乙是根据反应绘制的图象,下列有关说法正确的是( )
 ?
?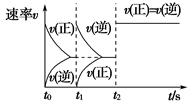
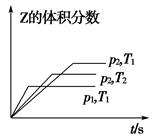
甲 ? 乙
A.图甲,p1>p2,a<3
B.图甲,T1<T2,Q>0
C.图乙,t1时表示恒温、恒压条件下,向平衡体系中充入一定量的Z气体
D.图乙,如果a=3,t2时表示向体系中加入了催化剂或增大压强
参考答案:D
本题解析:A项,图甲,在同一温度下(T1),p1压强下先达到平衡,说明p1>p2,由图可知压强大时Z的体积分数反而小,说明增大压强平衡逆向移动,则a>3;B项,图甲,在同一压强下(p2),T2温度下先达到平衡,说明T2>T1,由图可知温度高时Z的体积分数反而小,说明升高温度平衡逆向移动,则Q<0;D项,图乙,t2时正、逆反应速率同等倍数增大,则可能是使用了催化剂或a=3时增大压强。
本题难度:一般
2、选择题 已知25 ℃时,AgCl 的溶度积Ksp=1.8×10-10,则下列说法正确的是
A.向饱和AgCl水溶液中加入盐酸,Ksp值变大
B.AgNO3溶液与NaCl溶液混合后的溶液中,;一定有c(Ag+)=c(Cl-)
C.温度一定时,当溶液中c(Ag+)×c(Cl-)=Ksp时,此溶液为AgCl的饱和溶液
D.将固体AgCl加入到较浓的KI溶液中,部分AgCl转化为AgI,AgCl溶解度小于AgI
参考答案:C
本题解析:略
本题难度:简单
3、填空题 在锌与盐酸反应的实验中,一个学生得到的结果如下表所示:
?
| 锌的质量/g
| 锌的形状
| 温度/℃
| 溶解于酸所花的时间/s
|
A
| 2
| 薄片
| 5
| 400
|
B
| 2
| 薄片
| 15
| 200
|
C
| 2
| 薄片
| 25
| 100
|
D
| 2
| 薄片
| 35
| 50
|
E
| 2
| 薄片
| 45
| 25
|
F
| 2
| 粉末
| 15
| 5
|
试求:
(1)画一幅以时间对温度的曲线图(纵轴表示时间,横轴表示温度).
(2)利用所画的曲线图,关于温度影响反应速率你能得出什么结论?
(3)20℃时,2g锌箔溶解于酸中需花多少时间?
(4)对比结果B与F,解释F为什么那么快?
参考答案:详见解析
本题解析:
(1)如下图所示
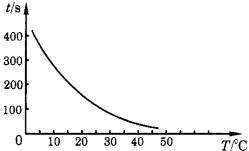
(2)对于该溶液,温度每升高10℃,反应速率加快到原来的2倍。
(3)约150s。
(4)这是因为B中锌是块状,F中锌是粉末状,粉末状与酸溶液的接触面积要比块状大得多,从而使有效碰撞次数大大增多,加快了反应速率。
本题难度:简单
4、选择题 对于实验室制O2的反应:2KClO3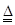 2KCl+3O2↑,下列条件的改变,可加快反应速率的是?
2KCl+3O2↑,下列条件的改变,可加快反应速率的是?
A.加热
B.增大KClO3固体的量
C.使用MnO2做催化剂
D.降温
参考答案:AC
本题解析:加热加快反应速率,A正确;改变固体的质量,反应速率不变,B不正确;二氧化锰是催化剂,可以加快反应速率,C正确;降低温度反应速率降低,D不正确,答案选AC。
点评:该题是基础性试题的考查,主要是考查学生外界条件对影响反应速率的熟悉掌握程度,有利于培养学生的逻辑推理能力、提高学生的应试能力。该题的关键是记住外界条件是如何影响反应速率的,然后灵活运用即可。
本题难度:一般
5、选择题 设C+CO2?2CO-Q1,反应速率v1;N2+3H2?2NH3+Q2反应速率v2.对于上述反应,当温度升高时,v1和v2的变化情况为( )
A.同时增大
B.同时减小
C.v1增大,v2减小
D.v1减小,v2增大
参考答案:升高温度时,活化分子的百分数增大,正逆反应速率都增大,吸热反应或放热反应的速率都增大,与吸放热无关.
故选A.
本题解析:
本题难度:简单