微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 100mL浓度为4mol/L的盐酸跟过量的锌片反应,为减小反应速率,又不影响生成氢气的总量,可采用的方法是
[? ]
A. 加入适量CH3COONa晶体
B. 加入数滴氯化铜溶液
C. 加入适量蒸馏水
D. 加入适量的氯化钠固体
2、实验题 (12分)某化学小组为了研究外界条件对化学反应速率的影响,进行了如下实验:
【实验原理】2KMnO4 + 5H 2C2O4 + 3H2SO4 ="==" K2SO4 + 2MnSO4 + 10CO2↑ + 8H2O
【实验内容及记录】
实验编号
| 温度/℃
| 试管中所加试剂及其用量/ mL
| 溶液褪至无色所需时间/ min
|
0.6 mol/L
H 2C2O4溶液
| H2O
| 0.2 mol/L KMnO4溶液
| 3 mol/L
稀硫酸
|
1
| 20
| 3.0
| 2.0
| 3.0
| 2.0
| 4.0
|
2
| 20
| 3.0
| m
| 2.5
| n
| 4.8
|
3
| 20
| 3.0
| 3.0
| 2.0
| 2.0
| t1
|
4
| 30
| 3.0
| 2.0
| 3.0
| 2.0
| t2
|
(1)已知:实验1、2、3的目的是探究KMnO4浓度对反应速率的影响。则实验2中m= ,
n= 。如果研究温度对化学反应速率的影响,需利用实验4和 。
(2)通过查阅已有的实验资料发现,该实验过程中n(Mn2+)随时间变化的趋势如图所示。

为进行实验探究,该小组同学通过讨论提出假设:Mn2+对该反应有催化作用。
①请你填写表中空白帮助该小组同学完成实验方案。
实验编号
| 温度/℃
| 试管中所加试剂及其用量/mL
| 再向试管中加入少量固体
| 溶液褪至无色所需时间/ min
|
0.6 mol/L
H 2C2O4溶液
| H2O
| 0.2 mol/L KMnO4溶液
| 3 mol/L
稀硫酸
|
5
| 20
| 3.0
| 2.0
| 3.0
| 2.0
|
| t3
|
②能说明该小组同学提出的假设成立的实验事实是 。
(3)有人将酸性KMnO4溶液和H 2C2O4溶液的反应设计成原电池,则该原电池的正极反应式为 。
3、填空题 (I)下图是工业生产硝酸铵的流程。

(1)吸收塔C中通入空气的目的是 。A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) +6H2O(g) △H =-1266.8kJ/mol
N2(g) + O2(g) = 2NO(g) △H =" +180.5" kJ/mol
写出氨高温催化氧化的热化学方程式:
(II)某合作小组同学将铜片加入稀硝酸,发现开始时反应非常慢,一段时间后反应速率明显加快。该小组通过实验探究其原因。
(3)该反应的离子方程式为___________________________________________________。
(4)提出合理假设。该实验中反应速率明显加快的原因可能是_____________________。
A.反应放热导致温度升高 B.压强增大
C.生成物有催化作用 D.反应物接触面积增大
(5)初步探究。测定反应过程中溶液不同时间的温度,结果如下表:
时间/min
| 0
| 5
| 10
| 15
| 20
| 25
| 35
| 50
| 60
| 70
| 80
|
温度/℃
| 25
| 26
| 26
| 26
| 26
| 26
| 26.5
| 27
| 27
| 27
| 27
|
结合实验目的和表中数据,你得出的结论是__________________________________。
(6)进一步探究。查阅文献了解到化学反应的产物(含中间产物)可能对反应有催化作用,请完成以下实验设计表并将实验目的补充完整:
实验
编号
| 铜片
质量/g
| 0.1mol・L-1的
硝酸体积/mL
| 硝酸铜
晶体/g
| 亚硝酸钠
晶体/g
| 实验目的
|
①
| 5
| 20
| _______
| _______
| 实验①和②探究_________的影响;实验①和③探究亚硝酸根的影响。
|
②
| 5
| 20
| 0.5
| 0
|
③
| 5
| 20
| 0
| 0.5
|
4、选择题 等质量的铁与过量的盐酸在不同的实验条件下进行反应,测定在不同时间t产生氢气体积V的数据,根据数据绘制得下图,则曲线a、b、c、d所对应的实验组别可能是?
 ?
? 
[? ]
A.4-3-2-1
B.1-2-3-4
C.3-4-2-1
D.1-2-4-3
5、选择题 在容积不变的密闭容器中发生反应:2A(g)+B(g)?2C(g)△H<0.某研究小组进行了当其他条件不变时改变某一条件对上述反应影响的研究.下列关于图象的分析正确的是( )
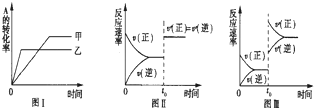
①图Ⅰ研究的是温度对化学平衡韵影响,且乙的温度高于甲的温度?
②图Ⅱ研究的是催化剂对反应速率的影响,化学平衡不移动?
③图Ⅱ研究的是t0时刻通入氦气增大体系压强对反应速率的影响?
④图Ⅲ研究的是t0时刻增大B的浓度对反应速率的影响.
A.①②
B.②③
C.②④
D.③④