微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
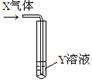
1、选择题 将X气体通入Y溶液中,实验结果与预测的现象一致的组合是
?
| X气体
| Y溶液
| 预测的现象
| 
|
①
| CO2
| 饱和Na2CO3溶液
| 白色沉淀析出
|
②
| SO2
| Ba(NO3)2溶液
| 白色沉淀析出
|
③
| Cl2
| AgNO3溶液
| 白色沉淀析出
|
④
| NH3
| AlCl3溶液
| 白色沉淀析出
|
?
A.只有①②③?B.只有①②④? C.只有①③④? D.①②③④
参考答案:D
本题解析:
试题分析:①将CO2通入到饱和Na2CO3溶液中发生化学反应:CO2+H2O+ Na2CO3=2NaHCO3,NaHCO3比Na2CO3的溶解度小,因此有沉淀析出,正确;②SO2和水反应可以生成H2SO3,溶液显酸性,Ba(NO3)2可以电离出NO3-,在酸性溶液中具有强氧化性,因此SO2与Ba(NO3)2不可能发生简单的复分解反应,SO2通入到Ba(NO3)2溶液中可发生氧化还原反应:3SO2+2H2O+2NO3-=3SO42- 十4 H++2NO↑,SO42-+Ba2+=BaSO4↓,错误;③Cl2+H2O=HCl+HClO,HCl+AgNO3=AgCl↓+HNO3,正确;④NH3 +H2O= NH3・H2O,3NH3・H2O+AlCl3=Al(OH)3↓+3NH4Cl,正确。故答案为D。3-在酸性条件下具有强氧化性以及H2SO3具有还原性的性质。)。
本题难度:一般
2、实验题 实验室用MnO2和浓盐酸制取氯气并验证氯气的部分性质,实验装置如下图所示。
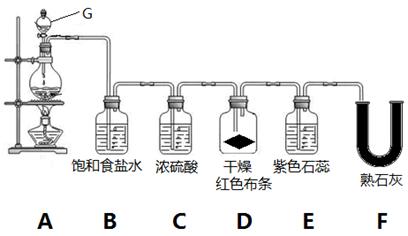
(1)G装置名称___________________。A装置的离子反应化学方程式是?,氧化剂与还原剂的物质的量之比为?。
(2)B装置的作用是_____________。
(3)实验开始几分钟后,D装置红布条是否褪色__________,E装置中观察到的现象是_____________
_____________________________________________________________。
(4)装置F中发生反应的化学方程式是_____________________________________________________。(5)F装置后应再连接一个尾气处理装置,装置里加入NaOH溶液,尾气处理的离子反应方程式为_____
____________________________________________________。
参考答案:(1)分液漏斗(1分)?MnO2+4H++2Cl- Mn2++Cl2↑+2H2O(2分)?1:2?(1分)
Mn2++Cl2↑+2H2O(2分)?1:2?(1分)
(2)除氯气中的氯化氢(1分)?(3) 不褪色,?(1分)?先变红后褪色?(1分)
(4)2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O?(2分) (5)Cl2+2OH-=Cl-+ClO-+H2O?(2分)
本题解析:(1)根据装置的特点可知,G装置是分液漏斗;A装置是制备氯气的,反应的离子反应方程式是MnO2+4H++2Cl- Mn2++Cl2↑+2H2O。其中二氧化锰中Mn元素的化合价从+4价降低到+2价,得到2个电子,二氧化锰是氧化剂。氯化氢中氯元素的化合价从-1价升高到0价,失去1个电子,氯化氢是还原剂。根据电子得失守恒可知,氧化剂与还原剂的物质的量之比是1:2。
Mn2++Cl2↑+2H2O。其中二氧化锰中Mn元素的化合价从+4价降低到+2价,得到2个电子,二氧化锰是氧化剂。氯化氢中氯元素的化合价从-1价升高到0价,失去1个电子,氯化氢是还原剂。根据电子得失守恒可知,氧化剂与还原剂的物质的量之比是1:2。
(2)由于浓盐酸易挥发,生成的氯气中含有氯化氢,所以B装置的作用是除氯气中的氯化氢。
(3)由于生成的氯气先经过浓硫酸被干燥,干燥的氯气不能使有色布条褪色,所以实验开始几分钟后,D装置红布条不褪色。氯气溶于水生成盐酸和次氯酸,溶液具有酸性和强氧化性,所以E装置中观察到的现象是先变红后褪色。
(4)氯气是酸性气体,与熟石灰反应生成氯化钙、次氯酸钙和水,反应的化学方程式为2Cl2+2Ca(OH)2=CaCl2+Ca(ClO)2+2H2O。
(5)氯气有毒需要尾气处理,氯气和氢氧化钠溶液反应生成氯化钠、次氯酸钠和水,反应的离子方程式为Cl2+2OH-=Cl-+ClO-+H2O。
本题难度:一般
3、选择题 生活中的某些问题,常涉及到化学知识,下列分析不正确的( )
A.冰箱中使用的含氟制冷剂泄漏后,会破坏臭氧层
B.Cl2和SO2都有漂白作用,都可以使有色棉布褪色
C.减少硫的氧化物和氮氧化物向空气中的排放,是防止酸雨形成的有效措施
D.严格地讲实验室使用排风扇是种不负责任的防污染手段,因为产生的有害气体没有得到转化或吸收
参考答案:A.臭氧层在氟氯代烃的催化作用下可转化为氧气,破坏臭氧层,应减少使用,故A正确;
B.干燥的氯气不具有漂白性,不能使有色布条褪色,故B错误;
C.硫的氧化物和氮氧化物可导致酸雨,应减少硫的氧化物和氮氧化物向空气中的排放,故C正确;
D.实验室使用排风扇,可减少实验室污染,但没有使有害气体转化和吸收,是一种不负责任的做法,故D正确.
故选B.
本题解析:
本题难度:简单
4、选择题 有一混合溶液,其中只含有Fe2+、Cl-、Br-、I-(忽略水的电离),Cl-、Br-、I-的个数比为2:3:4,向该溶液中通入氯气使溶液中Cl-和Br-的个数比为3:1,则通入氯气的物质的量与溶液中剩余Fe2+的物质的量之比为( )
A.7:4
B.7:3
C.7:2
D.7:1
参考答案:由题意可设Cl-、Br-、I-的物质的量分别为2mol、3mol、4mol,
由电荷守恒可得:2n(Fe2+)=n(Cl-)+n(Br-)+n(I-)=2mol+3mol+4mol=9mol,n(Fe2+)=4.5mol,通入氯气后,要满足 n(Cl-):n(Br-)=3:1,
Cl-只要增加7mol就可以,即需通入氯气3.5mol.4mol I-先消耗2mol氯气,3mol Fe2+消耗1.5mol氯气,
剩余Fe2+1.5mol,则通入氯气与剩余Fe2+的物质的量之比为:3.5:1.5=7:3,
故选B.
本题解析:
本题难度:一般
5、选择题 某混合气体可能含有N2、HCl和CO,把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体的体积都没有变化。再通过足量的Na2O2固体,气体体积减小。最后通过灼热的铜网,经充分反应后气体体积又减小,但还有剩余气体。以下对混合气体组成的判断,正确的是
A.一定没有N2,CO和HCl中至少有一种
B.一定有N2、HCl和CO
C.一定有N2,CO和HCl中至少有一种
D.一定有N2和HCl,没有CO
参考答案:C
本题解析:因为反应到最后还有剩余的气体,因此一定含氮气。再通过足量的Na2O2固体,气体体积减小,证明在这之前产生了二氧化碳。最后通过灼热的铜网,经充分反应后气体体积又减小,表明一定含有二氧化碳,二氧化碳跟过氧化钠产生的氧气与铜反应了。把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体的体积都没有变化,有三种情况:一是氮气、氯化氢,氯化氢跟碳酸氢钠反应生成与氯化氢体积相等的二氧化碳,二是氮气、一氧化碳, 一氧化碳与灼热的氧化铜反应生成等体积的二氧化碳,三是氮气、一氧化碳、氯化氢三种混和气体,综上所述,选C。
本题难度:一般