微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 在一定温度下,反应A2(g)+B2(g)  ?2AB(g)达到平衡的标志是(?)
?2AB(g)达到平衡的标志是(?)
A.单位时间内消耗n mol A2,同时生成2n mol AB
B.容器内总压强不随时间改变
C.单位时间内生成2n mol AB同时生成n mol B2
D.任何时间内A2、B2的物质的量之比为定值
参考答案:C
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态。A中反应速率的方向是相同的,速率之比是相应的化学计量数之比,因此A中的关系始终是成立,不正确。反应前后气体的体积不变,因此气体的总物质的量、体积和压强始终是不变的,B不能说明。C中反应速率的方向相反,且满足速率之比是相应的化学计量数之比,正确。由于不能确定反应物的起始浓度,所以D不能说明,因此答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可。
本题难度:一般
2、选择题 可逆反应2SO2+O2 2SO3达平衡后,通18O2气体,再次达平衡时,18O存在于(?)
2SO3达平衡后,通18O2气体,再次达平衡时,18O存在于(?)
A.SO3、O2
B.SO2、SO3
C.SO2、SO3、O2
D.SO3、O2
参考答案:C
本题解析:平衡的特征之一是动态平衡,反应可逆,因此,加入18O2后,SO2、SO3、O2中均含有18O。
本题难度:简单
3、计算题 将等物质的量的A、B混合于2L的密闭容器中,发生下列反应3A(g)+B(g) xC(g)+2D(g),经反应5min后,测知D的浓度为0.5mol/L,A、B的物质的量浓度之比为3∶5,C的平均反应速率是
xC(g)+2D(g),经反应5min后,测知D的浓度为0.5mol/L,A、B的物质的量浓度之比为3∶5,C的平均反应速率是
0.1mol/(L・min),试计算:
(1)x的值?
(2)5min内B的平均反应速率?
(3)5min时A的物质的量浓度?
参考答案:(1)2
(2)0.05mol・L-1・min-1
(3)0.75 mol・L-1
本题解析:
本题难度:一般
4、选择题 在体积不变的密闭容器中,2NO2(g) 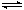 ?N2O4(g) 达到平衡的标志是
?N2O4(g) 达到平衡的标志是
①消耗1 mol NO2的同时消耗1 mol N2O4 ?②容器内NO2 和N2O4的物质的量相等
③混合气体的颜色不再改变?④容器内NO2的物质的量浓度不再变化
A.①②
B.①②③
C.③④
D.①③④
参考答案:C
本题解析:在一定条件下,当可逆反应的正反应速率和逆反应速率相等时(但不为0),反应体系中各种物质的浓度或含量不再发生变化的状态,称为化学平衡状态,所以选项④正确。颜色的深浅和浓度有关系,混合气体的颜色不再改变,说明NO2的浓度不再发生变化,所以选项③可以说明。①中反应速率的方向相反,但不能满足速率之比是相应的化学计量数之比,不能说明。平衡时各种物质的浓度不再发生变化,但各种的浓度之间不一定满足某种关系,②不能说明,因此答案选C。
点评:该题是中等难度的试题,也是高考中的常见题型和考点。试题基础性强,难易适中,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力。该题的关键是明确平衡状态的特点,然后结合具体的可逆反应灵活运用即可。
本题难度:一般
5、选择题 在一定温度下的定容容器中,当下列物理量不再改变时,表明反应:A (s)+2B (g) 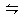 ?C(g)+ D(g)已达到平衡的是? (? )
?C(g)+ D(g)已达到平衡的是? (? )
A.混合气体的压强
B.混合气体的密度
C.B的物质的量浓度
D.气体的总物质的量
参考答案:BC
本题解析:由于反应前后方程式的系数不变,故在一定温度下的定容容器中,混合气体的压强及气体的总物质的量始终不变,所以A、D选项不正确;而反应前后气体的质量发生改变,气体的总物质的量,则混合气体的密度也会改变,它不变时可标明反应已达平衡状态,B正确;在反应的容器不变的情况下,某一物质的浓度不变,说明该物质的物质的量不变,则可说明反应已达平衡状态,故C选项正确。
本题难度:一般