微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 钢铁生锈过程发生如下反应:
①2Fe+O2+2H2O=2Fe(OH)2;
②4Fe(OH)2+O2+2H2O=4Fe(OH)3;
③2Fe(OH)3=Fe2O3+3H2O。
下列说法正确的是
A.反应①、②中电子转移数目不相等
B.反应①中还原剂是氢氧化亚铁
C.反应①属于析氢腐蚀
D.可将地下输油钢管与外加直流电源的负极相连以保护它不受腐蚀
参考答案:
D
本题解析:略
本题难度:简单
2、选择题 下列叙述正确的是
①锌跟稀硫酸反应制取氢气,加入少量硫酸铜溶液能加快反应速率?
②镀层破损后,白铁(镀锌的铁)比马口铁(镀锡的铁)更易腐蚀
③电镀时,应把镀件置于电解槽的阴极
④冶炼铝时,用电解熔融氧化铝的方法
⑤钢铁表面常易锈蚀生成Fe2O3?nH2O?
A.①②③④⑤
B.①③④⑤
C.①③⑤
D.②④
参考答案:B
本题解析:①当加入少量硫酸铜溶液时发生:Zn+Cu2+=Zn2++Cu,锌、铜跟稀硫酸构成了原电池,能加快反应速率。正确。②镀层破损后,由于活动性Zn>Fe>Sn,在白铁中Fe作正极,马口铁中Fe作负极,故马口铁(镀锡的铁)更易腐蚀。错误。③电镀时镀件作电解槽的阴极,镀层金属作阳极,含有镀层金属的离子的溶液作电镀液。正确。④由于Al的活动性很强,所以在冶炼铝时,用电解熔融氧化铝的方法。正确。⑤钢铁腐蚀主要是吸氧腐蚀。产物是Fe2O3?nH2O。正确。
本题难度:一般
3、填空题 如图所示,水槽中试管内有一枚铁钉,放置数天观察:
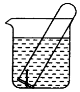
(1)铁钉在逐渐生绣。
(2)若试管内液面上升,发生?腐蚀,电极反应:
负极:?,正极:?。
(3)若试管内液面下降,则原溶液呈?性,发生的电极反应:
正极:?。
参考答案:(2)吸氧;2Fe-4e- = 2Fe2+? O2+2H2O+4e=4OH-
(3)较强的酸性2H+ + 2e - = H2↑
本题解析:(2)若试管内液面上升,说明试管内压强降低,所以发生的是吸氧腐蚀。负极是铁失去电子,正极是氧气得到电子,所以电极反应式分别是2Fe-4e- = 2Fe2+、O2+2H2O+4e=4OH-。
(3)若试管内液面下降,说明试管内氧气增大,有气体生成,所以发生的是析氢腐蚀,因此溶液的首先较强。正极反应式为2H+ + 2e - = H2↑。
本题难度:一般
4、选择题 关于下图的说法正确的是 (? )
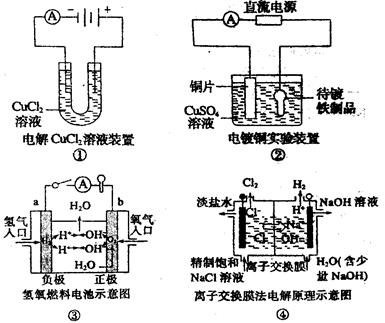
A.①装置中阴极处产生的气体能够使湿润淀粉KI试纸变蓝
B.②装置中待镀铁制品应与电源正极相连
C.③装置中电子由b极流向a极
D.④装置中的离子交换膜可以避免生成的Cl2与NaOH溶液反应
参考答案:D
本题解析:①装置中阴极氢离子放电,生成氢气,A不正确。电镀时待镀铁制品应与电源负极相连,B不正确。原电池中电子从负极流向正极,即从a极流向b极,C不正确。所以选项D是正确的,答案选D。
本题难度:一般
5、填空题 (9分)下图所示水槽中试管内有一枚铁钉,放置数天后观察:
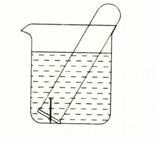
(1)铁钉在逐渐生锈,则铁钉的腐蚀属于?腐蚀。
(2)若试管内液面上升,则原溶液呈?性,发生?腐蚀,正极反应式为?。
(3)若试管内液面下降,则原溶液呈?性,发生?腐蚀,正极反应式为?。
参考答案:(9分)
(1)电化学(2)弱酸性或中;吸氧);O2+2H2O+4e―====4OH―
(3)较强的酸;析氢;2H++2e―===H2 ↑
本题解析:(1)铁钉表面形成无数个微小的铁碳原电池,属于电化学腐蚀;
(2)若试管内液面上升,说明发生了吸氧腐蚀,溶液呈弱碱性,相关方程式:正极:O2+2H2O+4e―====4OH―;负极:Fe? -2e-=Fe2+;
(3)若试管内液面下降,说明发生了析氢腐蚀,溶液呈酸性;相关方程式:正极:2H++2e―===H2 ↑;负极:Fe? -2e -=Fe2+?。
本题难度:一般