��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �������ж�����Ԫ�����ʵ����ݣ�
?Ԫ�ر��
Ԫ������
| ��
| ��
| ��
| ��
| ��
| ��
| ��
|
ԭ�Ӱ뾶
| 0.74
| 1.60
| 1.52
| 1.10
| 0.99
| 1.86
| 0.75
|
����ϼ�
| ?
| +2
| +1
| +5
| +7
| +1
| +5
|
��ͻ�����
| ��2
| ?
| ?
| ��3
| ��1
| ?
| ��3
|
����˵����ȷ���ǣ�?��
A. ��һ�����ܣ��� > ��? B. �縺�ԣ��� < ��
C. ��Ӧ���ӵİ뾶�� �� >��> ��
D. ��̬�⻯����ȶ��Ժͷе㣺�ߩ���
�ο��𰸣�B
�������������ԭ�Ӱ뾶�������ͻ��ϼۿ����жϢ���O������Mg������Li������P������Cl������Na������N��
A:Nԭ�����ڰ����״̬���ʵ�һ�����ܵ�������
B��þΪ���ý�������PΪ�ǽ������縺���״���þ
C���������ӵĺ�������Ų���ͬ���˵����Խ�����Ӱ뾶ԽС�������� >��> ��
D��NԪ�صķǽ�����ǿ��P����NH3�ȶ���ǿ����PH3�����ڰ������Ӽ������������е�Ҳ��Խϸ�
�ʴ�ΪB
�����Ѷȣ�һ��
2��ѡ���� ���з�ɢϵ�У���ɢ������ֱ��������
A.��
B.ʯ����
C.������������
D.ʳ��ˮ
�ο��𰸣�B
���������ʯ����������Һ������ֱ�����
�����Ѷȣ���
3��ѡ���� ����������ȷ���ǣ�?��
A�����Ӳ����ٵ�Ԫ��ԭ�Ӱ뾶һ��С�ڵ��Ӳ������Ԫ�ص�ԭ�Ӱ뾶
B��������Ӳ�ṹ��ͬ�ĵ������뾶��ͬ
C����������ͬ�IJ�ͬ��������������Խ�࣬�뾶Խ��
D��ԭ������Խ��ԭ�Ӱ뾶Խ��
�ο��𰸣�C
�������������ͬ��������Ԫ��ԭ�Ӱ뾶��С���ʢ�A���ԭ�Ӱ뾶��һ������һ���ڢ�A��Ԫ��ԭ�Ӱ뾶����r(Li)>r(S)>r(Cl)������A����ȷ�����ں�����Ӳ�ṹ��ͬ�ĵ������Ӻ�ԭ�ӣ��뾶�Dz�ͬ�ģ�����B����ȷ����������ͬ�IJ�ͬ�������������Ӱ뾶>ԭ�Ӱ뾶>�����Ӱ뾶������C��ȷ������ԭ������������ԭ�Ӱ뾶����һֱ�����dz��������Ա仯������D����ȷ����ѡC��
���������⿼��Ԫ�����ڱ�������Ԫ�����ʵĵݱ���ɣ�ԭ�Ӱ뾶���������жϣ���Ŀ�Ѷ��еȡ�
�����Ѷȣ�һ��
4��ѡ���� �������е�A��B��C��D��E����Ԫ�أ�ԭ��������������A��D��C��E�ֱ�ͬ���壬AΪ�ǽ���Ԫ�أ���A��B��ԭ������֮�͵���C��ԭ��������C2����D���ĺ����������ȡ�������˵����ȷ����
A��B��Aֻ���γɻ�����BA3?
B��C��ԭ�Ӱ뾶�����Ӱ뾶���ֱ�С��D��ԭ�Ӱ뾶�����Ӱ뾶
C��A��B��C�γɵĻ�������ܴٽ�ˮ�ĵ��룬Ҳ��������ˮ�ĵ���?
D��A��D������C�γ�ԭ�Ӹ�����Ϊ1�U1��2�U1�Ļ������A2C2��D2C2�Ļ�ѧ��������ͬ
�ο��𰸣�C
�����������C��Eͬ���壬����C2������C��O��E��S��C2����D���ĺ����������ȣ�D��Na��A��Dͬ���壬AΪ�ǽ���Ԫ�أ�A��H��A��B��ԭ������֮�͵���C��ԭ��������B��N��A��B��A�γɻ�����NH3��N2H4�ȣ�B��Na��ԭ�Ӱ뾶����O��Na+���Ӱ뾶С��O2-�뾶��C��A��B��C�γɵĻ�����ΪHNO3��HNO2�ܴٽ�ˮ�ĵ��룬NH4NO3��NH4NO2������ˮ�ĵ��룻D��H2O2��ѧ�������Ǽ��Լ��ͷǼ��Լ���Na2O2�Ļ�ѧ�����������Ӽ��ͷǼ��Լ���
�����Ѷȣ�һ��
5��ѡ���� ijЩ�������Ϻ��з�����Ԫ���(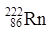 )������������һ��Σ������ԭ������������������֮���ǣ�?��
)������������һ��Σ������ԭ������������������֮���ǣ�?��
A��136
B��50
C��86
D��222
�ο��𰸣�B
����������ڱ�ʾԭ�����ʱԪ�ط��ŵ����½DZ�ʾ�����������ϽDZ�ʾ����������Ϊ��������������֮�������������Һ���������������������Ը�ԭ�Ӻ�������������������֮��222��86��86��50����ѡB��
�����������Ǹ߿��еij������ͣ����ڻ���������Ŀ��飬���ض�ѧ������֪ʶ�Ĺ��̺�ѵ��������Ĺؼ�����ȷԭ����ɵı�ʾ�������Լ��й���֮���������ϵ������������ü��ɡ�
�����Ѷȣ���