| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《水的电离平衡》高频考点预测(2017年最新版)(八)
参考答案:A 本题解析:略 本题难度:一般 2、填空题 某学生用0.10 mol/L标准NaOH溶液滴定某浓度的盐酸。记录数据如下:
(1)滴定时选用酚酞试液作指示剂,如何判断滴定达到终点 。 (2)盐酸的物质的量浓度为_____________ (3)碱式滴定管尖嘴部分有气泡,滴定后消失,对测定结果的影响是 (填“偏高”或“偏低”或“无影响”,下同)。 (4)某同学用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,高锰酸钾溶液应盛放在 中(填“甲”或“乙”),该反应的离子方程式为: 。 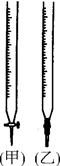 参考答案:(1)当滴入最后一滴标准液,溶液由无色变为浅红色,且半分钟内不退色 本题解析:(1)因为这是由已知浓度的碱滴定未知浓度的酸,酚酞指示剂在酸溶液中,是无色的,随着碱的滴加,溶液的酸性逐渐减弱,当滴加到最后一滴时,溶液由无色变为浅红色,半分钟内不褪色时酸碱中和恰好完成。(2)碱溶液的平均体积为V=(V1+V2+V3)÷3=" ((20.54-0.05)+(26.00-6.00)" +(21.36-1.40)) ÷3=20.00ml,利用酸碱恰好发生中和反应时C酸?V酸=C碱?V碱,C酸="(" C碱?V碱) ÷V酸="(0.10" mol/L×20.00ml) ÷20.00ml="0.10mol/L." (3)若在滴定前碱式滴定管尖嘴部分有气泡,滴定后消失,碱溶液的体积偏大,以此为标准计算的酸的浓度偏高。(4)若用已知准确浓度的高锰酸钾溶液滴定溶液中Fe2+的浓度,由于高锰酸钾溶液有强的氧化性,容易腐蚀碱式滴定管的橡胶管,所以应盛放在酸式滴定管甲中,发生该反应的离子方程式为5Fe2+ + MnO4- + 8H+ = 5Fe2+ + Mn2+ + 4H2O。 本题难度:一般 3、选择题 将pH=8和NaOH固体分别加入pH=10的两种NaOH溶液等体积混合后,溶液中c(H+)最接近 | |||||||||||||||||||
参考答案:D
本题解析:pH=8的NaOH溶液中c(OH-)=10-6 mol・L-1,pH="10" NaOH溶液中 c(OH-)=10-4 mol・L-1混合后c(OH-)=(10-6+10-4)/2,则溶液中的(H+)=10-14÷(10-6+10-4)/2=2×10-10mol・L-1(两数值相加时,如果相差100倍,小的数值可以忽略不计
考点:混合溶液的离子浓度计算。
本题难度:一般
4、实验题 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择甲基橙作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的NaOH溶液时,左手握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 ,直到最后加入一滴盐酸后,溶液由 色变为 ,且 为止。
(2)下列操作中可能使所测NaOH溶液的浓度数值偏低的是________
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放NaOH溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
(3)若滴定开始和结束时,酸式滴定管中的液面如图所示,则反应消耗盐酸的体积为________ mL,
(4)某学生根据3次实验分别记录有关数据如下表:
| 滴定 次数 | 待测NaOH溶液的体积/mL | 0.100 mol/L盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.20 | 20.22 | |
| 第二次 | 25.00 | 0.56 | 24.54 | |
| 第三次 | 25.00 | 0.42 | 20.40 | |
参考答案:锥形瓶内溶液颜色的变化(1分) 黄色(1分) 橙色(1分)半分钟不变色(1分)
(2)D(1分) (3)20.00mL(1分) (4)0.0800 mol/L(2分)
本题解析:(1)酸碱中和滴定时,眼睛要注视锥形瓶内溶液的颜色变化,滴定终点时溶液颜色由黄色突变为橙色,且半分钟内不褪色.(2)A、酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)=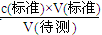 可知,测定c(NaOH)偏大,故A不符合。B、滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=
可知,测定c(NaOH)偏大,故A不符合。B、滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥,待测液的物质的量不变,对V(标准)无影响,根据c(待测)=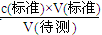 可知,测定c(NaOH)无影响,故B不符合;C选项酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=
可知,测定c(NaOH)无影响,故B不符合;C选项酸式滴定管在滴定前有气泡,滴定后气泡消失,造成V(标准)偏大,根据c(待测)=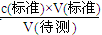 可知,测定c(NaOH)偏大,故C不符合;D选项,读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,造成V(标准)偏小,根据c(待测)=
可知,测定c(NaOH)偏大,故C不符合;D选项,读取盐酸体积时,开始仰视读数,滴定结束时俯视读数,造成V(标准)偏小,根据c(待测)=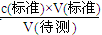 可知,测定c(NaOH)偏低,故D符合;(3)起始读数为0.10mL,终点读数为20.10mL,盐酸溶液的体积为20.00mL。(4)根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(盐酸)=20.00mL,
可知,测定c(NaOH)偏低,故D符合;(3)起始读数为0.10mL,终点读数为20.10mL,盐酸溶液的体积为20.00mL。(4)根据数据的有效性,舍去第2组数据,然后求出1、3组平均消耗V(盐酸)=20.00mL,
HCl +NaOH = NaCl +H2O
0.0200L×0.1000mol/L 0.025L×C(NaOH)
则C(NaOH)=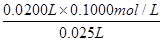 =0.0800 mol/L
=0.0800 mol/L
考点:酸碱中和滴定,物质的量浓度计算。
本题难度:一般
5、选择题 25℃时,在等体积的 ① pH=0的H2SO4溶液、② 0.05 mol/L的Ba(OH)2溶液、③ pH=10的Na2S溶液、④ pH=5的NH4NO3溶液中,发生电离的水的物质的量之比是
[? ]
A.1∶10∶1010∶109
B.1∶5∶5×109∶5×108
C.1∶20∶1010∶109
D.1∶10∶104∶109
参考答案:A
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点总结《碳族元素》.. | |