��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �谢���ӵ�����ΪNA������˵����ȷ����
[? ]
A. ���³�ѹ�£�NA��CO2���ӵ�����Ϊ44 g
B. 8 g?CH4�У����еĵ�����ĿΪ4NA��
C. 1.12 L Cl2(g)�У����е�ԭ����ĿΪ0.1NA
D. 0.1 mol/L��Na2CO3��Һ�У�����0.2NA��Na+
�ο��𰸣�A
���������
�����Ѷȣ���
2��ѡ���� ���ڡ�12��̼-12��������˵��������ǣ�������
A�����а����ӵ�������̼ԭ��
B������6�����Ӻ�6������
C������Լ6.02��1023��̼ԭ��
D������1mol̼ԭ��
�ο��𰸣�A������12g12C�к��а����ӵ�������̼ԭ�ӣ�Լ��6.02��1023������A��ȷ��
B������12g12C�к���6mol���Ӻ�6mol���ӣ�����6��6.02��1023�����Ӻ�6��6.02��1023�����ӣ���B����
C������12g̼���ʵ�����1mol������̼ԭ����Լ��6.02��1023����C��ȷ��
D��12C��Ħ��������12g/mol��12g̼���ʵ�����1mol����D��ȷ��
��ѡB��
���������
�����Ѷȣ�һ��
3��ѡ���� ��nA���������ӵ�������NA������ֵ������˵����ȷ����
A.1?mol?Na�ڿ�����ȼ�գ�ת�Ƶĵ�����Ϊ2?nA
B.�����£�2.7g������������������Һ��Ӧ��ʧȥ�ĵ�����Ϊ0.3?nA
C.0.10?mol?Fe?��������ˮ������Ӧ���ɵ�H2������Ϊ0.10?nA
D.11.2L?Cl2���е�ԭ����ΪNA
�ο��𰸣�B
���������������A��һ����ԭ��ʧȥһ�����ӣ�
B����ԭ��ʧȥ3�������γ�ƫ�����������n=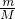 �����������ʵ������ٸ���N=nNA����ʧȥ�ĵ�������
�����������ʵ������ٸ���N=nNA����ʧȥ�ĵ�������
C�����ݷ���ʽ3Fe+4H2O��g�� Fe3O4+4H2���⣻
Fe3O4+4H2���⣻
D������������״̬��һ���DZ�״����
���A��һ����ԭ��ʧȥһ�����ӣ�1?mol?Na�ڿ�����ȼ�գ�ת�Ƶĵ�����Ϊ?nA����A����
B��2.7g��������������������Һ��Ӧʧȥ�ĵ�����Ϊ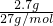 ��3��NAmol-1=0.3NA����B��ȷ��
��3��NAmol-1=0.3NA����B��ȷ��
C�����ݷ���ʽ3Fe+4H2O��g�� Fe3O4+4H2��0.1 mol Fe����������ˮ������Ӧ����H2�ķ�����Ϊ
Fe3O4+4H2��0.1 mol Fe����������ˮ������Ӧ����H2�ķ�����Ϊ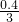 NA����C����
NA����C����
D������������״̬��һ���DZ�״��������ʹ������Ħ�����22.4L/mol�������������ʵ�����ԭ��������D����
��ѡB��
���������⿼���˰���٤��������Ӧ�ã��ѶȲ���ע�����֪ʶ�Ļ��ۣ�
�����Ѷȣ�һ��
4��ѡ���� ��NA��������ӵ�����������˵����ȷ���ǣ�������
A��2.3�˽����Ʊ�Ϊ������ʱʧȥ�ĵ�����ĿΪ0.1NA
B��18��ˮ�����ĵ�����ĿΪNA
C���ڳ��³�ѹ��11.2������������ԭ����ĿΪNA
D��32������������ԭ����ĿΪNA
�ο��𰸣�A��2.3g �Ƶ����ʵ���Ϊ��2.3g23g/mol=0.1mol����Na��Na+ʧȥһ�����ӣ���2.3�˽����Ʊ�Ϊ������ʱʧȥ�ĵ�����ĿΪ0.1NA����A��ȷ��
B��18��ˮ�����ʵ���Ϊ��18g18g/mol=1mol��1��H2O��������Ϊ��2��1+8�T10����18��ˮ�����ĵ�����ĿΪ10NA����B����
C�����³�ѹ�£����Ħ���������22.4L/mol����11.2�����������ʵ�������0.5mol��������ԭ����ĿҲ����NA����C����
D��32�����������ʵ���Ϊ��32g32g/mol=1mol�������ķ���ʽΪ��O2����������ԭ����ĿΪ2NA����D����
��ѡ��A��
���������
�����Ѷȣ���
5��ѡ���� NAΪ�����ӵ���������ֵ������˵������ȷ���ǣ�������
A�����ܱ������м���l.5mol?H2��0.5molN2����ַ�Ӧ��õ�NH3������ΪNA
B��һ�������£�2.3g��Na��ȫ��O2��Ӧ����3.6g����ʱʧȥ�ĵ�����Ϊ0.1NA
C��1.0L��0.1?mol?L-1Na2S��Һ�к��е�S2-������Ϊ0.1NA
D����״���£�22.4L��CCl4�к��е�CCl4������ΪNA
�ο��𰸣�A�������͵�����Ӧ���ɰ����ǿ��淴Ӧ�����ܽ��г� �ף����ܱ������м���l.5mol H2��0.5molN2����ַ�Ӧ��õ�NH3������С��NA����A����
B��һ�������£�2.3g��Na���ʵ�����Ϊ0.1mol����ȫ��O2��Ӧʧ����Ϊ0.1mol����������3.6g����ʱʧȥ�ĵ�����Ϊ0.1NA����B��ȷ��
C��1.0L��0.1 mol?L-1Na2S��Һ�У�������ˮ����٣�������Һ�к��е�S2-������С��0.1NA����C����
D����״���£�CCl4�������壬22.4L��CCl4���ʵ�������1mol����D����
��ѡB��
���������
�����Ѷȣ���