��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1������� ����������ˮ�в��ֵ��������ڵ���ʵ��ǣ�������
A��NaOH
B��CH3COOH
C��H2SO4
D��CO2
�ο��𰸣�A��NaOH��ˮ������ȫ���룬��ˮ��Һ���磬���ڵ���ʣ���A����
B��CH3COOH�����ᣬ��ˮ���ܲ��ֵ��룬����ˮ��Һ���磬��CH3COOH���ڵ���ʣ���B��ȷ��
C��H2SO4��ǿ�ᣬ��ˮ������ȫ���룬����ˮ��Һ���磬���������ڵ���ʣ���C����
D��CO2��ˮ��Һ�ܵ��磬���������̼��ˮ��Ӧ����̼�ᣬ̼������������Ӷ����磬���������벻��CO2��������CO2���ڷǵ���ʣ���D����
��ѡB��
���������
�����Ѷȣ�һ��
2��ѡ���� �Ҵ���Һ����ˮ�����Է�����ż���룬��H2O+H2O?H3O++OH-��NH3+NH3?NH4++NH2-��������������ȷ���ǣ�������
A���Ҵ��ĵ��뷽��ʽ��2CH3CH2OH?CH3CH2OH2++CH3CH2O-
B��Һ�������ӻ�����Ϊ��1.0��10-28����Һ��Ũ��Ϊ1.0��10-14mol/L
C����������pH�൱�Ķ������涨pOH��pNH2-�ȣ����Ҵ�����pH�൱��Ϊ-lgc��CH3CH2OH2+��
D���Ҵ���KW=c��CH3CH2OH2+����c��CH3CH2O-��=1.0��10-30�����ʱ��p?CH3CH2O-=-15
�ο��𰸣�A��������ż��ʵ���Ƿ��ӽ����һ���ӵ��������γ������ӣ���һ�����γ������ӷ������룬�Ҵ��ĵ��뷽��ʽ��2CH3CH2OH?CH3CH2OH2++CH3CH2O-����A��ȷ��
B��Һ�������ӻ�����Ϊ��1.0��10-28�����ӻ��������ˮ�����ӻ�����д����[NH4+][NH2-]=1.0��10-28�����ݵ��뷽��ʽ��֪��NH3+NH3?NH4++NH2-����[NH4+]=[NH2-]=1.0��10-14mol/L������Һ��Ũ�ȴ���1.0��10-14mol/L����B����
C��ˮ��Һ��pH=-lg[H+]��pOH=-lg[OH-]��������pPH���õ������������Ũ�ȵĸ��������㣬�Ҵ�����pH�൱��Ϊ-lgc��CH3CH2OH2+������C��ȷ��
D���Ҵ���KW=c��CH3CH2OH2+����c��CH3CH2O-��=1.0��10-30�����뷽��ʽΪ2CH3CH2OH?CH3CH2OH2++CH3CH2O-���õ�c��CH3CH2OH2+��=c��CH3CH2O-��=1.0��10-15����ʱ��p?CH3CH2O-=-lg[1.0��10-15]=15����D����
��ѡAC��
���������
�����Ѷȣ�һ��
3��ѡ���� ��֪25��ʱ���������ʵĵ��볣����С˳��Ϊ��H2SO3(һ������)��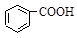 ��HSO3����
��HSO3����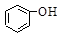 ˮ���ᣨ
ˮ���ᣨ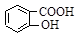 ��������������Һ��Ӧ�����ܷ�����Ӧ�����ӷ���ʽ��д��ȷ����
��������������Һ��Ӧ�����ܷ�����Ӧ�����ӷ���ʽ��д��ȷ����
A��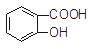 + SO32�D��
+ SO32�D��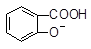 + HSO3�D
+ HSO3�D
B��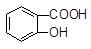 + SO32�D��
+ SO32�D��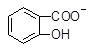 +HSO3�D
+HSO3�D
C��2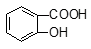 + SO32�D��2
+ SO32�D��2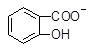 +SO2��+H2O
+SO2��+H2O
D��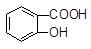 +2SO32�D��
+2SO32�D��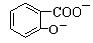 +2HSO3�D
+2HSO3�D
�ο��𰸣�B
������������ݵ��볣����С˳��A��Ӧ�����Ȼ�ʧȥ�����ӣ�������Ӧ������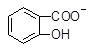 + HSO3�D����B��ȷ��C���ڵ��볣�� H2SO3(һ������)��
+ HSO3�D����B��ȷ��C���ڵ��볣�� H2SO3(һ������)��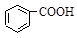 �ʲ���������SO2������D��ȷ��д��Ӧ����
�ʲ���������SO2������D��ȷ��д��Ӧ����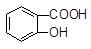 +SO32�D��
+SO32�D��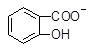 + HSO3�D������
+ HSO3�D������
�����Ѷȣ�һ��
4��ѡ���� ������ʵһ����˵��HNO2Ϊ������ʵ���
�ٳ�����Na NO2��Һ��PH��7 ��10mL1mol/L HNO2ǡ����10mL1mol/LNaOH��ȫ��Ӧ��HNO2��NaCl���ܷ�Ӧ��0.1mol/L HNO2��Һ��PH=2.1
A���٢ڢۢ� B���ڢۢ� C���٢� D���ڢ�
�ο��𰸣�C
�����������
�����Ѷȣ�һ��
5��ѡ���� ��ˮ������ƽ�⣺NH3��H2O  ?NH4+ + OH�C ��������������ʱ���ı�����������ƽ�������ƶ�����c(NH4+)������ǡ�
?NH4+ + OH�C ��������������ʱ���ı�����������ƽ�������ƶ�����c(NH4+)������ǡ�
A����NaOH��
B�������ᡡ
C����NH4Cl��
D������
�ο��𰸣�C
���������A����NaOH?����Һ��OH�C Ũ������Ӧ�����ƶ�����NH4+Ũ�Ȼ��С��A����B��������H++OH-? ?H2O����Һ�� OH�C Ũ�ȼ�С����Ӧ�������ƶ���B����D����ˮ�������ȣ����ȷ�Ӧ�����ƶ���D����ѡC��
?H2O����Һ�� OH�C Ũ�ȼ�С����Ӧ�������ƶ���B����D����ˮ�������ȣ����ȷ�Ӧ�����ƶ���D����ѡC��
���������⿼��ѧ��Ӱ�컯ѧƽ���ƶ������أ����Ը��ݽ̲�֪ʶ���ش��ѶȲ���
�����Ѷȣ�һ��