微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 浩瀚的海洋是一个巨大的宝库,蕴含有80多种元素,可供提取利用的有50多种。
(1)其中“氯碱工业”就是以食盐水为原料制取Cl2等物质,有关的化学方程式为:?。
(2)实验室用二氧化锰制取氯气的化学方程式为:?;根据上述实验原理,从下列装置中选择合适的发生装置用于实验室制取少量氯气?(填写装置的序号)。
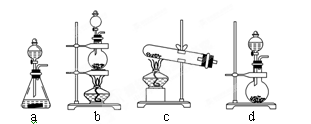
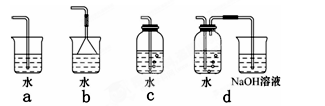
(3)实验室中模拟Br―→Br2的转化,可以通过在KBr溶液中滴加少量新制氯水的实验进行实现。写出Br―→Br2的转化离子方程式为:?;氯水不稳定,要现用现配,下列吸收氯气制备氯水的装置最合理的是?(选填下列选项的编号字母)。
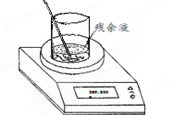
(4)实验室制备氯气的反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,探究小组同学进行了以下实验:取100 mL残余液放入烧杯中,将烧杯(含玻璃棒)放在电子天平上(如右图),再把已称好50.0 g CaCO3粉末慢慢加入到残余液中,边加边搅拌使其充分反应。观察读数变化如下表所示:
CaCO3用量
| 未加CaCO3时
| 加约四分之一时
| 加一半时
| 全部加完时
|
读数/g
| 318.3
| 325.3
| 334.5
| 359.5
|
请你据此分析计算:
①实验中产生的CO2气体质量为?;
②残余液中盐酸的物质的量浓度为 (结果精确到小数点后一位)?。
参考答案:(1)2NaCl+2H2O 2NaOH+H2↑+Cl2↑(2分)
2NaOH+H2↑+Cl2↑(2分)
(2)MnO2+4HCl(浓)  MnCl2+2H2O+Cl2↑(2分);b(1分)
MnCl2+2H2O+Cl2↑(2分);b(1分)
(3)2Br-+Cl2=2Cl-+Br2(2分);d(1分) (4)①8.8g(2分);②4.0mol/L(3分)
本题解析:(1)“氯碱工业”是以食盐水为原料,通过电解法制取Cl2等物质,有关的化学方程式为2NaCl+2H2O 2NaOH+H2↑+Cl2↑。
2NaOH+H2↑+Cl2↑。
(2)实验室用二氧化锰制取氯气的化学方程式为MnO2+4HCl(浓)  MnCl2+2H2O+Cl2↑。根据方程式可知该反应是固体与液体加热制备气体,因此需要的主要仪器是酒精灯、分液漏斗、烧瓶,则实验装置应该是装置b,即答案选b。
MnCl2+2H2O+Cl2↑。根据方程式可知该反应是固体与液体加热制备气体,因此需要的主要仪器是酒精灯、分液漏斗、烧瓶,则实验装置应该是装置b,即答案选b。
(3)氯气的氧化性强于单质溴的,能把溴离子氧化生成单质溴,所以Br―→Br2的转化离子方程式为2Br-+Cl2=2Cl-+Br2。氯气能溶于水,但溶解度很小。另外氯气有毒,需要尾气处理,可以用氢氧化钠溶液吸收,因此正确的答案选d。
(4)①根据质量守恒定律可知,反应中产生CO2的质量=318.3g+50.0g-359.5g=8.8g。
②CO2的物质的量=8.8g÷44g/mol=0.2mol,则根据方程式可知
CaCO3+2HCl=CaCl2+H2O+CO2↑
2mol? 1mol
0.4mol? 0.2mol
所以盐酸的浓度=0.4mol÷0.1L=4.0mol/L
本题难度:一般
2、实验题 实验室用下述装置制取氯气,并用氯气进行下列实验。 回答下列问题:
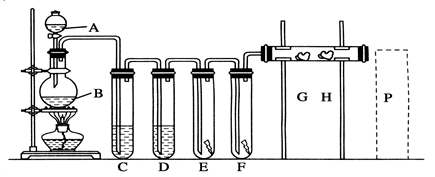
(1)A、B两仪器的名称:A_________________,B________________。
(2)洗气装置C是为了除去Cl2中的HCl气体,应放入的试剂是________________,D中浓H2SO4的作用是________________。
(3)E中为红色干布条,F中为红色湿布条,可看到有色布条褪色的是 _______。(填E或F)
(4)G是浸有淀粉KI溶液的棉花球,G处现象是棉花球表面变成______________。
H是浸有NaBr溶液的棉花球,H处反应的离子方程式是___________________________________________。
(5)P处为尾气吸收装置, 写出实验室利用烧碱溶液吸取Cl2的离子方程式: ___________________。
(6)B中发生反应的化学方程式为_______________________ ,若实验中使用12 mol・L-1的浓盐酸10 mL与足量的二氧化锰反应, 实际生成的Cl2的物质的量总是小于0.03 mol,试分析可能存在的原因是______________________________________________________。
参考答案:(1)分液漏斗 圆底烧瓶? (2)饱和食盐水 除去氯气中的水蒸气
(3)F ?(4)蓝色? 2 Br-+Cl2=2Cl-+Br 2
(5)Cl2+2OH-=Cl-+ClO-+H2O?
(6)MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O随着反应的进行,消耗氯化氢,同时生成水,且氯化氢挥发,使盐酸的浓度逐渐减小,稀盐酸与二氧化锰不反应。
MnCl2+Cl2↑+2H2O随着反应的进行,消耗氯化氢,同时生成水,且氯化氢挥发,使盐酸的浓度逐渐减小,稀盐酸与二氧化锰不反应。
本题解析:(1)由装置图示可知:A是分液漏斗;B是圆底烧瓶。(2)用浓HCl与MnO2在加热条件下发生反应MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O制取氯气。由于浓盐酸有挥发性,所以在氯气中含有杂质HCl。由于氯气在饱和食盐水中的溶解度小,所以为了除去Cl2中的HCl气体,应放入的试剂是饱和食盐水。此时产生的氯气中任然含有水蒸气。用浓硫酸来干燥。因此D中浓H2SO4的作用是除去氯气中的水蒸气。(3)氯气没有漂白性,当氯气遇水时二者发生反应产生HClO,有漂白性。因此E中红色干布条不褪色,F中红色湿布条褪色。(4)G是浸有淀粉KI溶液的棉花球,氯气会与KI发生反应:2 I-+Cl2=2Cl-+I 2,I 2遇淀粉变为蓝色。因此G处现象是棉花球表面变成蓝色。H是浸有NaBr溶液的棉花球,由于活动性Cl2>Br 2。所以H处反应的离子方程式是2 Br-+Cl2=2Cl-+Br 2。(5)氯气是大气污染物,所以在排放前应该进行尾气处理。由于氯气能与碱发生反应,所以若P处为尾气吸收装置,实验室利用烧碱溶液吸取Cl2的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O。(6)在B中发生的实验室制取氯气的反应的化学方程式为MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O制取氯气。由于浓盐酸有挥发性,所以在氯气中含有杂质HCl。由于氯气在饱和食盐水中的溶解度小,所以为了除去Cl2中的HCl气体,应放入的试剂是饱和食盐水。此时产生的氯气中任然含有水蒸气。用浓硫酸来干燥。因此D中浓H2SO4的作用是除去氯气中的水蒸气。(3)氯气没有漂白性,当氯气遇水时二者发生反应产生HClO,有漂白性。因此E中红色干布条不褪色,F中红色湿布条褪色。(4)G是浸有淀粉KI溶液的棉花球,氯气会与KI发生反应:2 I-+Cl2=2Cl-+I 2,I 2遇淀粉变为蓝色。因此G处现象是棉花球表面变成蓝色。H是浸有NaBr溶液的棉花球,由于活动性Cl2>Br 2。所以H处反应的离子方程式是2 Br-+Cl2=2Cl-+Br 2。(5)氯气是大气污染物,所以在排放前应该进行尾气处理。由于氯气能与碱发生反应,所以若P处为尾气吸收装置,实验室利用烧碱溶液吸取Cl2的离子方程式:Cl2+2OH-=Cl-+ClO-+H2O。(6)在B中发生的实验室制取氯气的反应的化学方程式为MnO2+4HCl(浓) MnCl2+Cl2↑+2H2O。若实验中使用12 mol/L的浓盐酸10 mL与足量的二氧化锰反应, 实际生成的Cl2的物质的量总是小于0.03 mol,是因为随着反应的进行,消耗氯化氢,同时生成水,且氯化氢挥发,使盐酸的浓度逐渐减小,稀盐酸与二氧化锰不反应。
MnCl2+Cl2↑+2H2O。若实验中使用12 mol/L的浓盐酸10 mL与足量的二氧化锰反应, 实际生成的Cl2的物质的量总是小于0.03 mol,是因为随着反应的进行,消耗氯化氢,同时生成水,且氯化氢挥发,使盐酸的浓度逐渐减小,稀盐酸与二氧化锰不反应。
本题难度:一般
3、选择题 自来水常用Cl2消毒,某学生用这种自来水去配制下列物质的溶液,不会产生明显的药品变质问题的是
[? ]
A.AgNO3
B.NaOH
C.Na2CO3
D.AlCl3
参考答案:D
本题解析:
本题难度:简单
4、填空题 洪灾过后,饮用水的消毒杀菌成为抑制大规模传染性疾病爆发的有效方法之一。漂白粉是常用的消毒剂之一。
(1)工业上将氯气通入石灰乳[Ca(OH)2]制取漂白粉,化学反应方程式为?(反应①)。
(2)漂白粉溶于水后,受空气中的CO2作用,即产生有漂白、杀菌作用的次氯酸,反应化学方程式为?(反应②)。
(3)次氯酸不稳定,容易分解,化学反应方程式为?(反应③)。
(4)反应①、反应②、反应③中,属于氧化还原反应的是(填反应编号)?。
参考答案:(1)2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O
(2)Ca(ClO)2+CO2+H2O=CaCO3+2HClO
(3)2HClO=2HCl+O2↑
(4)①,③
本题解析:(1)氯气与碱发生歧化反应,生成氯化钙和次氯酸钙,然后根据得失电子守恒配平即可。书写方程式时也可以看作氯气先与水反应生成盐酸和次氯酸,然后酸再和碱发生中和反应。
(2)根据强酸制弱酸的原理,碳酸的酸性大于次氯酸,所以Ca(ClO)2+CO2+H2O=CaCO3+2HClO
(3)次氯酸不稳定,见光分解为HCl和O2。
(4)有元素化合价升降的反应是氧化还原反应。反应②中元素化合价没有发生变化。
本题难度:一般
5、选择题 自来水可以用氯气消毒。某学生用这种自来水去配制下列物质的溶液,不会产生明显的变质问题的是
A.硝酸银
B.氯化亚铁
C.亚硫酸钠
D.氯化铝
参考答案:D
本题解析:略
本题难度:一般