微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
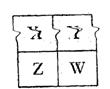
1、填空题 (1)已知X、Y、Z、W四种短周期主族元素在周期表中的相对位置如图所示,
W的气态氢化物的稳定性比Y?(填“强”、“弱”或“不一定”),W的原子序数?(填“可能”或“不可能”)是Y的原子序数的2倍。
(2)已知物质M由同一短周期的X、Y两种元素组成,X原子的最外层电子数是最内层
电子数的一半,Y元素最高正价与它的负价代数和为6。M与其他物质的转化关系如下(部分产物已略去):
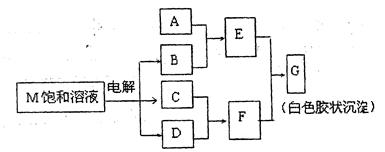
①若A是与X、Y同周期的一种常见金属,则A元素原子结构示意图为?,
写出A与B溶液反应的离子方程式?。
②若A是某元素的一种常见酸性氧化物,则该元素的周期表中的位置是?,
写出E与F反应的化学方程式?。
③电解M饱和溶液的产物之一B中的化学键为?。工业上用电解物质M的另一产物氧化有毒含氰(CN-)碱性废水,得到无毒的N2、CO2等。写出此反应的离子反应方程式?。
参考答案:
本题解析:略
本题难度:一般
2、选择题 下列物质属于纯净物的是
A.漂白粉
B.液氯
C.氯水
D.磷在氯气中燃烧产物
参考答案:B
本题解析:分析:纯净物是指只由一种物质组成,而混合物是指两种或两种以上的物质组成.
解答:A、漂白粉中由氯化钙、次氯酸钙组成,是混合物,故A错误;
B、液氯指的是液态氯气,是纯净物,故B正确;
C、氯水是氯气的水溶液,是混合物,故C错误;
D、磷在氯气中燃烧产物是五氧化二磷,三氧化二磷,是混合物,故D错误;
故选B.
点评:本题难度不大,主要考查了纯净物和混合物的判别,从而加深学生对有关知识的理解和应用.
本题难度:困难
3、实验题 四种短周期元素A、B、C、D的性质或结构信息如下:
信息①?原子半径大小:A>B>C>D
信息②?四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题。
(1)B元素在周期表中的位置?,请写出BC2分子的电子式?。
(2)A所在周期中,E元素的单质还原性最强,F元素的某些盐类常用作净水剂。E单质与甲反应有化合物X生成。请写出以下两个反应的离子方程式。
①A元素的单 质与物质甲发生的反应?。
质与物质甲发生的反应?。
②F、C两种元素组成的化合物Y可作为高温结构陶瓷材料,X与Y两种化合物在溶液中发生的反应?。
(3)物质丁的元素组成和甲相同,丁分子具有18电子结构。向盛有一定浓度丁溶液的试管中,逐滴加入用少量稀硫酸酸化的硫酸亚铁溶液。滴加过程中的现象是 :
:
①浅绿色溶液变成深棕黄色,②有少量气泡出现(经验证是氧气),片刻后反应变得剧烈,并放出较多热量,继续滴加溶液,静置一段时间,③试管中出现红褐色。向其中再滴入稀硫酸,红褐色变为黄色。请用化学方程式或离子方程式①、②、③中加点的字。
①?②? ?③?。
?③?。
参考答案:(1)第2周期IVA族?(1分 )
(2)①Cl2+H2O 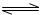 ?H++Cl-+HClO?(2分)
?H++Cl-+HClO?(2分)
②Al2O3+2OH-===2AlO-2+H2O?(2分)
(3)①2Fe2++H2O2+2H+=2Fe3++2H2O?(2分)
②2H2O2=2H2O+O2↑?(2分)
③Fe3++3H2O 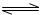 ?Fe(OH)3+3H+?(2分)(注:①③写化学方程式也给分)
?Fe(OH)3+3H+?(2分)(注:①③写化学方程式也给分)
本题解析:略
本题难度:一般
4、选择题 化学工作者从C2H6(g)+Cl2(g)→C2H5Cl(l)+HCl(g)受到启发,提出从农药和有机合成工业中可获得副产品盐酸.这一设想已成为现实,试指出从上述反应产物中获得盐酸的最佳分离方法
A.升华法
B.蒸馏法
C.水洗分液法
D.水洗萃取法
参考答案:C
本题解析:C2H5Cl(l)不溶于水,HCl(g)易溶于水形成盐酸.升华法、蒸馏法不能获得盐酸,水洗萃取法不是最佳方案.
本题难度:一般
5、选择题 欲寻求新的催化剂和制造耐高温、耐腐蚀的合金材料,应对元素周期表中进行研究的区域是(?)
A.碱金属
B.第ⅡA族元素
C.过渡元素
D.金属与非金属分界线附近的元素
参考答案:C
本题解析:元素周期表中位置相近的元素性质相似,因此人们可以在元素周期表中一定的区域内研究合成有特定性质的新物质。如在金属和非金属的分界线附近寻找半导体材料(如锗、硅、硒等),在过渡元素中寻找优良的催化剂和耐高温、耐腐蚀的合金材料(如制造火箭、飞机的钛、钼等元素)。
本题难度:简单