微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列描述正确的是
A.在pH=1溶液中,NH4+、K+、ClO―、Cl―可以大量共存
B.MgO可以除去MgCl2溶液中的FeCl3
C.足量铁粉与稀硝酸反应:Fe + 4H+ +NO3―== Fe3+ + 2H2O + NO ↑
D.对于平衡体系:H2(g)+I2(g)  2HI(g),其它条件不变时,增大体系压强,平衡向正反应方向移动,体系颜色加深
2HI(g),其它条件不变时,增大体系压强,平衡向正反应方向移动,体系颜色加深
2、选择题 下列反应的离子方程式正确的是(?)
A.向NaHCO3溶液中加入过量的Ba(OH)2溶液: Ba2++HCO3-+OH-= BaCO3↓+H2O

B.向Fe(NO3)2稀溶液中加入盐酸:3Fe2++4H++NO3-3Fe3++NO↑+2H2O

C.氢氧化镁加入醋酸:Mg(OH)2+2H+Mg2++2H2O
D.向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O Fe(OH)3↓+3H+
Fe(OH)3↓+3H+
3、选择题 向含有下列离子的溶液中分别加少量的Na2O固体后,该离子数目能增加的是( )
A.HS-
B.CO
C.NH
D.NO
4、选择题 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图(其中I代表H2A,II代表HA-,III代表A2-), 根据图示判断,下列说法正确的是
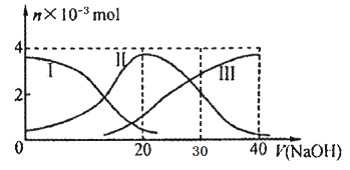
A.H2A在水中的电离方程式是: H2A?=== H+? +? HA-?;? HA-? ?H+? +? A2-
?H+? +? A2-
B.当V(NaOH)=20mL时,溶液中各粒子浓度的大小顺序为:c(Na+)>c(HA-)>c(H+)>c(A2-)>c(OH-)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水大
D. 当V(NaOH)=30mL时,溶液中存在以下关系:2c(H+)+ c(HA-)+ 2c(H2A)= c(A2-)+ 2 c(OH-)
5、选择题 在25℃的条件下,下列各组离子一定能在指定环境中大量共存的是
A.在c(H+)=10-10 mol/L的溶液中: Al3+、NH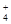 、Cl- 、NO
、Cl- 、NO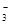
B.pH=13的溶液中:K+ 、Na+、SO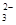 、Cl-
、Cl-
C.pH=2的溶液中: K+、NH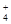 、Cl-、ClO-
、Cl-、ClO-
D.甲基橙呈红色的溶液中:Fe3+、Na+ 、SO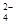 、CO
、CO