微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列反应的离子方程式正确的是?(?)?
A.把金属铁放入稀硫酸中 2Fe+6H+=2Fe3++3H2↑
B.碳酸钡与盐酸反应:BaCO3+2H+=Ba2++CO2↑+H2O
C.往澄清石灰水中滴入少量的碳酸氢钠溶液:C a2++OH-+HCO3-="=" CaCO3↓+H2O
a2++OH-+HCO3-="=" CaCO3↓+H2O
D.氢氧化钡溶液与稀 H2SO4反应:Ba2++SO42-=BaSO4↓
参考答案:BC
本题解析:略
本题难度:一般
2、选择题 下列类型的反应,一定发生电子转移的是(?)
A.分解反应
B.离子反应
C.置换反应
D.复分解反应
参考答案:C
本题解析:氧化还原反应中一定发生电子的转移,而置换反应一定是氧化还原反应,答案选C。
点评:氧化还原反应与四种基本反应类型的关系是:置换反应一定是氧化还原反应,复分解反应一定不是氧化还原反应,有单质参加的化合反应或有单质生成的分解反应都是氧化还原反应,据此可以进行有关判断。
本题难度:简单
3、选择题 某温度下,将氯气通入NaOH溶液中,反应得到NaCl、NaClO、NaClO3的混合溶液(已知氯气和NaOH在一定温度下能发生反应:Cl2+2NaOH=NaCl+NaClO+H2O ,3Cl2+6NaOH=5NaCl+NaClO3+3H2O),经测定ClO
参考答案:
本题解析:
本题难度:一般
4、简答题 已知氯元素的平均相对原子质量为35.5,由2311Na、3717Cl和3517Cl构成的11.7g氯化钠固体中含3717Cl的质量是多少?11.7g该固体刚好能和某250mL的AgNO3溶液完全反应,则该AgNO3溶液的物质的量浓度是多少?
参考答案:(1)设氯元素中35Cl的物质的量含量为x,则有35x+37(1-x)=35.5,
解之得x=75%.
11.7gNaCl的物质的量为n(NaCl)=11.7g58.5g/mol=0.2mol,
?m(37Cl)=0.2 mol×25%×37 g?mol-1=1.85g,
答:由2311Na、3717Cl和3517Cl构成的11.7g氯化钠固体中含3717Cl的质量是1.85g;
(2)由Ag++Cl-=AgCl↓可知,n(AgNO3)=n(NaCl)=0.2mol,
c(AgNO3)=0.2mol0.25L=0.8mol/L,
答:该AgNO3溶液的物质的量浓度是0.8mol/L.
本题解析:
本题难度:一般
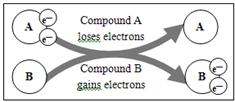
5、选择题 某国外化学教材中有一张关于氧化还原反应的插图:由图可知,在该反应中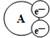 是
是
A.还原剂
B.氧化剂
C.氧化产物
D.还原产物
参考答案:A
本题解析:根据题给插图知,该物质在氧化还原反应中失电子生成A,作还原剂,选A。
本题难度:一般