��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ��80 ��ʱ��ˮ�����ӻ�KW=3.8��10-13�����¶�ʱ��ˮ��pH��?��
A������7
B����7
C������7
D����ȷ��
�ο��𰸣�B
�����������ˮ�����ԣ�c��H+��=c��OH-������ʹ������80 ��ʱ����Ϊc��H+��=c��OH-����������KW=c��H+����c��OH-��=��c��H+����2=3.8��10-13��c��H+��=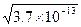 ?mol��L-1=6.16��10 -6 mol��L-1������ѡB��
?mol��L-1=6.16��10 -6 mol��L-1������ѡB��
�����Ѷȣ���
2�������� ��һpHΪ12��NaOH��Һ100mL���������pH��Ϊ11����ô��
(1)��������ˮӦ����______mL��
(2)����pH=10��NaOH��ҺӦ����______mL��
(3)����pH��2������Ӧ����________mL��
(4)����0.01mol/LH2SO4Ӧ����_____mL��
�ο��𰸣�(1)900? (2)1000? (3)81.8? (4)42.85
������������⿼��[H+]��pHֵ�ļ��㡣����Һ����ϡ�����Ի����Һ��������������֮������ʾ��������Һ������ΪV1mL��V2mL��V3mL��V4mL��
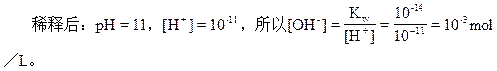
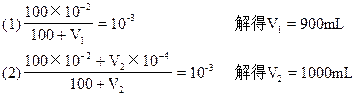
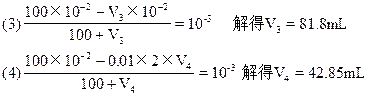
�����Ѷȣ�һ��
3��ʵ���� ��16�֣�50mL 0.50mol/L�����50mL 0.55 mol/L NaOH��Һ����ͼ��ʾ��װ���н����кͷ�Ӧ��ͨ���ⶨ��Ӧ���������ų��������ɼ��㷴Ӧ�ȡ�
(1)�ձ���������ĭ���ϵ�������?��
(2)���ձ���������Ӳֽ�壬��õ��к�����ֵ?���ƫ�� ��ƫС��������Ӱ�족��
(3)����ͼ��ʾ������A��������_______________����ʵ������У���������¶ȼ��ϵ�����ˮ��ϴ�ɾ�ֱ�Ӳ���NaOH��Һ���¶ȣ����õġ�H?-57.3KJ/mol�����������������������
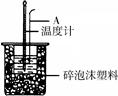
(4)ʵ���и���80mL 0.50mol/L�����100mL 0.55 mol/L NaOH��Һ���з�Ӧ��������ʵ����ȣ����ų�������?�����ȡ�������ȡ�)��
�����к���?�����ȡ�������ȡ�) ��
(5)����ͬŨ�Ⱥ�����İ�ˮ����NaOH��Һ��������ʵ�飬��õ��к��ȵ���ֵ��?�������ƫ����ƫС��������Ӱ�족��
(6)������ϡǿ�ᡢϡǿ�Ӧ����1molˮʱ�ų�57.3kJ��������д��ϡ�����ϡ����������Һ��Ӧ���к��ȵ��Ȼ�ѧ����ʽ?��
�ο��𰸣���1�����·�ֹ������ʧ��?��2��ƫС?��3�����β���������H��-57.3KJ/mol
��4������ȡ����?��5��ƫС?
��6��1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l)����H=-57.3KJ/mol
�����������1����ʵ����Ӧ�þ����ܵļ�����������ʧ�������ձ���������ĭ���ϵ������DZ��·�ֹ������ʧ��
(2)���ձ���������Ӳֽ�壬��������������ʧ���ⶨ���ƫ�͡�
��3�����������Ľṹ��֪��Ӧ�����ǻ��β��������������ܺ��������Ʒ�Ӧ�ų������������������������Һ����ʼ�¶ȸߣ���˵������շų�������ƫ�٣����H��-57.3KJ/mol��
��4���ı���ͼ����������Ӧ�зų���������仯������Ӧ���Dz���ģ���Ϊ�к�����ָ�������кͷ�Ӧ����1Ħ��H2Oʱ���ų��������������������ء�
��5����ˮ��������ʣ����ڵ���ƽ�⣬�������ȣ����Բ�õ��к��ȵ���ֵƫС��
��6�������к��ȵĸ����֪���Ȼ�ѧ����ʽΪ1/2H2SO4(aq)+NaOH(aq)=1/2Na2SO4(aq)+H2O(l)����H=-57.3KJ/mol��
�����Ѷȣ�һ��
4������� ��4�֣����е������Һ����Na2CO3?��NaHCO3?��CH3COONa?�� NaOH
��1����������Һ��pH��ͬʱ�������ʵ���Ũ���ɴ�С��˳����?������,������ͬ��
��2�����������ֵ������Һ�У��ֱ����AlCl3��Һ���������������?
�ο��𰸣�4�֣�ÿ��2�ֹ�4�֣�
��1��?�ۢڢ٢�?��2���ۢ�
�����������
�����Ѷȣ�һ��
5�������� 6�֣���0.3mol NaCl������0.1mol CuSO4?5H2O����������ˮ�����1�����Һ��Ȼ��ȡ��200ml��Һ����ʯī�缫��ͨ��һ��ʱ�䣨������ˮ�⣩����Cl������ȫ����Ϊ�����ݳ�ʱ�������ϲ����������������״���£��Ƕ��٣�������Һ��PHΪ���٣�������Һ������䣩��
�ο��𰸣�0.224L��? PH��13
����������������Լ�pH���йؼ��㡣
������������ʧȥ���ӣ�����ʽΪ2Cl�D�D2e��=Cl2��
����ת�Ƶ�����0.3mol��5��0.06mol
������ͭ���ӷŵ磬����ʽΪCu2����2e��=Cu
ת�Ƶ�����0.1mol��5��2��0.04mol
���Ը��ݵ��ӵ�ʧ�غ��֪�����������ӵõ�0.06mol��0.04mol��0.02mol
���������ĵ缫��ӦʽΪ2H����2e��=H2��
����������0.01mol�����״���µ������0.224L��
ͬʱ��Һ����������������0.01mol��2��0.02mol
Ũ����0.02mol��0.2L��0.1mol/L
PH��13
�����Ѷȣ�һ��