��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ������Һ�У�����ϵʽ��ȷ���ǣ���
A����Ũ�ȡ��������NaOH �Ͷ�Ԫ����H2A �����Һ�У�
c(Na+) + c(H+) ��c(HA��) + c(OH��) + c(A2��)
B��1 L 0.1 mol?L-1 CuSO4��(NH4)2SO4��6H2O ����Һ�У�
c(SO42��) ��c(NH4��)��c(Cu2��)��c(H��)��c(OH��)
C����֪��������HA��HB �ĵ���ƽ�ⳣ��Ka��HA����Ka��HB����������0.1 mol?L-1��HA��HB��NaA��NaB ��Һ�У�pH��NaA����pH��NaB����pH��HA����pH��HB��
D�����ʵ���Ũ����ȵ�Na2CO3��NaHCO3��Һ�������Ϻ����Һ�У�
3c(H2CO3��+2c(H+��+c(HCO3������2c(OH����+c(CO32����
�ο��𰸣�BD
���������
��ȷ�𰸣�BD
A������ȷ���ɵ���غ㣬��Ũ�ȡ��������NaOH �Ͷ�Ԫ����H2A �����Һ�У�
c(Na+) + c(H+) ��c(HA��) + c(OH��) + 2c(A2��)
B����ȷ��1 L 0.1 mol?L-1 CuSO4��(NH4)2SO4��6H2O ����Һ�У�2mol?L-1c(SO42��)��NH4��Ҫˮ�⣬c(NH4��)<2mol?L-1��Cu2��Ҫˮ�⣬c(Cu2 ��)<1mol?L-1��������Ũ��˳��Ϊ
c(SO42��) ��c(NH4��)��c(Cu2��)��c(H��)��c(OH��)
C������ȷ����֪��������HA��HB �ĵ���ƽ�ⳣ��Ka��HA����Ka��HB����������0.1 mol?L-1��HA��HB��NaA��NaB ��Һ�У�pH��NaB����pH��NaA����pH��HB����pH��HA��
D����ȷ���ɵ���غ�������غ�ļ���ʽ����ȥNa����Ũ�ȣ����ɡ����ʵ���Ũ����ȵ�Na2CO3��NaHCO3��Һ�������Ϻ����Һ�У�
����غ�
c(Na+) + c(H+) ��c(HCO3�D) + c(OH��) +2 c(CO32��)
�����غ�
2c(Na+)=3 c(HCO3�D) + 3c(CO32��)��3c(H2CO3��
��ȥc(Na+)�ɵ�
3c(H2CO3��+2c(H+��+c(HCO3������2c(OH����+c(CO32����
�����Ѷȣ���
2��ѡ���� ��ʹˮ�ĵ���ƽ�����ƣ���ˮ��Һ�����Ե������ǣ���
A��H+
B��OH-
C��Al3+
D��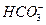
�ο��𰸣�C
���������Al3+��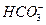 ˮ���ʹˮ�ĵ��룬ƽ�����ƣ�Al3+ˮ������ԣ�
ˮ���ʹˮ�ĵ��룬ƽ�����ƣ�Al3+ˮ������ԣ�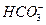 ˮ��ʼ��ԡ�
ˮ��ʼ��ԡ�
�����Ѷȣ���
3��ѡ���� ����������ˮ����ٽ������ܹ�����ǣ���
A��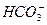 ��Na+��Cl-��OH-
��Na+��Cl-��OH-
B��Al3+��Na+��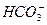 ��
��
C��H+��Fe2+�� ��Cl-
��Cl-
D��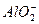 ��K+��
��K+�� ��Al3+
��Al3+
�ο��𰸣�BD
����������������Ĺؼ����ж���Һ���Ƿ�ͬʱ������������������������ӡ�Aѡ����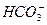 ��OH-�������ֽⷴӦ���ܴ������档Bѡ����Al3+��
��OH-�������ֽⷴӦ���ܴ������档Bѡ����Al3+��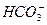 ����ٽ�ˮ������ܴ������棺Al3++3
����ٽ�ˮ������ܴ������棺Al3++3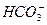 ====Al��OH��3��+3CO2����Cѡ����Fe2+��H+��
====Al��OH��3��+3CO2����Cѡ����Fe2+��H+��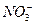 ����������ԭ��Ӧ���ܴ������档Dѡ����Al3+��
����������ԭ��Ӧ���ܴ������档Dѡ����Al3+��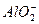 ����ٽ�ˮ�ⲻ�ܴ������棺Al3++3
����ٽ�ˮ�ⲻ�ܴ������棺Al3++3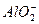 +6H2O====4Al��OH��3����
+6H2O====4Al��OH��3����
�����Ѷȣ���
4��ѡ���� �����£����и���Һ���������ʵ���Ũ�ȹ�ϵ��ȷ����
A��0.1 mol��L-1��Na2CO3��Һ�У�c(OH��)=c(HCO3��)+c(H+)+c(H2CO3)
B����pH=6��H2SO4ϡ��1000����c(H+)="2" c(SO42��)
C��Ũ�ȷֱ�Ϊ0.1 mol��L-1��0.01 mol��L-1��CH3COOH��Һ�У�c(CH3COO��)ǰ���Ǻ��ߵ�10��
D��NaA��Һ��pH��8��c(Na+)-c(A-) ="9" .9��10-7 mol��L-1
�ο��𰸣�D
���������A�������غ�Ϊ��c(OH��)=c(HCO3��)+c(H+)+2c(H2CO3)��B����pH=6��H2SO4��Һ�У�c��H+��= 10��6 mol/L, c��SO42����= 10��6/2 mol/L, ϡ��1000�����ǵ�ˮ�ĵ��룬c��H+��= 10��7 mol/L,��c��SO42����= 10��9/2 mol/L,�ʶ��ߵ��ܶȱ�Ϊ200��1��C��0.01 mol��L-1��CH3COOH��Һ�൱�ڽ�0.1 mol��L-1��CH3COOH��Һϡ��ʮ����ϡ�ʹٽ�ˮ�ĵ��룬����ϡ�ͺ��c(CH3COO��)����ԭ��Һ��1/10��D���ɵ���غ��֪��NaA��Һ��c(Na+)+ c(H+)= c(A-)+ c(OH-)����c(H+)=10-8 mol��L-1��c(OH-)=10-6 mol��L-1����ɵ�c(Na+)-c(A-) ="9" .9��10-7 mol��L-1����ѡD
�����Ѷȣ�һ��
5��ѡ���� ����˵������ȷ����?��?��
A�������£�ϡ��0.1 mol��L�İ�ˮ����Һ��c(OH-)��c(NH4+)��c(H+)���½�
B�������£�c(NH4+)��ȵĢ�(NH4)2SO4��(NH4)2Fe(SO4)2��NH4Cl��(NH4)2CO3��Һ�У��������ʵ���Ũ�ȴ�С��ϵ�ǣ���<��<��<��
C��pH��ȵ�CH3COONa��NaHCO3��Na2CO3������Һ��c(CH3COONa)��c(NaHCO3) ��c(Na2CO3)
D��ij�¶�ʱˮ�����ӻ�����KW=10-13�������¶���pH=11��NaOH��ҺaL��pH=1��ϡ����bL��ϣ������û��ҺPH=2����a��b=2��9
�ο��𰸣�B
�����������ϡ��Һ��c(H+)��c(OH-)�ij˻��Ǹ���ֵ��������ͬʱ�½������ߣ�A�����Fe2+��ˮ������NH4+��ˮ�⣬CO32-��ˮ��ٽ�NH4+��ˮ�⣬���Ե�Ũ�ȵĢ�(NH4)2SO4����(NH4)2Fe(SO4)2����NH4Cl����(NH4)2CO3��Һc(NH4+)��>��>��>�ۣ���ˣ�c(NH4+)��ȵĢ�(NH4)2SO4����(NH4)2Fe(SO4)2����NH4Cl��?��(NH4)2CO3��Һ�У��������ʵ���Ũ�ȴ�С��ϵ�ǣ���<��<��<�ۣ�B����ȷ������Խ��Խˮ���֪Ũ����ͬ��CH3COONa��NaHCO3��Na2CO3������Һ��pHΪ��Na2CO3>NaHCO3>CH3COONa�����pH��ȵ�CH3COONa��NaHCO3��Na2CO3������Һ��c(CH3COONa)>c(NaHCO3)>c(Na2CO3)��C�����pH=11��NaOH��Һc(OH-)=10-2mol/L��pH=1��ϡ����c(H+)=10-1 mol/L����Ϻ�pH=2����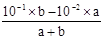 =10-2����a��b=9��2��D�����ѡB��
=10-2����a��b=9��2��D�����ѡB��
�����������ۺ���ǿ���Ѷȴ���Ҫ����ѧ����֪ʶ�ķ�������������������
�����Ѷȣ�һ��