|
高中化学必备知识点《影响盐类水解的因素》高频试题预测(2017年最新版)(十)
2017-08-06 11:25:26
来源:91考试网
作者:www.91exam.org 【 大 中 小】
|
微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式正确的是(?)
A.氯化铝溶液与氨水反应:
Al3++3NH3・H2O====Al(OH)3↓+3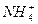
B.磷酸二氢钙溶液跟足量的氢氧化钠溶液混合:
3Ca2++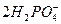 z4OH-====Ca3(PO4)2↓+4H2O z4OH-====Ca3(PO4)2↓+4H2O
C.硝酸亚铁溶液中滴入稀硫酸:
Fe2++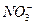 +2H+====Fe3++NO↑+2H2O +2H+====Fe3++NO↑+2H2O
D.硫氢化钠水解:
| HS-+H2O====H2S↑+OH-
参考答案:A
本题解析:B选项中钙离子和磷酸根离子的比例错,应为6个磷酸二氢根离子;C选项中电子不守恒;D选项中HS-水解较弱,不会产生硫化氢气体,且应用可逆号。
本题难度:简单
2、选择题 有下列盐:① FeCl3② CH3COONa ③ NaCl,其水溶液的pH由大到小排列正确的是
A.①>③>②
B.②>③>①
C.③>②>①
D.①>②>③
参考答案:B
本题解析:FeCl3溶液中三价铁离子水解显酸性PH小于7, CH3COONa 溶液中醋酸根离子水解显碱性,PH大于7,氯化钠溶液显中性,PH等于7,所以PH由大到小的顺序是②>③>①,所以答案选B。
本题难度:简单
3、选择题 常温下,向20mL 0.2mol/L H2A溶液中滴加0.2 mol/L NaOH溶液。有关微粒的物质的量变化如下图, 根据图示判断,下列说法正确的是
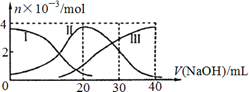
A.H2A在水中的电离方程式是:H2A 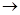 ?H+ + HA-;HA― ?H+ + HA-;HA― 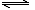 H+ + A2- H+ + A2-
B.当V(NaOH)=20mL时,则有:c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH-)
C.等体积等浓度的NaOH溶液与H2A溶液混合后,其溶液中水的电离程度比纯水小
D.当V(NaOH)=30mL时,则有:2c(H+) + c(HA-) + 2c(H2A) = c(A2-) + 2 c(OH-)
参考答案:BC
本题解析:由图像可知溶液中存在H2A 、HA―、A2-三种微粒。所以H2A为二元弱酸。Ⅰ为H2A的变化曲线;Ⅱ为HA-的变化曲线;Ⅲ为A2-的变化曲线。H2A在水中的电离方程式是:H2A  H+ + HA-;HA― H+ + HA-;HA― H+ + A2-。错误。B.当V(NaOH)=20mL时,恰好发生反应NaOH+ H2A=NaHA+H2O.根据物料守恒可得c(Na+) =c(H2A)+c(HA-)+c(A2-).因此c(Na+) > c(HA-)。在加入NaOH溶液20ml前HA-已经大量存在而且随NaOH体积的增大而增多,说明HA-的电离作用大于水解作用。所以c(H+) > c(OH-) 。因为在溶液中除了HA-电离产生H+,水也电离产生H+。所以c(H+) > c(A2-)。强电解质的电离作用远大于弱电解质的电离,所以c(HA-) > c(H+)。因此c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH-)。正确。C. 等体积等浓度的NaOH溶液与H2A溶液混合后得到NaHA.由于HA-的电离作用大于水解作用,所以溶液显酸性。HA-电离产生的H+对水的电离平衡H2O H+ + A2-。错误。B.当V(NaOH)=20mL时,恰好发生反应NaOH+ H2A=NaHA+H2O.根据物料守恒可得c(Na+) =c(H2A)+c(HA-)+c(A2-).因此c(Na+) > c(HA-)。在加入NaOH溶液20ml前HA-已经大量存在而且随NaOH体积的增大而增多,说明HA-的电离作用大于水解作用。所以c(H+) > c(OH-) 。因为在溶液中除了HA-电离产生H+,水也电离产生H+。所以c(H+) > c(A2-)。强电解质的电离作用远大于弱电解质的电离,所以c(HA-) > c(H+)。因此c(Na+) > c(HA-) > c(H+) > c(A2-) > c(OH-)。正确。C. 等体积等浓度的NaOH溶液与H2A溶液混合后得到NaHA.由于HA-的电离作用大于水解作用,所以溶液显酸性。HA-电离产生的H+对水的电离平衡H2O H++OH-起到了抑制作用。所以其溶液中水的电离程度比纯水小。正确。D. 当V(NaOH)=30mL时,溶液为NaHA与Na2A等物质的量的混合物。根据电荷守恒可得①c(Na+)+ c(H+)= 2c(A2-) +? c(OH-)+ c(HA-).根据物料守恒可得②2c(Na+)=3c(H2A)+3 c(HA-)+3c(A2-)。将 ①整理代入②,可得2c(H+) + c(HA-) + 3c(H2A) = c(A2-) + 2 c(OH-)。错误。 H++OH-起到了抑制作用。所以其溶液中水的电离程度比纯水小。正确。D. 当V(NaOH)=30mL时,溶液为NaHA与Na2A等物质的量的混合物。根据电荷守恒可得①c(Na+)+ c(H+)= 2c(A2-) +? c(OH-)+ c(HA-).根据物料守恒可得②2c(Na+)=3c(H2A)+3 c(HA-)+3c(A2-)。将 ①整理代入②,可得2c(H+) + c(HA-) + 3c(H2A) = c(A2-) + 2 c(OH-)。错误。
本题难度:一般
4、填空题 现有学生做如下实验:将盛有滴加酚酞的0.1 mol/L NaHCO3溶液的试管微热时,观察到该溶液的浅红色加深;若冷却至室温时又变回原来的浅红色,发生该现象的主要原因是__________________________________________________________。(结合反应方程式说明)
参考答案:因NaHCO3溶液中存在HCO3-+H2O H2CO3+OH-的水解平衡,水解反应为吸热反应,加热使水解平衡向右移动,c(OH-)增大,溶液的浅红色加深;降温时,平衡向左移动,c(OH-)减小,溶液颜色变浅。 H2CO3+OH-的水解平衡,水解反应为吸热反应,加热使水解平衡向右移动,c(OH-)增大,溶液的浅红色加深;降温时,平衡向左移动,c(OH-)减小,溶液颜色变浅。
本题解析:
本题难度:一般
5、选择题 某溶液中存在的离子有:S2-、HS-、OH-、Na+、H+,则下列有关对该溶液的叙述中不正确的是( )
A.离子浓度可能是c(Na+)>c(S2-)>c(OH-)>c(HS-)>c(H+)
B.组成该溶液的溶质只能是Na2S或NaHS或两者的混合物
C.该溶液可能呈中性,或碱性,或酸性
D.离子物质的量的关系是2n(S2-)+n(HS-)+n(OH-)=n(Na+)+n(H+)
参考答案:B
本题解析:略
本题难度:简单
|