��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� �����й�ʵ��ԭ���������ͽ��۶���ȷ���ǣ�
A��ij��ɫ��Һ�μ���ˮ��CCl4�������÷ֲ���²���Һ����ɫ����ԭ��Һ����I��
B��ȡ������ҺX�������м����������ư�ˮ���ټӼ���KSCN��Һ����Һ��죬
˵��X��Һ��һ������Fe2��
C����ij��Һ�еμ�BaCl2��Һ�����а�ɫ�������ٵμ�����ϡHNO3�����������ܽ⣬
��˵��ԭ��Һ��һ����SO42��
D��ij��ɫ��Һ�ýྻ��˿պȡ��Һ������ɫ��Ӧ������ʻ�ɫ����ԭ��Һ����Na+��K+
�ο��𰸣�A
���������A����ȡ���̣���ȷ��
B������ԭ��Һ����Fe3+��
C���������ǿ�����ԣ�ԭ��Һ��������������ܱ�����Ϊ�������
D����Ҫ�������ܲ������ܿ����Ƚ����Ե���ɫ��
�����Ѷȣ���
2������� ��δ�ʯ���л�ø��������ȼ��һֱ�ǻ�ѧ��̽���Ŀ��⣬��ʯ�ͷ���õ������ͽ����ѻ����Ի�ø��������ȼ�͡�
����һ��ʯ���Ǻ���20��30��̼ԭ�ӵ������Ļ��������³ʹ�̬��
���϶���ʯ�ʹ��ѻ���ͨ��ʹ��Al2O3��������
ij�о���ѧϰС����ʵ������ģ��ʯ�͵Ĵ��ѻ���װ����ͼ��ʵ������пɹ۲쵽��ƿ�й���ʯ�����ۻ����Թܢ���������Һ�����ᣬ�Թܢ������Ը��������Һ��ɫ��ʵ������Թܢ���Һ����ζ���������͵���ζ��
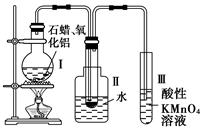
(1)��װ���������ӵ�˳��Ӧ��ѭ��ԭ��Ϊ__________________��
Ϊ��֤ʵ��ɹ���ʵ��ǰ������еIJ�����_________________��
װ���нϳ����ܵ�������_____________________��
(2)�Թܢ�������Һ������˵����______��
(3)�Թܢ�����Һ��ɫ˵����________________��
(4)�ܷ����Թܢ��е�Һ����ȡ��ˮ�е��壬������_______________��
(5)д����ʮ���ѻ��õ������ϩ�Ļ�ѧ����ʽ________________��
(6)ʯ���ѻ�����Ҫ������_____________��
�ο��𰸣�(1)�������ϣ��������ҡ����װ�õ������ԡ���������������
(2)�ѻ�������̼ԭ��������4����
(3)�ѻ�������̼ԭ����С��5��ϩ��
(4)���ܣ���Ϊ�ѻ���������ϩ���������巢���ӳɷ�Ӧ
(5)C20H42 C10H22��C10H20
C10H22��C10H20
(6)�����ʯ�Ͳ�Ʒ������ȼ�ͣ��ر������͵IJ���������
����������������ӵ�˳��Ӧ��ѭ�������ϣ������ҵ�ԭ��װ��ҩƷ֮ǰҪ���װ�õ������ԡ�����ʯ�ͷ���ҵ�ķ�����ԭ���������˳����ܣ������ó������⣬����������������ã��Թܢ�����Һ�����ɣ�˵������4��̼ԭ�������ϵ�������Ϊ���¡���ѹ�£�4��̼ԭ�������ϵ�����Һ̬���Թܢ�������KMnO4��Һ��ɫ˵�����ɳ��¡���ѹ�³���̬��5��̼ԭ�������µ�ϩ���������ѻ���������ϩ�����ɣ������巢���ӳɷ�Ӧ�����Բ���������ȡ±�ص��ʣ������ϱ仯���Կ�����ʯ���ѻ�����ҪĿ����Ϊ�˻�ø��������ȼ�ͣ��ر���������͵IJ�����������
�����Ѷȣ�һ��
3������� ij����С�������������ʵ�飨����ͼ��ʾ��
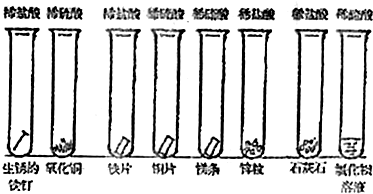
��1��������ʵ������η���ģ���д��������Թܱ�ţ�
��һ��______��
�ڶ���______��
������______��
����Ϊ��˷���������ǣ�______
��2��д���Թܢڢݢ��ʵ�������йص����ӷ���ʽ��
��______��______��
��______��______��
��______��______��
��3������Ϊ����С���Ա������ʵ�鼰����ķ������Ƚϣ����ɳ��Ľ��ۣ����ٴ�3������
��______��
��______��
��______��
��______��
��______��
�ο��𰸣���1����ʵ���Ŀ����̽��������ʣ����������������Ҫ�ɷ��������������������������ͭ�������������Ƭ�ǽ���������ͭƬ�ǽ���������þ���ǽ���������п���ǽ���������ʯ��ʯ���Σ������Ȼ������Σ��������ᷴӦ����𣬷�Ϊ������������Σ�
�ʴ�Ϊ���٢ڣ��ۢܢݢޣ��ߢࣻ ��Ϊ��ʵ���Ŀ�����о�ǿ�ᣨ��������ᣩ�ֱ������������������εķ�Ӧ��������˷��ࣻ
��2��������ͭ��ϡ���ᷴӦ����������ͭ��ˮ����������ͭ�����ܽ⣬���ɵ�����ͭ��ͭ���ӵ���ɫΪ��ɫ��
�ʴ�Ϊ�������ܽ⣬�õ���ɫ����Һ��CuO+2H+�TCu2++H2O��
��þ��Ϊ�������ʣ�����ϡ���ᷴӦ��������þ������������þ���ܽ⣬���������ɣ�
�ʴ�Ϊ��þ���ܽ⣬�����������壻 Mg+2H+�TMg2++H2����
��ϡ�������Ȼ�������Ӧ��
�ʴ�Ϊ��û��������Ӧ��
��3���ڸ��ֽⷴӦ�У�������������ˮ��������������ʱ������ʹ�������е�����Ũ�ȼ�С����Ӧ�������У�̽��������ʣ��뿼�����ܷ�����֮�������ֽⷴӦ�����Կ�������������������ijЩ�η�Ӧ��
�ʴ�Ϊ�����ܸ�ijЩ���������ﷴӦ�� ���ܸ�ijЩ�η�Ӧ�����ܸ����ֻ��ý�����Ӧ���Ტ���ܸ����н�����Ӧ��������ý�����Ӧʱ�ٶȲ�ͬ��
���������
�����Ѷȣ�һ��
4��ѡ���� ijѧ���������εķ���ͼ��ʾ��

���н�����ȷ���ǣ�������
A������һ����Fe3+
B������һ����Fe3+
C����ΪAgI����
D����һ��ΪFeBr2��Һ
�ο��𰸣�A�����к���Fe3+������Fe2+���������ɣ���һ������Fe3+����A����
B�����м���KSCN����ҺΪѪ��ɫ��Ӧ����Fe3+����B��ȷ��
C�������м���������������Һ���ɵ���ɫ����������ΪS��AgI����C����
D�������п��ܺ���Fe3+��Fe2+��I-��S2-�����ӣ���һ��ΪFeBr2����D����
��ѡB��
���������
�����Ѷȣ�һ��
5��ʵ���� (14��)ij����С����ʵ���������������������Ҵ���Ũ�������Ϊԭ���Ʊ�1,2?�������顣��֪1,2?���������۵�Ϊ9 �棬C2H5OH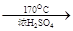 CH2=CH2����H2O��
CH2=CH2����H2O��
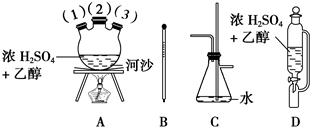
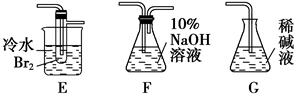
��1�������������Ϊ�����ң���ȷ������˳����(�̽ӿڻ���Ƥ�ܾ�����ȥ)��B��A��1������A�У�D��A��2����A��3����________��________��________��________��
��2��װ��A��������ƿ������D��©�����ص���________����ɳ������Ϊ________��
��3��д������C���������ã�_______________________________________________��
��4���¶ȼ�ˮ�������ȷλ����______________________________________________��
��5����Ӧ��E�м�������ˮ���ѷ�Ӧ��E����ʢ����ˮ��С�ձ�������Ϊ
________________________________________________________________________��
��6����������������δ��Ӧ��Br2�������________(����ȷѡ��ǰ����ĸ)ϴ�ӳ�ȥ��
a������������������Һ? b������������Һ
c���⻯����Һ? d���Ҵ�
��7����Ʒ�п��ܻ��е��л�������________������________������ȥ��
�ο��𰸣���1��C��F��E��G��
��2����ѹ��Һ?������
��3���ٰ�ȫƿ���������ڷ�ֹ����ͨ��������������Σ��
��4��Ӧ����Һ�����£����Ӵ�ƿ��
��5�����ӷ������Լ�����Ļӷ���ʧ
��6��a
��7�����ѡ�����
�����������1��1,2?���������۵�ͣ����������ܣ�Cװ��Ӧ��������1,2?��������֮ǰ����E��1,2?�������������������ܣ�C��ֱ����Һ��������������ֹͣʵ�飬����ȡ��CH2===CH2�����п��ܺ���SO2���壬���ȳ�ȥ����4���¶ȼ��������ⶨ��ӦҺ�¶ȵģ����Ҫ����Һ�����¡���5������Һ���ӷ�������ˮҺ�⡣��6��1,2?������������NaOH��Ӧ��b�����ã�c������I2����1,2?���������У�d���Ҵ���1,2?�������黥�ܡ���7������ȡ��ϩʱ���Ҵ����Ӽ���ˮ���������ѡ�
�����Ѷȣ�һ��