微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 化学反应原理在科研和生产中有广泛应用
(1)利用“化学蒸气转移法”制备TaS2晶体,发生如下反应TaS2(s)+2I2(g) TaI4(g)+S2(g) △H
TaI4(g)+S2(g) △H
2、填空题 (10分)进入2013年以来,我国中东部地区多次遭遇大范围、长时间的雾霾天气。车辆排放的氮氧化物、煤燃烧产生的二氧化硫是导致雾霾天气的“罪魁祸首”。
(1)活性炭可处理大气污染物NO。在2 L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
 物质 物质
T/℃ n/mol
| 活性炭
| NO
| E
| F
|
初始
| 2.030
| 0.10
| 0
| 0
|
T1
| 2.000
| 0.040
| 0.030
| 0.030
|
T2
| 2.005
| 0.050
| 0.025
| 0.025
|
①结合上表数据,写出NO与活性炭反应的化学方程式 。
②上述反应T1℃时的平衡常数K1= 。
③根据上述信息判断,温度T1和T2的关系是(填序号) 。
a.T1>T2 b.T1<T2 c.无法比较
(2)车辆排放的氮氧化物和碳氧化物在催化剂作用下可发生反应:2CO+2NO N2+2CO2在一体积为1L的密闭容积中,加入0.40mol的CO和0.40mol的NO ,反应中N2的物质的量浓度的变化情况如图所示,回答下列问题。
N2+2CO2在一体积为1L的密闭容积中,加入0.40mol的CO和0.40mol的NO ,反应中N2的物质的量浓度的变化情况如图所示,回答下列问题。
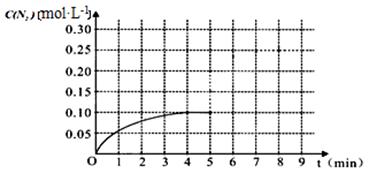
①计算从反应开始到平衡时,平均反应速率v(N2)= 。
②在第5分钟末将容器的体积缩小一半后,若在第8分钟末达到新的平衡(此时N2的浓度约为0.25 mol・L-1)。请在上图中画出第5分钟末到此平衡时N2浓度的变化曲线。
3、填空题 在一定条件下,有反应xA+yB zC。
zC。
Ⅰ、若A、B、C均为气体,在2 L的密闭容器中,加入2 mol A、1 mol B,一定温度下达到平衡。测得平衡后的压强为反应前的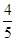 ,平衡时C为0.6 mol・L-1,B为0.2 mol・L-1。
,平衡时C为0.6 mol・L-1,B为0.2 mol・L-1。
试回答下列问题:
(1)平衡时B的物质的量是 ,B的转化率=
(2)x∶y∶z= ,该温度下平衡常数=
Ⅱ、若反应xA+yB zC已达到平衡。改变条件后,其速率与时间的变化如图甲和乙。试回答下列问题:
zC已达到平衡。改变条件后,其速率与时间的变化如图甲和乙。试回答下列问题:
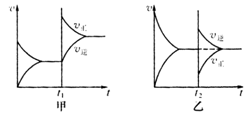
(1)图甲中t1时改变的条件可能是 (填字母序号)。
A.若A、B均为固体,加入A或B
B.若A或B为气体,C为固体,增大压强
C.A、B中至少有一种是气体,且加入该气体
D.升高温度
E.加入催化剂
(2)若A、B、C均为气体,加入x mol A、y mol B,达到平衡后发生如图乙中t2时的变化。则此时发生变化的条件为(写出一种情况即可):
4、选择题 已知次氯酸是比碳酸还弱的酸,反应Cl2+H2O HCl+HClO达到平衡后,要使HClO浓度增大,可加入
HCl+HClO达到平衡后,要使HClO浓度增大,可加入
[? ]
A.NaCl固体
B.水
C.CaCO3固体
D.NaOH固体
5、选择题 下列实验事实不能用平衡移动原理解释的是( )
c(醋酸) /
(mol・L-1)
| 0.1
| 0.01
|
pH
| 2.9
| 3.4
|