��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� Ǧ��������ĿǰӦ���ձ�Ļ�ѧ��أ�����Һ��ʽǦ�������Կ��ܵļ�����ǦΪ����ʣ�����ܷ�Ӧ��Pb��PbO2��4H��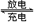 2Pb2����2H2O�������й�����Һ��ʽǦ�����ص�˵����ȷ����
2Pb2����2H2O�������й�����Һ��ʽǦ�����ص�˵����ȷ����
A����ŵ�ʱ����Һ��Pb2��Ũ�ȱ��ֲ���
B����ŵ�ʱ����Һ�ĵ��������仯����
C���ŵ�ʱ�ĸ�����ӦʽΪ��Pb��2e����Pb2��
D�����ʱ��������ӦʽΪ��Pb2����4OH����2e����PbO2��2H2O
�ο��𰸣�BC
����������ŵ�ʱΪԭ���ԭ����
������ӦΪ��Pb��2e����Pb2��?������ӦΪ��PbO2��4H����2e����Pb2����2H2O
���ʱΪ����ԭ����
������ӦΪ��Pb2����2e����Pb?������ӦΪ��Pb2����2H2O��2e����PbO2��4H��
A�����ʱ����Һ��Pb2��Ũ������֮��С���ų�
B����Һ�������ƶ�����������ɲ��䣬��ȷ
C����ȷ
D������
��ΪBC
�����Ѷȣ���
2������� ��Դ��ȱ���������ٵ��ش����⡣�״���һ�ֿ�������Դ�����й㷺�Ŀ�����Ӧ��ǰ����
��1����ҵ��һ������������ַ�Ӧ�ϳɼ״���
��ӦI��CO2(g)+3H2(g) CH3OH(g)+H2O(g) ��H1
CH3OH(g)+H2O(g) ��H1
��ӦII��CO(g)+2H2(g) CH3OH(g) ��H2
CH3OH(g) ��H2
������Ӧ���ϡ�ԭ�Ӿ��á�ԭ�����__________�������
��2���±����������Ƿ�Ӧ���ڲ�ͬ�¶��µĻ�ѧƽ�ⳣ��(K)
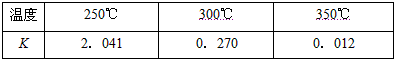
���ɱ��������жϦ�H2_______0�����������������������
���������ݻ����䣬���д�ʩ�����Ӽ״����ʵ���______________��
A�������¶�
B����CH3OH(g)����ϵ�з���
C��ʹ�ú��ʵĴ���
D������He��ʹ��ϵ��ѹǿ����
E����ԭ�����ٳ���CO��H2
��ij�¶��£���2mol CO��6mol H2����2L���ܱ������У���ַ�Ӧ���ﵽƽ����c(CO)=
0��2mol��L-1����CO��ת����Ϊ____________����ʱ���¶�Ϊ____________�����ϱ���ѡ��
��3��ijʵ��С�����ݼ״�ȼ�յķ�Ӧԭ���������ͼ��ʾ��ԭ���װ�á�
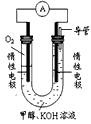
�ٸõ�ع���ʱ��OH-��_______���ƶ����������������
�ڸõ�������ĵ缫��ӦʽΪ___________________��
�ο��𰸣���1���٢�
��2���٣�����BE����80%��250��
��3���ٸ�����O2+2H2O+4e-��4OH-
���������
�����Ѷȣ�����
3��ѡ���� ��ͼ���г��ϳ���������ȼ�ϵ��ʾ��ͼ
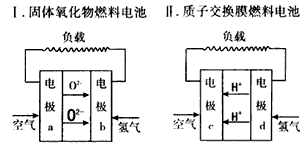
�����йص�ص缫a��b��c��d��������ȷ����
[? ]
A���缫aΪ�������缫��Ӧ����ΪH2O
B���缫bΪ�������缫��Ӧ����ΪH2O
C���缫cΪ�������缫��Ӧ����ΪH2O
D���缫dΪ�������缫��Ӧ����ΪH2O
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� ���Խ���ӦZn+Br2 = ZnBr2��Ƴ����أ�����4���缫��Ӧ
��Br2 + 2e��= 2Br- ��2Br- - 2e��= Br2 ��Zn
�ο��𰸣�
���������
�����Ѷȣ�һ��
5��ѡ���� ij��ȼ�ϵ�����Լ��飨CH4���Ϳ���Ϊԭ�ϣ���KOHΪ�������Һ���ɵ�ԭ��أ���ص��ܷ�Ӧ���Ƽ����������е�ȼ�գ�����˵����ȷ���ǣ�������
��ÿ����1molCH4���������·�ṩ8mole-
��CH4�ڸ�������������Ӧ���缫��Ӧʽ�ǣ�CH4+10OH--8e-=CO32-+7H2O
��ȼ�ϵ�ذѻ�ѧ��ֱ��ת��Ϊ���ܣ���������������һ���м���ʽ��������������ת��Ч�ʸߣ����Ҽ����˶Ի�������Ⱦ
������ȼ�ϵ��Ҫ���ڸ����������Һ��
A���٢�
B���٢ڢۢ�
C���٢ۢ�
D���ڢ�
�ο��𰸣��ٸ��ݵ缫��Ӧʽ��CH4+10OH--8e-=CO32-+7H2O����ÿ����1molCH4���������·�ṩ8mole-���ʢ���ȷ��
��ȼ���ڸ�����ʧ���ӷ���������Ӧ������ȼ�������ɶ�����̼��ˮ��������̼���������ط�Ӧ����̼��أ����Ե缫��ӦʽΪ��CH4+10OH--8e-�TCO32-+7H2O���ʢ���ȷ��
��ȼ�ϵ�ذѻ�ѧ��ֱ��ת��Ϊ���ܣ���������������һ���м���ʽ��������������ת��Ч�ʸߣ���Ӧ�IJ�����̼��غ�ˮ�����Լ��ٶԻ�������Ⱦ���ʢ���ȷ��
�ܸõ�صĵ�ط�ӦʽΪ��CH4+2O2+2KOH=K2CO3+3H2O����Һ�ɼ���Һ�������Һ��Ҫ���ڸ����������Һ���ʢ���ȷ��
��ѡB��
���������
�����Ѷȣ�һ��