微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 氨基甲酸铵(NH2COONH4)是一种白色固体,易分解、易水解,可用作肥料、灭火剂、洗涤剂等。某化学兴趣小组模拟工业原理制备氨基甲酸铵,反应的化学方程式如下:
2NH3(g)+CO2(g)?NH2COONH4(s) ΔH<0。
(1)如图所示装置制取氨气,你所选择的试剂是________________________。

(2)制备氨基甲酸铵的装置如图13-7所示,把氨气和二氧化碳通入四氯化碳中,不断搅拌混合,生成的氨基甲酸铵小晶体悬浮在四氯化碳中。当悬浮物较多时,停止制备。

注:四氯化碳与液体石蜡均为惰性介质。
①发生器用冰水冷却的原因是________________________________________________________________________________________________________________________________________________。
液体石蜡鼓泡瓶的作用是________________________________________________________________________。
②从反应后的混合物中分离出产品的实验方法是________________________________________________________________________
(填写操作名称)。为了得到干燥产品,应采取的方法是________(填写选项序号)。
a.常压加热烘干
b.高压加热烘干
c.真空40 ℃以下烘干
③尾气处理装置如图所示。
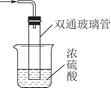
双通玻璃管的作用:____________;浓硫酸的作用:______________________、__________________________________________________________________。
(3)取因部分变质而混有碳酸氢铵的氨基甲酸铵样品1.173 0 g,用足量石灰水充分处理后,使碳元素完全转化为碳酸钙,过滤、洗涤、干燥,测得质量为1.500 g。则样品中氨基甲酸铵的物质的量分数为________。[Mr(NH2COONH4)=78,Mr(NH4HCO3)=79,Mr(CaCO3)=100]
参考答案:(1)浓氨水与氢氧化钠固体(CaO、碱石灰)等合理答案
(2)①降低温度,提高反应物转化率(或降低温度,防止因反应放热造成产物分解) 通过观察气泡,调节NH3与CO2的通入比例
②过滤 c
③防止倒吸 吸收多余的氨气 防止空气中的水蒸气进入反应器使氨基甲酸铵水解
(3)80%
本题解析:(1)CaO与浓氨水中的水反应放热使氨气易于逸出。(2)该反应为放热反应,低温利于反应正向进行,且产物易分解,故采取冰水浴冷却、低温烘干等。(3)n(CaCO3)=n(C元素)=1.500 g÷100 g・ mol-1=0.015 mol,n(NH2COONH4)=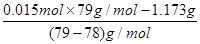 =0.012 mol。氨基甲酸铵的物质的量分数为
=0.012 mol。氨基甲酸铵的物质的量分数为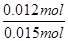 ×100%=80%。
×100%=80%。
本题难度:一般
2、选择题 今有下列三个氧化还原反应:
(1)2FeCl3+2KI =2FeCl2+2KCl+I2
(2)2FeCl2+Cl2 = 2FeCl3
(3)2KMnO4+16HCl = 2KCl+2MnCl2+8H2O+5Cl2↑
若某溶液中有Fe2+和I-共存,要氧化除去I-而又不影响Fe2+和Cl-,可加入的试剂是
[? ]
A.FeCl3
B.KMnO4
C.Cl2
D.HCl
参考答案:A
本题解析:
本题难度:一般
3、选择题 将溴水分别与酒精、己烯、苯和四氯化碳混合,充分振荡后静置,下列现象与所加试剂不相吻合的是( )
| ? | ?A | ?B | ?C | ?D
?与溴水混合的试剂
?酒精
?乙烯
?苯
?四氯化碳
?现象
?
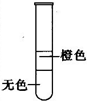
?

?

?
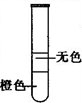
|
A.A
B.B
C.C
D.D
参考答案:A
本题解析:
本题难度:一般
4、选择题 100mL0.3mol・L-1Na2SO4溶液和50mL0.2mol・L-1Al2(SO4)3溶液混合后,溶液中SO42-离子的物质的量浓度(设体积为二者之和)为
A.0.2mol?L-1
B.0.25 mol?L-1
C.0.4 mol?L-1? ?
D.0.5 mol?L-1
参考答案:C
本题解析:试题分析:n(SO42-)=0.1×0.3mo・L-1+0.05L×3×0.2mol・L-1=0.06mol.C(SO42-)="n/V=0.06mol/0.15L=0.4" mol/L.选项为:C
考点:考查混合溶液中微粒的物质的量浓度的计算的知识。
本题难度:简单
5、选择题 氯化铵和氯化钠可用下列哪一种方法分离( )
A.加入氢氧化钠
B.加入AgNO3溶液
C.加热法
D.加入一种合适的酸
参考答案:氯化铵加热易分解,冷却后又可生成氯化铵,可通过加热的方法分离,无须加入其它试剂,
故选C.
本题解析:
本题难度:简单