微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列离子方程式书写正确的是
A.四氧化三铁与足量的稀硝酸反应:Fe3O4+8H+=2Fe3++Fe2++4H2O
B.向硫酸铜溶液中加入过量的氨水:Cu2++2NH3?H2O=Cu(OH)2↓+2NH4+
C.将Na2O2固体投入H218O中:2Na2O2+2H218O=4Na++4OH-+18O2↑
D.向次氯酸钠溶液中通入少量二氧化硫:SO2+ClO-+2OH-=SO42-+Cl-+H2O
参考答案:D
本题解析:分析:A、硝酸具有强氧化性能氧化亚铁离子;
B、氢氧化铜溶于过量氨水;
C、依据过氧化钠和水反应的实质分析判断;
D、次氯酸根离子具有强氧化性能氧化二氧化硫为硫酸.
解答:A、四氧化三铁与足量的稀硝酸反应:3Fe3O4+NO3-+28H+=9Fe3++NO↑+14H2O,故A错误;
B、向硫酸铜溶液中加入过量的氨水:Cu2++4NH3?H2O=Cu(NH3)42++4H2O,故B错误;
C、将Na2O2固体投入H218O中:反应过程为:Na2O2+H218O=2Na18OH+H2O2,2H2O2=2H2O+O2,反应应为:2Na2O2+2H218O=4Na++418OH-+O2↑,故C错误;
D、向次氯酸钠溶液中通入少量二氧化硫,次氯酸根离子具有强氧化性能氧化二氧化硫为硫酸:SO2+ClO-+2OH-=SO42-+Cl-+H2O,故D正确;
故选D.
点评:本题考查了离子方程式书写方法和注意问题,注意量不同产物不同,反应实质的理解和分析是解题关键,需要熟练掌握基础,题目难度中等.
本题难度:简单
2、选择题 下列式子正确的是(? )
A.H×
B.Na×+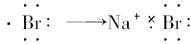
C.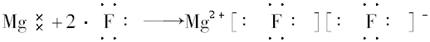
D.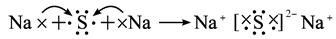
参考答案:D
本题解析:在元素符号周围用・或×来表示元素原子最外层电子的数目,这种式子叫电子式。
从题意看,是检查用电子式表示离子或分子形成的过程。检查时注意:
(1)阴、阳离子是否已标明电荷数;
(2)阴离子必须加括号,表示得到电子;
(3)阴或阳离子相同时不能合并写。
A不正确,因为H不是金属原子,故与氯化合后不是离子化合物,不能用“[?]”表示;B项错在阴离子未用方括号括起,未标出电荷;C项错在相同的阴离子排在一起。D项正确。
本题难度:一般
3、选择题 下列叙述正确的是(?)
A.两种元素构成的共价化合物分子中的化学键都是极性键
B.两种同种非金属元素原子间形成的化学键都是极性键
C.含有极性键的化合物分子一定不含非极性键
D.只要是离子化合物,其熔点就比共价化合物的熔点高
参考答案:B
本题解析:A项错,例如H2O2中含有O―O非极性键。C项错,如CH3CH2OH(酒精)分子中既含极性键,又含非极性键。D项错,例如由共价化合物形成的原子晶体的熔点可能比由离子化合物构成的离子晶体的熔点高。
本题难度:简单
4、选择题 已知下列两个热化学方程式
2H2(g)+O2(g)=2H2O(l);ΔH=-571.6kJ/mol
C3H8(g)+5O2(g)=3CO2(g)+4H2O(l);ΔH=-2220kJ/mol
实验测得氢气和丙烷的混合气体共0.5mol,完全燃烧时放出热量723.2kJ,则混合气体中氢气和丙烷的体积比约为
A.1:3
B.2:3
C.3:2
D.3:1