微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 MgSO4?7H2O在医药上常用做泻药,工业上可用氯碱工业中的一次盐泥为原料生产。已知一次盐泥中含有镁、钙、铁、铝、锰的硅酸盐和碳酸盐等成分。其主要工艺如下:
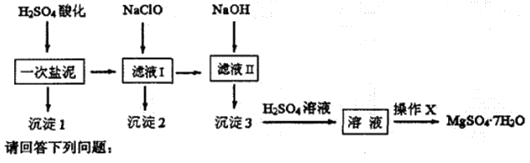
用H2SO4调节溶液PH至1~2,H2SO4作用是 ?。
(2)加NaClO溶液至PH=5~6并加热煮沸5~10分钟,沉淀2中主要含有MnO2和另外两种难溶物,这两种难溶物的化学式分别为?、?;其中NaClO溶液将MnSO4转化为MnO2的离子方程式为 ?。
(3)检验滤液Ⅱ中是否含有Fe3+的实验方法是??。
(4)“操作X”是将溶液?、?、过滤洗涤,即得到MgSO4?7H2O晶体。
(5)准确称量制得的样品5g,用200mL水溶解,加入2 mol?L―1的盐酸5mL,在不断搅拌下滴加足量2 mol?L―1 BaCl2溶液,充分反应后,得沉淀4.46g,则样品纯度为?。
参考答案:
(1)溶解盐泥变成可溶性硫酸盐,除去Ca2+、SiO32-、CO32-
(2)Fe(OH)3、Al(OH)3? Mn2++ClO-+H2O=MnO2↓+Cl-+2H+
(3)取少量的上层滤液Ⅱ,加热KSCN,观察溶液是否显血红色,若显血红色则有Fe3+,若不显血红色则无Fe3+
(4)蒸发浓缩、冷却结晶
(5)93.5%
本题解析:
(1)H2SO4的作用主要是调节PH,溶解盐泥,除去CO32-,生成硅酸沉淀及CaSO4微溶除去Ca2+及SiO32-
(2)根据沉淀3只有Mg(OH)2所以沉淀2中有Fe(OH)3及Al(OH)3(原因是物质的Ksp不同,Fe3+及Al3+在PH较小时就可以沉淀);Mn2+被氧化成MnO2沉淀而ClO-被还原成Cl-,再根据溶液显酸性及电荷守恒配出方程式;
(3)检验离子操作过程应该为:取液、加试剂、观察现象、出结论
(5)根据原子守恒,MgSO4.7H2O――BaSO4,算出MgSO4.7H2O的质量[n(BaSO4)=0.019mol,取两位有效数字,由此得到答案为93.5%]
本题难度:一般
2、选择题 某氯化镁溶液的密度为1.18g?cm-3,其中镁离子的质量分数为5.11%.300mL该溶液中Cl-离子的物质的量约等于
A.0.37mol
B.0.63mol
C.0.74mol
D.1.5mol
参考答案:D
本题解析:分析:根据c= 计算镁离子的物质的量浓度,再利用MgCl2可知,c(Cl-)=2c(Mg2+),以此来解答.
计算镁离子的物质的量浓度,再利用MgCl2可知,c(Cl-)=2c(Mg2+),以此来解答.
解答:氯化镁溶液的密度为1.18g?cm-3,其中镁离子的质量分数为5.11%,
则c(Mg2+)=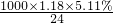 ≈2.5mol/L,
≈2.5mol/L,
c(Cl-)=2c(Mg2+)=5.0mol/L,
所以300mL该溶液中Cl-离子的物质的量约等于0.3L×5.0mol/L=1.5mol,
故选D.
点评:本题考查物质的量及浓度的有关计算,明确浓度与质量分数的换算公式即可解答,难度不大.
本题难度:困难
3、选择题 下列化学实验或操作能够达到目的是( )
A.欲除去蛋白质溶液中的NaCl而又不改变它的性质,可加入适量的BaCl2溶液,再过滤
B.将溴乙烷和NaOH溶液共热后,再滴加AgNO3溶液可检验其中的溴元素
C.为除去含有Mg(OH)2和Ca(OH)2的浊液中的Ca(OH)2,可向其中加入足量的MgCl2,充分反应后,过滤
D.除去乙酸乙酯中混有少量乙酸:加入乙醇和浓硫酸,加热、静置、分液
参考答案:A.BaCl2是重金属盐能使蛋白质发生变性,变性是不可逆过程,故A错误;
B.氢氧根会和银离子结合形成AgOH,但是AgOH不能在水中存在,会生成沉淀,故B错误;
C.Mg(OH)2比Ca(OH)2更难溶,由水中的离子平衡可得当往悬浊液加MgCl2时,Mg2+浓度增加,所以会以Mg(OH)2的形式沉淀出来,而OH-浓度有限,所以Ca(OH)2中的Ca又会以离子形式存在于溶液中,过滤即可除掉,故C正确;
D.如果加入乙醇和浓硫酸,虽然可以反应掉部分乙酸,但是又会引入乙醇,而且加热会使它挥发,最好不用,一般加入少量碳酸钠即可,故D错误.
故选C.
本题解析:
本题难度:一般
4、选择题 用海带灰制备单质碘的实验中,涉及的操作正确且能达到实验目的的是

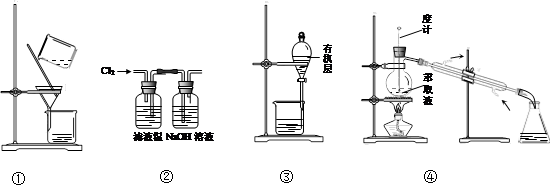 A.用图①所示装置,过滤海带灰浸取液
A.用图①所示装置,过滤海带灰浸取液
B.用图②所示装置,在滤液中通入Cl2
C.用图③所示装置,先放出下层液体,再放出有机层
D.用图④所示装置,回收萃取剂苯并获得单质碘
参考答案:C
本题解析:A项正确;B中应该是长进短出,错误;C中在分液时上层液体要从分流漏斗上口倒出下层液体流出,错误;D项中由于碘受热能升华,无法分离,错误;
本题难度:简单
5、选择题 只用一种试剂可区别Na2SO4、MgCl2、FeCl2、Al2(SO4)3四种溶液,这种试剂是(?)
A.Ba(NO3)2
B.H2SO4
C.NaOH
D.AgNO3
参考答案:C
本题解析:只有NaOH 与四种试剂混合后的现象不同:
与Na2SO4不反应无现象;与MgCl2有白色沉淀生成;与FeCl2有白色沉淀生成,但迅速转化为灰绿色,最终为红褐色;与Al2(SO4)3有白色沉淀生成,但随着加入NaOH的增多,沉淀又会溶解,故答案为C
本题难度:一般