微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 有关元素X、Y、Z、D、E的信息如下:
?
| 有关信息
|
X
| 元素主要化合价为-2,原子半径为0.074 nm
|
Y
| 所在主族序数与所在周期序数之差为4
|
Z
| 原子半径为0.102 nm,其单质在X的单质中燃烧,发出明亮的蓝紫色火焰
|
D
| 最高价氧化物对应的水化物可溶于水,且能电离出电子数相等的阴、阳离子
|
E
| 单质是生活中常见金属,其制品在潮湿空气中易被腐蚀或损坏
|
?
请回答下列问题:
(1)X的一种氢化物可用于实验室制取X的单质,其反应的化学方程式为___________。
(2)E元素与Y元素可形成EY2和EY3两种化合物,下列说法正确的是(填序号)_______。
①保存EY2溶液时,需向溶液中加入少量E单质
②EY2只能通过置换反应生成,EY3只能通过化合反应生成
③铜片、碳棒和EY3溶液组成原电池,电子由铜片沿导线流向碳棒
(3)将Z单质在X的单质中燃烧的产物和等物质的量的Y单质同时通入足量的水中,充分反应后的溶液中滴入品红溶液,现象是__________________,有关反应的离子方程式为________________________________________________________________________。
参考答案:(1)2H2O2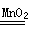 2H2O+O2↑
2H2O+O2↑
(2)①、③
(3)溶液呈红色且不褪去 SO2+Cl2+2H2O=4H++SO42-+2Cl-
本题解析:元素主要化合价为-2的X为氧元素;所在主族序数与所在周期序数之差为4的情况有两种,一是氧元素,二是氯元素,显然Y不可能再是氧,而是氯元素;单质在氧气中燃烧,发出明亮的蓝紫色火焰的Z是硫元素;最高价氧化物对应的水化物电离出电子数相等(各10个)的阴阳离子的是碱,该可溶性碱只能是NaOH,D是钠元素;在潮湿空气中易被腐蚀或损坏的常见金属为铁。
(1)氧的氢化物中可用于实验室制取O2的是H2O2,其化学方程式为2H2O2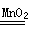 2H2O+O2↑。
2H2O+O2↑。
(2)铁与氯可形成两种化合物FeCl2、FeCl3, 保存FeCl2溶液时,需向溶液中加入少量Fe单质,防止Fe2+被氧化,①正确;FeCl2也可以通过化合反应生成,如2FeCl3+Fe=3FeCl2,②不正确;铜片、碳棒和FeCl3溶液组成的原电池中铜片为负极,电子由铜片沿导线流向碳棒,③正确。(3)SO2与Cl2等物质的量反应可生成不具有漂白性的HCl和H2SO4,反应后的溶液中滴入品红溶液,品红不褪色。
本题难度:一般
2、选择题 某元素最高价氧化物对应水化物的分子式是H4RO4,则其氢化物的分子式是
[? ]
A.RH4
B.RH3
C.H2R
D.HR
参考答案:A
本题解析:
本题难度:简单
3、选择题 可能存在的第119号元素,有人称“类钫”,据周期表结构及元素性质变化趋势,有关“类钫”的预测说法正确的是
[? ]
A.“类钫”在化合物中呈+1价
B.“类钫”属过渡元素,具有放射性
C.“类钫”单质的密度小于1g/cm3
D.“类钫”单质有较高的熔点
参考答案:A
本题解析:
本题难度:一般
4、选择题 下列关于非金属元素气态氢化物的叙述正确的是( )
A.气态氢化物的水溶液都是酸
B.气态氢化物都可由非金属单质和H2直接化合
C.气态氢化物是极性分子
D.气态氢化物都是共价化合物
参考答案:A、非金属元素氮元素的气态氢化物是氨气,它的水溶液氨水显碱性,属于碱,故A错误;
B、不是所有的非金属都能直接与氢气化合,如碲、砹等非金属不能直接与氢气化合,故B错误;
C、非金属元素气态氢化物有的是极性分子,如水分子,有的是非极性分子,如甲烷分子等,故C错误;
D、非金属元素气态氢化物中,只含有共价键,均是共价化合物,故D正确.
故选D.
本题解析:
本题难度:简单
5、推断题 下表是元素周期表的一部分,A、B、C、D、E、X是表中给出元素组成的常见单质或化合物。已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去)
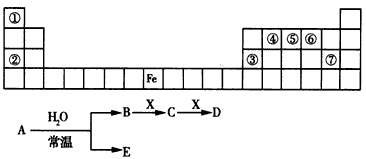
(1)①若E为氧化物,则A与水反应的化学方程式为___________________。
②当X是碱性盐溶液,C分子中有22个电子时,C的电子式为___________。向空气中大量排放C可能导致的后果是_________________。
③当X为金属单质时,X与B的稀溶液反应生成C的离子方程式为________________。
(2)若E为气体单质,D为白色沉淀,A的化学式可能是__________,B含有的化学键类型为_________。
(3)若B为气体单质,D可与水蒸气在一定条件下发生可逆反应,生成C和一种可燃性气体单质,写出该可逆反应的化学方程式_________________。
参考答案:(1)①3NO2+H2O=2HNO3+NO;②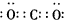 ;使地球温度升高(或温室效应);③Fe+4H++NO3-=Fe3+
;使地球温度升高(或温室效应);③Fe+4H++NO3-=Fe3+
+NO↑+2H2O
(2)Na、Na2O2或NaH;离子键和极性共价键
(3)CO+H2O(g) CO2+H2
CO2+H2
本题解析:
本题难度:一般