微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 欧盟原定于2012年1月1日起征收航空碳排税以应对冰川融化和全球变暖,使得对如何降低大气中CO2的含量及有效地开发利用碳资源的研究显得更加紧迫。请运用化学反应原理的相关知识研究碳及其化合物的性质。
(1)用电弧法合成的储氢纳米碳管常伴有大量的碳纳米颗粒(杂质),这种颗粒可用如下氧化法提纯,请完成该反应的化学方程式:
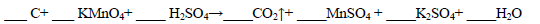
(2)焦炭可用于制取水煤气。测得12 g 碳与水蒸气完全反应生成水煤气时,吸收了131.6 kJ热量。该反应的热化学方程式为 。
(3)活性炭可处理大气污染物NO。在2 L密闭容器中加入NO和活性炭(无杂质),生成气体E和F。当温度分别在T1和T2时,测得各物质平衡时物质的量如下表:
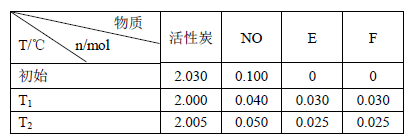
上述反应T1℃时的平衡常数为K1,T2℃时的平衡常数为K2。
Ⅰ.计算K1= 。
Ⅱ.根据上述信息判断,温度T1和T2的关系是(填序号) 。
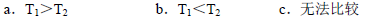
(4)CO2经常用氢氧化钠来吸收,现有0.4 molCO2,若用200ml 3mol/LNaOH溶液将其完全吸收,溶液中离子浓度由大到小的顺序为: 。
(5)CO还可以用做燃料电池的燃料,某熔融盐燃料电池具有高的发电效率,因而受到重视,该电池用Li2CO3和 Na2CO3的熔融盐混合物作电解质,CO为负极燃气,空气与CO2的混和气为正极助燃气,制得在 650 ℃下工作的燃料电池,其负极反应式: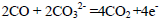 则
则
正极反应式:___ ,电池总反应式 。
参考答案:(1)5、4、6、5、4、2、6(2)C(s)+H2O(g)=CO(g)+H2(g),ΔH=+131.6 kJ?mol―1(3)①Ⅰ.0.5625 Ⅱ.c(4)c(Na+) > c(HCO3-) > c(CO32-) > c(OH-) > c(H+)(5)O2 +2CO2+4e-=2CO32-, 2CO+O2=2CO2
本题解析:(1)反应中C元素的化合价由0升高为+4价,一个碳化合价变化4,Cr元素的化合价由+6价降低为+3价,1个K2Cr2O7化合价变化6,4和6的最小公倍数为12,由化合价升降总数相等可知,C的化学计量数为3,K2Cr2O7的化学计量数为2,由于产物中有Cr2(SO4)3,所以未知的反应物为H2SO4,最后由质量守恒定律可知得化学反应为3C+2K2Cr2O7+8H2SO4
本题难度:困难
2、选择题 在反应3Cu2S+22HNO3=6Cu(NO3)2+3H2SO4+10NO↑+8H2O中,1mol还原剂失去电子的物质的量为: (?)
A.6mol
B.8mol
C.10mol
D.12mol
参考答案:C
本题解析:略
本题难度:简单
3、选择题 以下为在浓盐酸中H3AsO3与SnCl2反应的离子方程式,关于该反应的说法正确的组合是:(? )?
a SnCl2+b Cl-+c H3AsO3+d H+=e As+f SnCl62-+g M?
①氧化剂是H3AsO3;?②M为OH-;
③每生成7.5gAs,还原剂失去的电子为0.3?mol;?④ SnCl62-是氧化产物。
A.①③④
B.①②④
C.①②③④
D.只有①③
参考答案:A
本题解析:Sn元素由+2价升至+4价,SnCl62-是氧化产物,而As元素由+3价降至0价,氧化剂是H3AsO3;
由化合价的升降守恒得:3SnCl2+b Cl-+2H3AsO3+d H+=2As+3SnCl62-+g M,再由由电荷守恒及原子守恒可得:3SnCl2+12Cl-+2H3AsO3+6H+=2As+3SnCl62-+6H2O
故每生成7.5gAs,还原剂SnCl2失去的电子为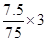 =0.3mol
=0.3mol
由于溶液为强酸性溶液,M不可能为OH―,排除②
答案为A
本题难度:一般
4、填空题 配平下列离子方程式,并用双线桥法表示电子转移的关系:
MnO4-+SO32-+H+-------Mn2++SO42-+H2O
参考答案: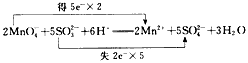
本题解析:
本题难度:一般
5、填空题 实验室里通常用MnO2与浓盐酸反应制取氯气,其反应的化学方程式为:
MnO2+4HCl(浓)  MnCl2+Cl2↑+ 2H2O
MnCl2+Cl2↑+ 2H2O
(1)在该反应中,如有1 mol Cl2生成,被氧化的HCl的物质的量是?mol,转移电子的物质的量是?mol。
(2)某温度下,将Cl2通入NaOH溶液中,反应得到含有ClO-与ClO3-物质的量之比为1∶1的混合液,反应的化学方程式是 ??。
(3)报纸报道了多起卫生间清洗时,因混合使用“洁厕灵”(主要成分是盐酸)与“84消毒液”(主要成分是NaClO)发生氯气中毒的事件。试根据你的化学知识分析,原因是(用离子方程式表示)?。
参考答案:(1)2? 2 (2)4Cl2+8NaOH = 6NaCl+NaClO3+NaClO+4H2O
(3)Cl-+ClO-+2H+ = Cl2↑+H2O
本题解析:(1)当1mol Cl2参加反应时,由Cl2~2HCl可知被氧化的HCl为1mol×2=2mol,转移电子的物质的量为:1mol×(4-2)=2mol;(2)由题意可知反应物为氯气和氢氧化钠,生成物为NaCl、NaClO3、NaClO和H2O,氯元素从0价变为NaClO3中+5价,两个氯原子失10个电子,氯元素从0价变为NaCl中-1价,两个氯原子得到2个电子,所以氯化钠前得系数为6,氯酸钠前的系数为1,再根据原子守恒就可得到反应的化学方程式为:4Cl2+8NaOH = 6NaCl+NaClO3+NaClO+4H2O;(3)次氯酸钠有强氧化性,盐酸有强还原性,两者相遇发生氧化还原反应生成氯气,故化学反应方程式为:Cl-+ClO-+2H+ = Cl2↑+H2O。2与浓盐酸反应制取氯气
本题难度:一般