微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 配制一定物质的量浓度溶液时,会导致所配溶液浓度偏大的操作是
A.在用蒸馏水洗涤烧杯时,洗液未全部注入容量瓶中
B.定容摇匀后,发现液面低于刻度线,又加水到刻度
C.定容时俯视刻度线
D.用来配制溶液的容量瓶用蒸馏水洗涤后未进行干燥处理
参考答案:C
本题解析:应逐个分析每个选项,找出正确的选项:因为cB=nB/V,若错误操作使nB增大,V减小,则cB偏大,若错误操作使nB减小,V增大,则cB偏小.A操作使nB减少,B操作使V增大,C操作使V减小,D操作对nB和V均无影响,故A、B操作使cB减小,C操作使cB增大,D无影响.
本题难度:简单
2、选择题 有机物的天然提取和人工合成往往得到的是混合物,假设给你一种这样的有机混合物让你研究,一般要采取的几个步骤是
[? ]
A.分离、提纯→确定化学式→确定实验式→确定结构式
B.分离、提纯→确定实验式→确定化学式→确定结构式
C.分离、提纯→确定结构式→确定实验式→确定化学式
D.确定化学式→确定实验式→确定结构式→分离、提纯
参考答案:B
本题解析:
本题难度:一般
3、实验题 (4分)某学校化学科研小组从文献资料上获得如下信息:NaHCO3在潮湿的空气中会缓慢分解成Na2CO3、H2O和CO2。为了验证这一信息,该科研小组将一瓶在潮湿空气中久置的NaHCO3样品混合均匀后,进行如下实验:
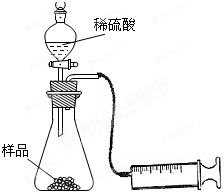
(1)在一个质量为ag的蒸发皿中加入一些样品,称得总质量为bg。用酒精灯对其充分加热,冷却后称得其总质量为cg。残留在蒸发皿中的固体是(填化学式)_________。
(2)另称取相同质量的样品放入锥形瓶中,实验装置如右图所示。为了保证实验成功,所选用针筒的最大刻度值应大于或等于_________(mL)。(设实验在标准状况下进行,请把合适的答案编号都挑选出来)
A.[(b-a)/84]×22.4×1000 mL
B.[(b-c)/31]×22.4×1000 mL
C.[(c-a)/106]×22.4×1000 mL
D.[(c-a)/106]×2×22.4×1000 mL
参考答案:(1)Na2CO3(1分)(2)ABD(3分,答对一个给1分,答错一个倒扣一分)
本题解析:(1)NaHCO3受热会发生会发生如下反应:2NaHCO3?→ Na2CO3?+?CO2 ?↑+?H2O,其中CO2?气体跑出,水也会蒸发掉。只剩下Na2CO3固体。
(2) 由题意可知(b-a)为Na2CO3质量,则[(b-a)/84]×22.4×1000 mL为NaHCO3体积。所以选项A正确。由(1)可知冷却后的总质量其实是Na2CO3和蒸发皿质量,所以(c-a)就是Na2CO3质量。由化学方程式可知[(c-a)/106]×2就是NaHCO3物质的量,可算出[(c-a)/106]×2×22.4×1000 mL为NaHCO3体积。所以选项D正确。有题意可知(b-c)为NaHCO3与Na2CO3质量之差。由
2NaHCO3?→ Na2CO3?+?CO2 ?↑+?H2O? Δn
2? 1
n(NaHCO3)? (b-c)/62
可算出(b-c)/31就是NaHCO3物质的量,则[(b-c)/31]×22.4×1000 mL为NaHCO3体积。所以选项B正确。
本题难度:简单
4、实验题 Fe2O3、Cu2O都是红色粉末,常用作颜料。某校化学实验小组通过实验来探究一红色粉末是Fe2O3、Cu2O或二者混合物。探究过程如下:
查阅资料:Cu2O溶于稀硫酸生成Cu和CuSO4;在空气中加热生成CuO。
提出假设:?
假设1:红色粉末是Fe2O3?
假设2:红色粉末是Cu2O
(1)假设3:?
设计探究实验:
取少量粉末放入足量稀硫酸中,在所得溶液中再滴加 KSCN 溶液。
(2)若假设1成立,则实验现象是?。
(3)若滴加 KSCN 试剂后溶液不变红色,则证明原固体粉末中一定不含三氧化二铁。你认为这种说法合理吗??。
简述你的理由?。
(4)若固体粉末完全溶解无固体存在 , 滴加 KSCN 试剂时溶液不变红色 , 则证明原固体粉末是?,写出发生反应的离子方程式?、?、?。
探究延伸:经实验分析,确定红色粉末为Fe2O3和Cu2O的混合物。
(5) 实验小组欲用加热法测定Cu2O的质量分数。取a g固体粉末在空气中充分加热,待质量不再变化时,称其质量为bg(b > a),则混合物中Cu2O的质量分数为?。
参考答案:(1)假设3:红色粉末是Fe2O3和Cu2O的混合物(1分)
(2)溶液变为血红色(1分)
(3)不合理? Cu能将Fe3+还原为Fe2+(2分)
(4)Fe2O3和Cu2O的混合物?
Fe2O3+6H+ = 2Fe3++3H2O? Cu2O+2H+ =" Cu" + Cu2+ + H2O
2 Fe3+ + Cu =" 2" Fe2+ + Cu2+(每个1分,共4分)
(5)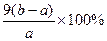 (1分)
(1分)
本题解析:略
本题难度:一般
5、实验题 (4分)某同学为探究碳酸钠的性质,进行了如下实验,请你按要求回答有关问题。
(1)配制100 mL 0.5 mol/L的Na2CO3溶液。该同学先用天平称量Na2CO3固体的质量,然后配制该溶液,要用到的玻璃仪器有量筒、烧杯、?、?。
(2)用pH试纸测所配溶液的pH,pH>7,说明Na2CO3溶液呈?(填“酸性”、“碱性”或“中性”);用试管取少量所配溶液,向溶液中滴加几滴酚酞试液,溶液变红,再用酒精灯加热,溶液的颜色变深,说明升高温度,对Na2CO3的水解有?作用。
参考答案:
(1)容量瓶、玻璃棒? (2)碱性、促进作用
本题解析:略
本题难度:简单