微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 Ⅰ某温度时,在2L密闭容器中某一反应的A、B物质的量随时间变化的曲线如图1所示,由图中数据分析求:
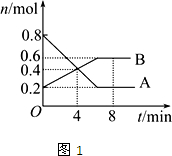
(1)该反应的化学方程式为______.
(2)反应开始至4min时,A的平均反应速率为______.
(3)第4min末时A、B的物质的量浓度依次为______、______.
第4min时,正、逆反应速率的大小关系为:v(正)______v(逆)(填“>”、“<”或“=”,同),第8min时,v(正)______v(逆).
Ⅱ有铜片、锌片和250mL稀硫酸组成的原电池,当在铜片上放出4.48L(标准状况下)的气体时,硫酸恰好完全反应.
(1)该原电池的正极反应式______
(2)原稀硫酸的物质的量浓度是______mol/L
(3)锌片减少的质量______g.
参考答案:Ⅰ.(1)由图可知,A减少,B增加,则A为反应物,B为生成物,相同时间内△n之比等于化学计量数之比,等于(0.8-0.2):(0.6-0.2)=3:2,所以该反应为3A 2B,故答案为:3A
2B,故答案为:3A 2B;
2B;
(2)反应开始至4min时,A减少0.8mol-0.4mol=0.4mol,v=△c△t=0.4mol2L4min=0.05mol/(L?min),故答案为:0.05mol/(L?min);
(3)4min末时A、B的物质的量均为0.4mol,c(A)=c(B)=0.4mol2L=0.2mol/L,第4min时向正反应方向进行,所以v(正)>v(逆),第8min时反应达到平衡,所以v(正)=v(逆),故答案为:0.2mol/L;0.2mol/L;>;=;
Ⅱ.(1)正极上氢离子得到电子,正极反应为2H++2e-=H2↑,故答案为:2H++2e-=H2↑;
(2)铜片上放出4.48L,n(H2)=n(H2SO4)=4.48L22.4L/mol=0.2mol,c=nV=0.2mol0.25L=0.8mol/L,故答案为:0.8;
(3)由Zn~H2↑可知,溶解的Zn为0.2mol×65g/mol=13g,故答案为:13.
本题解析:
本题难度:一般
2、填空题 工业生产硝酸铵的流程图如下图。请回答
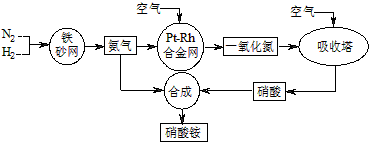
(1)已知:N2(g)+3H2(g)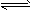 2NH3(g) ΔH=-92 kJ・mol-1。
2NH3(g) ΔH=-92 kJ・mol-1。
①在500℃、2.02×107Pa和铁催化条件下向一密闭容器中充入1molN2和3molH2,充分反应后,放出的热量______(填“<”“>”“=”)92.4kJ,理由是______________________________。
②为有效提高氢气的转化率,实际生产中宜采取的措施有____________
A.降低温度 B.最适合催化剂活性的适当高温 C.增大压强
D.降低压强 E.循环利用和不断补充氮气 F.及时移出氨
(2) 已知铂铑合金网未预热也会发热。写出氨催化氧化的化学方程式:________________________,该反应的化学平衡常数表达式K=________________,当温度升高时,K值______(填“增大”、“减小”或“无影响”)。
(3)在一定温度和压强的密闭容器中,将平均相对分子质量为8.5的H2和N2混合,当该反应达到平衡时,测出平衡混合气的平均相对分子质量为10,请计算此时H2的转化率(写出计算过程)
___________________________________________
参考答案:(1)①<;在101KPa和298K条件下,1mol氮气和3mol氢气完全反应生成2mol氨气,放出92.4kJ热量,该反应为可逆反应,反应物不能全部变为生成物;又因为反应温度为500℃,所以放出的热量小于92.4kJ
②CEF
(2)4NH3+5O2 4NO+6H2O; K=
4NO+6H2O; K= ;减小
;减小
(3)设充入气体总量为1mol,氮气的物质的量为x,则氢气的物质的量为(1-x)。
则有: 28x+2(1-x)=8.5(或用十字交叉法)
解得:N2:x=0.25mol H2:1mol-0.25mol=0.75mol
又设平衡时N2转化的物质的量为y,则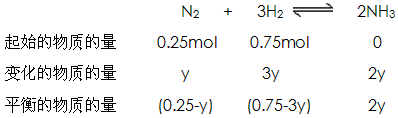 则有:
则有: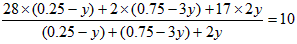
解得:y=0.075mol
则氢气的转化率为: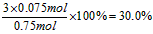
本题解析:
本题难度:困难
3、选择题 下列叙述中正确的是(? )
A.某反应的平衡常数仅是温度的函数,其数值大小与该反应的焓变(△H)无关
B.催化剂不能改变平衡常数的大小,平衡常数越大,反应一定越容易进行
C.对于一个处于平衡状态的化学反应来说,平衡常数发生变化,化学平衡不一定发生移动
D.化学平衡发生移动,平衡常数不一定发生变化
参考答案:A
本题解析:
本题难度:简单
4、填空题 已知反应:aA(g)+bB(g)?cC(g)
根据图形推测:
(1)P1______P2?(?填>或<)
(2)a+b______c?(?填>或<)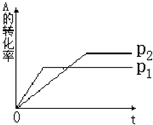
参考答案:(1)由图象可知P1曲线反应速率较大,说明P1压强较大,故答案为:>;
(2)压强增大,A的转化率减小,说明增大压强,平衡向逆反应方向移动,则有a+b<c,故答案为:<.
本题解析:
本题难度:一般
5、选择题 关于可逆反应A(s)+B(g)?2C(g);△H<0,平衡常数为K,下列说法正确的是( )
A.
B.K值越大表示达到平衡时,正反应进行程度越大
C.其它条件不变时,温度升高,K值增大
D.其它条件不变时,压强减小,K值减小
参考答案:B
本题解析:
本题难度:一般