��������ע"91������"���ں�,��30Ԫ,��ȡ����Ա����ҵ�ࡢ��ʦ�ȿ�������40G!
1��ѡ���� ����Ԫ�ء��ȶ������ļ���Ԥ�ԣ���Ȼ���п��ܴ�����ԭ������Ϊ114��Ԫ�ص��ȶ�ͬλ��208X��1999�����Ƿ�����114��Ԫ�أ�������֧���ˡ��ȶ�����ѧ˵�����������֪��Ԫ��������Ԥ��208X��Ԫ�����ڱ��е�λ��
A.�ڰ����ڢ���
B.�������ڢ�A��
C.�������ڢ�A��
D.�������ڢ�B��
�ο��𰸣�C
����������������е�Ԫ�������ɣ������������������Ӧ�ŵ�118�ţ���118��Ԫ��Ӧλ�ڵ�������0��(��18��)���ɴ˿�֪114��Ԫ��Ӧλ��ͬһ���ڣ��ڢ�A��(��14��)��
�����Ѷȣ�һ��
2������� W��X��Y��ZΪ�������ڳ�ϡ������Ԫ���������Ԫ�ء����ǵ�ԭ������������������ֻ��Y�ǽ���Ԫ�أ�Y��������������W������������ȣ�Y��Z��Ԫ�ص�������֮��ΪW��X��Ԫ��������֮�͵�3�����ɴ˿�֪Ԫ��WΪ ____��XΪ____��YΪ___;ZΪ___������Ԫ��������������ɵģ��Ⱥ������Ӽ��ֺ��й��ۼ��Ļ�����Ļ�ѧʽ������д���֣�_____��____��____������Ԫ���������ϣ������ɹ��ۻ�����Ļ�ѧʽ��(����д����)____��____��____��____��
�ο��𰸣�H ��O ��Na ��S
NaOH ��NaHS ��Na2SO4 ��Na2SO3�е�3��
H2O ��H2S ��SO2 ��H2O2 ��SO3�е�4��
���������
�����Ѷȣ�һ��
3������� �±���Ԫ�����ڱ���һ���֣�����������ĸ�ֱ�����������е�һ��Ԫ�أ�
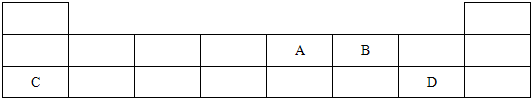
��1��A���ʵĵ���ʽ��______��BԪ�������ڱ��е�λ����______��
��2��D������C������������Ӧˮ���ﷴӦ�����ӷ���ʽ��______��
��3��B��C��Ԫ�طֱ��γɵ����ӵİ뾶��ϵ��B______C���������=����������
��4��A����̬�⻯����D����̬�⻯�ﷴӦ�IJ�����______���ò����к��еĻ�ѧ��������______��
��5��������ʵ����˵��D�ķǽ����Ա�A�ķǽ�����ǿ����______��
a��D���⻯���A���⻯���ȶ�
b��D����������ϼ۴���A����������ϼ�
c��D����ۺ������A����ۺ����������ǿ��
�ο��𰸣���Ԫ�������ڱ��е�λ�ÿ�֪��AΪN��BΪO��CΪNa��DΪCl��
��1��N���������5�����ӣ������д������Թ��õ��Ӷԣ������ʽΪ

��B��������Ϊ8����Ԫ�����ڱ��еĵڶ����ڵڢ�A�壬
�ʴ�Ϊ��

���ڶ����ڵڢ�A�壻
��2��������NaOH��Һ��Ӧ�����Ȼ��ơ��������ơ�ˮ�����ӷ�ӦΪCl2+2OH-�TCl-+ClO-+H2O��
�ʴ�Ϊ��Cl2+2OH-�TCl-+ClO-+H2O��
��3�������ӡ������Ӿ�����ͬ�����Ų������ӣ�Na��ԭ�������������Ӱ뾶С���ʴ�Ϊ������
��4��������HCl��Ӧ�����Ȼ�泥��仯ѧʽΪNH4Cl���������Ӽ������ۼ����ʴ�Ϊ��NH4Cl�����Ӽ������ۼ���
��5��a��D���⻯���A���⻯���ȶ�����D�ķǽ�����ǿ����aѡ��
b��D����������ϼ۴���A����������ϼۣ����ܱȽϷ� �����Ե�ǿ������b��ѡ��
c��D����ۺ������A����ۺ����������ǿ����D�ķǽ�����ǿ����cѡ��
�ʴ�Ϊ��ac��
���������
�����Ѷȣ�һ��
4��ѡ���� ����˵����ȷ����
A.ԭ������Խ��ԭ�Ӱ뾶һ��Խ��
B.ԭ�ӵĵ��Ӳ���Խ�࣬�뾶Խ��
C.Ԫ�����ʵ������Ա仯����Ԫ�����ʵļ��ظ�
D.��C��N��O��F��˳��Ԫ�ص����������������
�ο��𰸣�C
���������ԭ�Ӱ뾶��ԭ�������ĵ�������һֱ�������dz������Ա仯����Aѡ���ȷ��ԭ�Ӱ뾶�Ĵ�С�ܵ��Ӳ������˵��������������������ص�Ӱ�죬���е��Ӳ�������Ҫ�ģ�������Ψһ���أ����磬Clԭ�ӱ�Li��һ�����Ӳ㣬��ԭ�Ӱ뾶r(Li)��r(Cl)����B���ȷ��Ԫ�����ʵ������Ա仯���Ǽ��ظ��仯���仯�ij̶Ȳ�ͬ���仯�������յ�Ҳ��ͬ����C������ȷ�ģ���������õķǽ���Ԫ�أ���ֻ�и��ۣ�û�����ۣ����ķǽ�����Ҳ��ǿ��һ��ֻ�и��ۣ���Dѡ���ȷ��
�����Ѷȣ�����
5��ѡ���� �����е����Ų�ʽ��ԭ���У���һ��������С����
A.ns2np3
B.ns2np4
C.ns2np5
D.ns2np6
�ο��𰸣�B
���������ÿ�����ڵĵ�һ��Ԫ�ص�һ��������С�����һ��Ԫ�أ�ϡ�����壩�ĵ�һ������������з��������ܰ������ȫ�ձȽ��ȶ�������ڶ����ڵ�O<N���������ڵ�Mg>Al,P>S.
�����Ѷȣ���