微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 (共8分)A、B、C、D、E均为可溶于水的固体,组成他们的离子有
阳离子
| Na+ Mg2+ Al3+ Ba2+
|
阴离子
| OH- Cl- CO32- SO42- HSO4-
|
分别取它们的水溶液进行实验,结果如下:①A溶液与B溶液反应生成白色沉淀,沉淀可溶于E溶液;
②A溶液与C溶液反应生成白色沉淀,沉淀可溶于E溶液;③A溶液与D溶液反应生成白色沉淀,沉淀可溶于盐酸;④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失。
(1)据此推断它们是(写化学式)A ;B ;C ;D ;E 。
(2)写出④中反应的离子方程式: 。
(3)A溶液中各种离子浓度由大到小的顺序为 。
参考答案:(1)Na2CO3、Al2(SO4)3、MgCl2、Ba(OH)2、NaHSO4[或Mg(HSO4)2]
(2)2Al3++3SO42- +3Ba2+ +8OH-=== 3BaSO4↓+2AlO2- +4H2O
(3)c( Na+)> c(CO32-)>c( OH-) >c(HCO3-)>c( H+)
本题解析:阴离子CO32-只能和Na+结合为Na2CO3;OH-能和Ba2+结合为溶于水的Ba(OH)2,则SO42-和Al3+结合成的物质为Al2(SO4)3;最后剩余Cl-和HSO4-结合的阳离子Na+、Mg2+;由题干可知A和B、C、D都生成沉淀且沉淀都溶于酸溶液,所以A为Na2CO3;E中含HSO4-,沉淀可以是Mg2+、Al3+、Ba2+的碳酸盐沉淀;B、C、D物质中分别含这三种阳离子,由④B溶液与适量D溶液反应生成白色沉淀,加入过量D溶液,沉淀量减少,但不消失,说明溶解的沉淀是Al(OH)3,可推出B为Al2(SO4)3,D为Ba(OH)2,C为MgCl2,符合①②③沉淀形成的性质;①②生成的沉淀溶解于E,说明E中不能含和硫酸根离子、镁离子生成沉淀的离子,则E只能为:NaHSO4(或Mg(HSO4) 2),(1)综上所述,A为Na2CO3,B为Al2(SO4)3,C为MgCl2,D为Ba(OH)2,E为NaHSO4[或Mg(HSO4)2];(2)④中反应的离子方程式为2Al3++3SO42- +3Ba2+ +8OH-=== 3BaSO4↓+2AlO2- +4H2O;(3)A为碳酸钠,碳酸根离子水解显碱性,第一步水解大于第二步水解,则离子浓度大小为c( Na+)> c(CO32-)>c( OH-) >c(HCO3-)>c( H+)。
考点:考查无机物的推断。
本题难度:困难
2、选择题 下表中对应关系正确的是
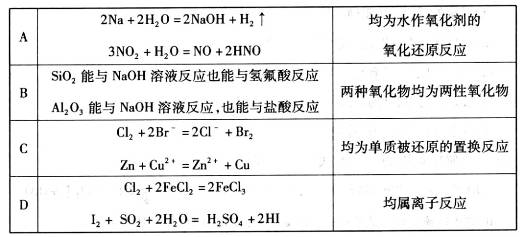
参考答案:D
本题解析:A、NO2与水的反应中NO2既是氧化剂,也是还原剂,水不是氧化剂,也不是还原剂,A错误;B、能与碱反应生成盐和水的氧化物是酸性氧化物,既能与碱反应生成盐和水,也能与酸反应生成盐和水的氧化物是两性氧化物。二氧化硅只能与氢氟酸反应生成四氟化硅和水,属于酸性氧化物,氧化铝是两性氧化物,B错误;C、锌置换铜的反应中锌元素的化合价降低,被氧化,C错误;D、反应中均离子参加或生成,属于离子反应,D正确,答案选D。
考点:考查氧化还原反应、离子反应以及两性氧化物等有关判断
本题难度:一般
3、填空题 (11分)有A、B、 C、D、E五种无色溶液,它们是硝酸钙、稀盐酸、硝酸银、碳酸钠和氯化钡。各取少量进行两两混合实验,结果如下(表中“↓”表示有沉淀出现,“↑
C、D、E五种无色溶液,它们是硝酸钙、稀盐酸、硝酸银、碳酸钠和氯化钡。各取少量进行两两混合实验,结果如下(表中“↓”表示有沉淀出现,“↑
 ”表示有气体生成,“―”表示没有明显现象):
”表示有气体生成,“―”表示没有明显现象):
| A
| B
| C
| D
| E
|
A
| 
| ↓
| ―
| ↓
| ―
|
B
|
|
| ↓
| ↓
| ―
|
C
| ―
| ↓
|
| ↑
| ―
|
D
| ↓
| ↓
| ↑
|
| ↓
|
E
| ―
| ―
| ―
| ↓
|
|
(1)请写出A、B、C、D 、E各溶液中溶质的化学式:
、E各溶液中溶质的化学式:
 A B C D E
A B C D E
(2)请写出A+B,C+D,D+E反应的离子方程式
①A+B:
②C+D:
③A+D: 
参考答案:(11分)
(1)A:BaCl2 B:AgNO3 C:HCl D:Na2 CO3 E:Ca(NO3)2(每空1分)
CO3 E:Ca(NO3)2(每空1分)
(2)Cl―+Ag+=AgNO3↓ 2H++CO32―=H2O+CO2↑或H++CO32―=HCO3―
2H++CO32―=H2O+CO2↑或H++CO32―=HCO3―
Ca2++CO32―=CaCO3↓ (每空2分)
本题解析:略
本题难度:一般
4、选择题 下列反应的离子方程式书写不正确的是
A.小苏打溶液显碱性:HCO3-+H2O