微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、简答题 (1)要配制浓度约为2mol/L?NaOH溶液100mL,下列操作正确的是(填代号)______.
A、称量8g?NaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯
中,同时不断搅拌至固体溶解
B、称量8g?NaOH固体,放入100mL量筒中,边搅拌边加蒸馏水,待固体完全溶解后用蒸馏水稀释至100mL
C、称量8g?NaOH固体,放入100mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加蒸馏水至刻度,盖好瓶塞,反复摇匀.
D、用100mL量筒量取40mL?5mol/L?NaOH溶液,倒入250mL烧杯中,再用同一量筒量取60mL蒸馏水,再慢慢搅拌下慢慢倒入烧杯中
(2)要配制500mL?0.200mol/L的H2SO4溶液,需要的仪器有量筒、烧杯、______.需要98%的浓硫酸(密度1.84g/mL)______mL.下列操作会使所配的溶液浓度偏小的是(填代号)______.
A、用量筒量取一定体积的98%的浓硫酸,稀释后未经冷却即转入容量瓶内;
B、稀释硫酸所用的小烧杯未洗涤?
C、定容时仰视观察液面
D、定容时俯视观察液面?
E、用蒸馏水洗涤后的容量瓶未干燥
F、定容摇匀后,倒入干燥的试剂瓶中储存时,有少量溶液溅出瓶外.
参考答案:(1)溶质的质量为m=nM=cvM=2mol/L×0.1L×40g/mol=8g,
A、根据浓度约为2mol/L?NaOH溶液100mL,这是粗略配制,所以可将8g?NaOH固体,放入250mL烧杯中,用100mL量筒量取100mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解,故A正确;
B、因量筒不能用来溶解固体,故B错误;
C、因容量瓶不能直接用来溶解固体,故C错误;
D、因浓度约为2mol/L?NaOH溶液100mL,这是粗略配制,用5mol/L?NaOH溶液来稀释需体积为2mol/L?×0.1L5mol/L=0.04L,即40mL,所以可用100mL量筒量取40mL?5mol/L?NaOH溶液,倒入250mL烧杯中,再用同一量筒量取60mL蒸馏水,再慢慢搅拌下慢慢倒入烧杯中,故D正确;
故选:A、D;?
(2)因配制步骤有:计算、量取、稀释、移液、洗涤、定容、摇匀、装瓶、贴签等操作,一般用量筒量取(还需胶头滴管),用药匙取用药品,在烧杯中溶解,冷却后转移到100mL容量瓶中,并用玻璃棒引流,当加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,使溶液的凹液面的最低点与刻线相平,振荡、摇匀后,装瓶、贴签.所以需要的仪器为:玻璃棒、烧杯、胶头滴管、量筒、容量瓶,设需要98%H2SO4的体积为VmL,根据溶液稀释前后溶质质量不变则,VmL×1.84g/cm3×98%=0.5L×0.2mol?L-1×98g/mol,解得V=5.4ml,
A、用量筒量取一定体积的98%的浓硫酸,稀释后未经冷却即转入容量瓶内,热溶液的体积偏大,一但冷却下来,溶液的体积偏小,浓度偏大,故A错误;
B、稀释硫酸所用的小烧杯未洗涤,因烧杯内壁沾有溶质,所以溶质的质量偏小,浓度偏小,故B正确;?
C、定容时仰视观察液面,溶液的液面高于刻度线,所以溶液的体积偏大,浓度偏小,故C正确;
D、定容时俯视观察液面,溶液的液面低于刻度线,溶液的体积偏小,浓度偏大,故D错误;
E、用蒸馏水洗涤后的容量瓶未干燥,对溶液的体积无影响,浓度不变,故E错误;
F、定容摇匀后,倒入干燥的试剂瓶中储存时,有少量溶液溅出瓶外,由于是均匀的溶液,对溶液的浓度无影响,故F错误;
故答案为:玻璃棒、胶头滴管、100mL容量瓶;5.4;B、C.
本题解析:
本题难度:一般
2、填空题 (2分)27.2g某二价金属的氯化物ACl2中含有0.4m ol Cl-离子,ACl2的摩尔质量是?,A的相对原子质量是?。
ol Cl-离子,ACl2的摩尔质量是?,A的相对原子质量是?。
参考答案:136g/mol??65??(各2分,共4分)
本题解析:略
本题难度:一般
3、选择题 科学家刚刚发现了某种元素的原子X,X原子的质量是ag。已知12C(含6个质子和6个中子的一种碳原子,相对原子质量为12)的原子质量是bg,nA是阿伏加德罗常数的值,下列说法正确的是
A.由已知信息可知:nA=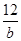
B.X原子的摩尔质量是nAa g/mol
C.Wg X原子的物质的量是 mol
mol
D.X原子的相对原子质量为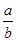
参考答案:AB
本题解析:
A、B正确;C、不正确,Wg X原子的物质的量是 mol ; D.不正确,X原子的相对原子质量为
mol ; D.不正确,X原子的相对原子质量为 。
。
本题难度:一般
4、选择题 下列有关物理量相应的单位表达错误的是( )
A.摩尔质量g/mol
B.物质的量mol
C.溶解度g/100g
D.密度g/cm3
参考答案:C
本题解析:
本题难度:简单
5、选择题 下列溶液中,Cl-的物质的量浓度最大的是( )
A.100mL0.5mol/LAlCl3(aq)
B.200mL0.5mol/LMgCl2(aq)
C.300mL1mol/LNaCl(aq)
D.400mL0.5mol/LBaCl2(aq)
参考答案:A、100 mL 0.5 mol/L AlCl3(aq),氯离子浓度为:0.5 mol/L×3=1.5 mol/L,
B、200 mL 0.5 mol/L MgCl2(aq),氯离子浓度为:0.5 mol/L×2=1mol/L,
C、300 mL 1 mol/L NaCl(aq),氯离子浓度为:1 mol/L×1=1 mol/L,
D、400 mL 0.5 mol/L BaCl2(aq),氯离子浓度为:0.5 mol/L×2=1mol/L,
所以氯离子浓度最大的是A,
故选A.
本题解析:
本题难度:一般