| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《物质的量》考点特训(2017年冲刺版)(四)
参考答案:D 本题解析:A.丙烷的相对分子质量是44,所以中17.6 g的物质的量是0.4mol,由于每1mol的该物质中含有极性键8mol,所以0.4mol中所含的极性共价键为 3.2NA,错误;B.常温常压下,2.24 L 乙烯的物质的量小于0.1mol,所以其中电子总数少于1.6NA,错误;C.将纤维素和硫酸加热水解后的液体取出少许,加入NaOH溶液中和催化剂硫酸后,再加入新制的Cu(OH)2悬浊液,并加热煮沸,若有红色沉淀生成,证明纤维素水解生成了葡萄糖,错误;D.由于1-溴丙烷和2-溴丙烷的H原子的种类、个数不同,所以可以利用核磁共振氢谱图可鉴别它们,正确。 本题难度:一般 3、计算题 (6分)常温下,将17.6g氢氧化钠和氢氧化钾的固体混合物溶于水,配成250mL溶液,从中取出25mL,用1mol/L的硫酸去滴定,结果用去硫酸20.00mL。求: 参考答案:⑴12g?(2)13 本题解析:(1)n(OH-)=1mol/L×2×0.02L×10=0.4mol,设NaOH为xmol,KOH为ymol。则40x+56y=17.6,x+y=0.4,求得x=0.3mol,y=0.1mol。所以NaOH的质量为0.3mol×40g/mol=12g。 本题难度:一般 4、选择题 在200 mL某硫酸盐溶液中,含有1.5NA个硫酸根离子(NA表示阿伏加德罗常数的值),同时含有NA个金属离子。则该硫酸盐的物质的量浓度为( ) |
参考答案:B
本题解析:金属离子与硫酸根离子的物质的量之比为2∶3,所以该硫酸盐的化学式为M2(SO4)3,n[M2(SO4)3]="0.5" mol
本题难度:一般
5、选择题 若100 mL 0.5 mol・L-1的某溶液中含溶质质量为3.7 g,则该溶质的摩尔质量是(? )
A.74 g・mol-1
B.56 g・mol-1
C.37 g・mol-1
D.58.5 g・mol-1
参考答案:A
本题解析:溶质的物质的量为:0.1 L×0.5 mol・L-1="0.05" mol
M=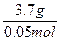 ="74" g・mol-1
="74" g・mol-1
本题难度:简单
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学知识点整理《化学反应进.. | |