| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点讲解《盐类水解的原理》在线测试(2017年最新版)(八)
参考答案:B 本题解析:A、FeCl3+3H2O 本题难度:一般 3、选择题 下列有关电解质溶液中微粒的物质的量浓度关系正确的是 |
参考答案:A
本题解析:
试题解析:A、0.1mol/L Na2CO3溶液中存在质子守恒:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3),故A正确;B. 在0.1 mol・L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(H2CO3)>c(CO32-),故B错误;C.向0.2 mol・L-1NaHCO3溶液中加入等体积0.1 mol・L-1NaOH溶液所得的溶液为等浓度的Na2CO3和NaHCO3溶液,由于碳酸根离子的水解程度大于碳酸氢跟离子的水解程度,则离子浓度的大小关系为: c(HCO3-)>c(CO32-)> c(OH-)>c(H+),故C错误;D.常温下,CH3COONa和CH3COOH混合溶液pH=7,则溶液显中性,所以c(CH3COONa)大于c(CH3COOH),但醋酸根离子的水解程度与醋酸的电离程度相等, 故:c(Na+) 等于c(CH3COO-),故D错误。
考点:离子浓度的比较
本题难度:困难
4、选择题 下列说法错误的是
①NaHCO3溶液加水稀释,c(Na+)/c(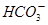 )的值保持增大
)的值保持增大
②浓度均为0.1mol・L-1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c( )+c(
)+c(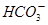 )]
)]
③在0.1mol・L-1氨水中滴加0.1mol・L-1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH-)=10-a mol・L-1
④向0.1mol・L-1(NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c(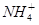 )、c(
)、c(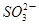 )均增大
)均增大
⑤在Na2S稀溶液中,c(H+)=c(OH-)+2c(H2S)+c(HS-)
A.①④
B.②④
C.①③
D.②⑤
参考答案:B
本题解析:①加水稀释,碳酸氢根的水解程度增大,所以比值增大,正确;②在同业中遵循物料守恒,钠原子:碳原子=3:2,所以有2c(Na+)=3[c(CO32-)+c(HCO3-)+c(H2CO3)],错误;③恰好完全反应时,溶液中的氢离子和氢氧根离子都是水电离的,所以溶液的pH=a,则溶液中的氢离子浓度=10-amol/L,则氢氧根离子浓度也为10-amol/L,正确;④加入氢氧化钠固体,促进铵根离子水解,抑制亚硫酸根离子水解,所以铵根离子浓度减小,亚硫酸根离子浓度增大,错误;⑤根据溶液中质子守恒,即水电离的氢离子和氢氧根离子浓度永远相等,可以写出c(H+)=c(OH-)+2c(H2S)+c(HS-),正确;所以选B。
考点:溶液的酸碱性和溶液中的离子浓度比较
本题难度:困难
5、实验题 硫酸亚锡(SnSO4)是一种重要的硫酸盐,主要用于电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等。某研究小组设计SnSO4制备路线如下: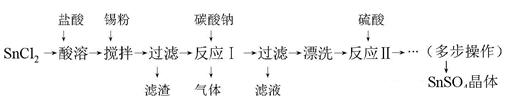
查阅资料:
Ⅰ.酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。
Ⅱ.SnCl2易水解生成难溶物Sn(OH)Cl(碱式氯化亚锡)。
请回答下列问题:
(1)SnCl2粉末需加浓盐酸进行溶解,请用平衡移动原理解释原因 。
(2)加入Sn粉的作用有两个:①调节溶液pH ② 。
(3)反应Ⅰ生成的气体为CO2,得到的沉淀是SnO。该沉淀经过滤后需漂洗,如何证明沉淀已经洗涤完全? 。
(4)多步操作包含的具体实验步骤的名称可以是: 。
(5)酸性条件下,SnSO4还可以用作双氧水去除剂,发生反应的离子方程式是 。
(6)该小组通过下列方法测所用锡粉样品的纯度(杂质不参与反应):
①将试样溶于盐酸中,发生的反应为:Sn + 2HCl→SnCl2 + H2↑;
②加入过量的FeCl3;
③用已知浓度的K2Cr2O7滴定生成的Fe2+,发生的反应为:6FeCl2 + K2Cr2O7 + 14HCl →6FeCl3 + 2KCl + 2CrCl3 +7H2O
取1. 226 g 锡粉样品,经上述各步反应后,共用去0.1000 mol/L K2Cr2O7溶液32.00 mL。则该锡粉样品中锡的质量分数是
参考答案:(1)加入盐酸,使水解平衡向左移动,抑制Sn2+水解
(2)防止Sn2+被氧化
(3)取最后一次洗涤液,向其中加入AgNO3溶液,若无沉淀,则说明已洗涤干净
(4)加热浓缩、冷却结晶、过滤、洗涤
(5)Sn2+ + H2O2 +2H+=Sn4+ +2H2O
(6)93.18%
本题解析:(1)SnCl2在水中发生水解反应:SnCl2+H2O Sn(OH)Cl+HCl. 生成难溶物Sn(OH)Cl,使溶液变浑浊。若加入HCl,可使平衡向逆反应方向移动,抑制Sn2+水解。
Sn(OH)Cl+HCl. 生成难溶物Sn(OH)Cl,使溶液变浑浊。若加入HCl,可使平衡向逆反应方向移动,抑制Sn2+水解。
(2)由于在酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式,Sn2+易被氧化。为了调节调节溶液pH并防止Sn2+被氧化为Sn4+要加入Sn粉。
(3)在反应过程中加入了HCl,沉淀的表面会有Cl-存在,只要能证明在洗涤液中无Cl-存在就可以证明沉淀已经洗涤完全。具体的检验方法是取最后一次洗涤液,向其中加入AgNO3溶液,若无沉淀,则说明已洗涤干净。
(4)在多步操作中所包含的具体实验步骤的名称是加热浓缩、冷却结晶、过滤、洗涤。
(5)酸性条件下,SnSO4与双氧水发生反应的离子方程式是Sn2+ + H2O2 +2H+=Sn4+ +2H2O。
(6)在处理过程中发生的反应为:Sn + 2HCl=SnCl2 + H2↑;2FeCl3+SnCl2=2FeCl2+ SnCl4
6FeCl2 + K2Cr2O7 + 14HCl =6FeCl3 + 2KCl + 2CrCl3 +7H2O。由方程式得关系式3Sn―3SnCl2 ―6FeCl3 ― K2Cr2O7.因为n(K2Cr2O7)="C・V=0.1000" mol/L×0.032L=3.2×10-3mol.所以n(Sn)= 3×3.2×10-3mol ="9.6" × 10-3mol.m(Sn)=n・M=9。6×10-3mol×119g/mol=1.14g.该锡粉样品中锡的质量分数是(1.14g÷1. 226 g) ×100%=93.18%.
考点:考查在电镀工业的镀锡、铝合金表面的氧化着色、印染工业的媒染剂、双氧水去除剂等有重要作用的SnSO4制备、性质反应原理等的知识。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《化学反应与.. | |