微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 已知氢氧化铁胶体是氢氧化铁胶粒吸附多余Fe3+生成的。现将氢氧化铁固体粉碎使粒子直径在10-9~10-7m,并悬浮于水中,再向悬浊液中加入______或______,即可制得Fe(OH)3胶体。(填两类不同物质)
参考答案:含三价铁的盐;适量的强酸
本题解析:
本题难度:一般
2、实验题 高纯MnCO3是制备高性能磁性材料的主要原料。实验室以MnO2为原料制备少量高纯MnCO3的操作步骤如下:
(1)制备MnSO4溶液:在烧瓶中加入一定量MnO2和水,搅拌,通入SO2和N2混合气体,反应3h。停止通入SO2,继续反应片刻,过滤 (已知MnO2+H2SO3=MnSO4+H2O)。
①石灰乳参与反应的化学方程式为____________________
②反应过程中,为使SO2尽可能转化完全,在通入SO2和N2比例一定、不改变固液投料的条件下,可采取的合理措施有________________、____________________。
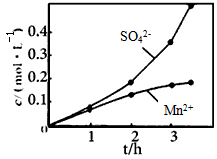
③若实验中将N2换成空气,测得反应液中Mn2+、SO42-的浓度随反应时间t变化如下图。导致溶液中
Mn2+、SO42-浓度变化产生明显差异的原因是____________________
(2)制备高纯MnCO3固体:已知MnCO3难溶于水、乙醇,潮湿时易被空气氧化,100℃开始分解;
Mn(OH)2开始沉淀时pH=7.7。请补充由(1)制得的MnSO4溶液制备高纯MnCO3的操作步骤[实验中可选用的试剂:Ca(OH)2、NaHCO3、Na2CO3、C2H5OH]
①________;②________;③________;④_______;⑤低于100℃干燥。
参考答案:(1)①Ca(OH)2+SO2=CaSO3+H2O;②控制适当的温度;缓慢通入混合气体;③Mn2+催化O2与H2SO3反应生成H2SO4
(2)①边搅拌边加入NaHCO3(Na2CO3),并控制溶液pH<7.7;②过滤,用少量水洗涤2~3次;③检验SO42-
是否被洗涤除去;④用少量C2H5OH洗涤
本题解析:
本题难度:一般
3、简答题 如图为乙酸和乙醇在一定条件下制取乙酸乙酯的实验,
试叙述:该实验反应现象:______
反应化学方程式:______.
说明:①药品加入顺序:浓硫酸一定不能第一个加入.
②浓硫酸的作用:______
③饱和碳酸钠作用:______
④此反应是可逆反应
⑤长导管不能伸入到液面以下:______.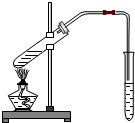
参考答案:
制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,碳酸钠水解呈碱性,乙酸乙酯不溶于饱和碳酸钠溶液,密度比水小,有香味;酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,故答案为:在碳酸钠溶液层上方有无色油状液体出现,闻到香味;CH3COOH+C2H5OH浓硫酸
本题解析:
本题难度:一般
4、实验题 乙酰水杨酸即阿司匹林,可通过水杨酸与乙酸酐反应制得。
主反应: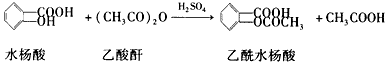
副反应: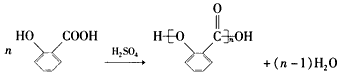
乙酰水杨酸能与碳酸钠反应生成水溶性盐,而副产物聚合物不溶于碳酸钠溶液。

制取乙酰水杨酸的实验步骤如下。
(1)投料。在125 mL的锥形瓶中依次加入2 g水杨酸、5 mL乙酸酐、5滴浓硫酸,小心旋转锥形瓶使水杨酸全部溶解后,加热5~ 10 min,控制温度在85~90℃。
①试剂添加时如果先加水杨酸和浓硫酸,产率会降低,原因是______________。
②最合适的加热方法是_________。
(2)粗产品结晶。取出锥形瓶,边摇边滴加1 mL冷水,然后快速加入50 mL冷水,立即进行冰浴冷却。待晶体完全析出后用布氏漏斗抽滤,用少量冰水分两次洗涤锥形瓶后,再洗涤晶体,抽干。洗涤晶体要用少量冰水的原因是_______________。
(3)粗产品提纯。将粗产品转移到150 mL烧杯中,在搅拌下慢慢加入适量_________,加完后继续搅拌几分钟,直到__________为止。 抽滤,副产物聚合物被滤出,用5~10 mL水冲洗漏斗,合并滤液,倒入预先盛有4~5mL浓盐酸和10 mL水配成溶液的烧杯中,搅拌均匀,即有乙酰水杨酸沉淀析出。
(4)纯度检验。检验粗产品中是否含有水杨酸,可取少许产品加入盛有5 mL水的试管中,加入1~2滴
_________溶液, 观察有无颜色反应。
参考答案:
(1)①水杨酸会被氧化;②水浴加热
(2)减少晶体的溶解
(3)饱和碳酸钠溶液;无二氧化碳气体产生
(4)三氯化铁或(FeCl3)
本题解析:
本题难度:困难
5、实验题 如下图所示,U形管的左端被水和胶塞封闭有甲烷和氯气(体积比为1:4)的混合气体,假定氯气在水中的溶解可以忽略。将封闭有甲烷和氯气的混合气体的装置放置在有光的地方,让混合气体缓慢的反应一段时间。

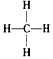
(1)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:________________________。写出甲烷的结构式:__________。
(2)经过几个小时的反应时,U形管右端的玻璃管中水柱变化是__________。
A.升高
B.降低
C.不变
D.无法确定
(3)U形管左端的气柱变化是__________。
A.体积增大
B.体积减小
C.消失
D.不变
参考答案:(1) ;
;
(2)B
(3)C
本题解析:
本题难度:一般