微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、实验题 聚合硫酸铁又称聚铁,化学式为[Fe2(OH)n(SO4)3-0.5n]m,广泛用于污水处理。实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁和绿矾(FeSO4・7H2O)过程如下
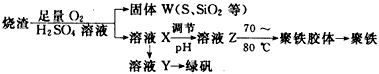
(1)验证固体W焙烧后产生的气体含有SO2的方法是________________________
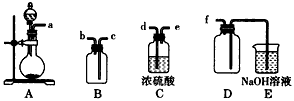
(2)①实验室制备、收集干燥的SO2,所需仪器如下。装置A产生SO2,按气流方向连接各仪器接口,顺序为a→____ →____→____→____→f装置。
②D的作用是______________,装置E中NaOH溶液的作用是______________
(3)制备绿矾时,向溶液X中加入过量__________,充分反应后,经_______________操作得到溶液Y,再经浓缩、结晶等步骤得到绿矾。
(4)溶液Z的pH影响聚铁中铁的质量分数,用pH试纸测定溶液pH的操作方法为___________ 若溶液Z的pH偏小,将导致聚铁中铁的质量分数偏______________。
2、实验题 我国著名化学家侯德榜生先发明的“侯氏制碱法”,因原料利用率高,并能进行连续生产,从而享誉海内外。“侯氏制碱法”的原理是向饱和食盐水中通入氨气和二氧化碳,获得碳酸氢钠晶体,再将所得的碳酸氢钠晶体加热分解后即 可得到纯碱。它的反应原理可用下列化学方程式表示:
NaCl(饱和)+NH3+CO2+H2O===NaHCO3↓+NH4Cl;2NaHCO3 Na2CO3+CO2↑+H2O。某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如图所示的一套实验装置:
Na2CO3+CO2↑+H2O。某课外兴趣小组同学,按照“侯氏制碱法”原理,设计了如图所示的一套实验装置:
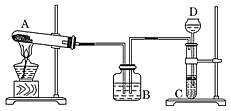
实验室可供选用的药品有:浓氨水、纯碱、大理石、稀盐酸、稀硫酸、熟石灰、氯化氨、氯化钠。
(1)A、D中最合适的试剂为:A________;D________(填名称)。
(2)本实验具体操作过程中,应先通入________气体,再通入________气体;原因是_________________________________________________________________。
(3)指出该装置中的错误(至少两处)__________________________________________ 。
(4)在改进装置中,该兴趣小组同学进行了实验,实验所用的饱和NaCl溶液中含溶质58.5 g,实验最后得到无水碳酸钠26.0 g,则其产率为________;该兴趣小组同学针对其实验结果,认真分析了造成损失的原因,发现其操作步骤并没有错误,则主要原因是_______________________________________________。
(5)在“侯氏制碱法”工业生产中,原料的利用率高,大大降低了成本.请问本实验中哪些物质可重复利用?____________。
3、选择题 用96%的乙醇溶液制取无水乙醇时,可选用的方法是
[? ]
A.加入无水硫酸铜,再过滤 ?
B.加入生石灰,再蒸馏 ?
C.加入浓硫酸,再加热,蒸出乙醇 ?
D.将96%的乙醇溶液直接加热蒸馏出来
4、实验题 实验室制备硝基苯的主要步骤如下:
①配制一定比例的浓硝酸和浓硫酸的混合酸,加入反应器中;
②在室温下 的混合酸中逐滴加入一定量的苯,充分振荡,混合均匀;
③在50~60℃下发生反应,直至反应结束;
④除去混 合酸后,粗产品依次用蒸馏水和5%的氢氧化钠溶液洗涤,最后再用蒸馏水洗涤;
⑤将用无水氯化钙干燥后的 粗硝基苯进行蒸馏,得到较纯的硝基苯。
试回答下列问题:
(1)配制一定比例的浓硫酸和浓硝酸的混合酸时,应注意的事项是____。
(2)步骤③中为了使反应在50~60℃下进行,常用的方法是____。
(3)步骤④中洗涤、分离粗硝基苯应使用的主要仪器是____。
(4)步骤④中粗产品用5%的氢氧化钠溶液洗涤的目的是____。
(5)纯净的硝基苯是____色,密度比水____,具有____气味的油状液体。
5、实验题 某工厂有废合金(含有铝、铁、铜)粉末,甲同学探索工业废料的利用,用该废合金粉末制取纯净的氯化铝溶液、绿矾晶体和胆矾晶体,其实验方案如下
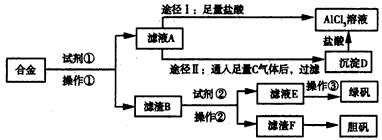
试回答下列问题:
(1)所加试剂①、②分别是___________、____________。
(2)写出废合金与试剂①反应的离子方程式:___________________。
(3)由滤液A制AlCl3溶液有途径I和途径Ⅱ两种,你认为合理的是____________,理由是_____________,写出A→D反应的离子方程式:________________。
(4)操作③的名称是______________。