微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、填空题 在氮的单质和常见化合物中(用N2、NH3、NH4Cl填空)
(1)常用作保护气(如填充灯泡、焊接保护等)的物质是?,
(2)常用作制冷剂的物质是??,
(3)能与酸反应生成盐,在常温下为气态的物质是??,
(4)用作氮肥的是??。
参考答案: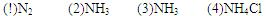
本题解析:略
本题难度:一般
2、填空题 写出实验室制取NH3的化学反应方程式为_____?__;常用?干燥NH3 ;收集时应用?法收集;检验NH3是否已充满试管的方法是?。
参考答案:2NH4Cl+Ca(OH)2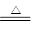 CaCl2+2NH3↑+2H2O ;碱石灰;向下排空气;?用润湿的红色石蕊试纸靠近导管口。
CaCl2+2NH3↑+2H2O ;碱石灰;向下排空气;?用润湿的红色石蕊试纸靠近导管口。
本题解析:实验室制备氨气为氯化铵与氢氧化钙加热,故反应方程式为2NH4Cl+Ca(OH)2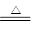 CaCl2+2NH3↑+2H2O。氨气为碱性气体,故用碱性物质干燥,故为碱石灰;氨气密度小于空气,故用向下排空气法收集;检验氨气是否充满试管的方法为用润湿的红色石蕊试纸靠近导管口。
CaCl2+2NH3↑+2H2O。氨气为碱性气体,故用碱性物质干燥,故为碱石灰;氨气密度小于空气,故用向下排空气法收集;检验氨气是否充满试管的方法为用润湿的红色石蕊试纸靠近导管口。
本题难度:一般
3、计算题 在硝酸生产过程中所排放出来的废气中含有NO和NO2,它们污染环境,现有氨催化还原法将它们转化为无毒气体(填名词)_____直接排放空气中,写出有关反应方程式:______。假设NO和NO2物质的量________之比恰好为1∶1,则两者的混合物相当于一种酸酐,写出由烧碱溶液吸收这种酸酐的化学方程式:________。
参考答案:氮气;6NO2+8NH3 7N2+12H2O
7N2+12H2O
6NO+4NH3 5N2+6H2O
5N2+6H2O
NO+NO2+2NaOH====2NaNO2+H2O
或(N2O3+2NaOH====2NaNO2+H2O)
本题解析:正价的氮的化合物与负价的氮的化合物往往可以发生反应生成单质N2。所以NO2与NH3在催化剂作用下生成无毒的N2单质。
第二空:NO和NO2物质的量之比为1∶1的混合物,相当于亚硝酸酸酐N2O3,其中N的化合价为+3价,与NaOH溶液反应,生成相应的价态的盐和水。反应式:N2O3+2NaOH====2NaNO2+H2O
本题难度:一般
4、填空题 雄黄(AS4S4)和雌黄(As2S3)是提取砷的主要矿物原料,二者在自然界中共生。根据题意完成下列填空:
⑴As2S3和SnCl2在盐酸中反应转化为As4S4和SnCl4并放出H2S气体。若As2S3和SnCl2正好完全反应,该反应的化学方程式为 。
⑵上述反应中的氧化剂是 ,反应产生的气体可用 吸收。
⑶As2S3和HNO3有如下反应:As2S3+ 10H++ 10NO3―=2H3AsO4+ 3S+10NO2↑+ 2H2O,若生成2mol H3AsO4,则反应中转移电子的物质的量为 。若将该反应设计成一原电池,则NO2应该在 极附近逸出。
⑷将⑶中反应产物NO2充满干燥的烧瓶,然后将烧瓶倒立于少水槽中,向烧瓶中通入一定量的氧气,气体恰好完全溶于水(假设溶液没有扩散),则烧瓶中溶液溶质的物质的量浓度为 (设该条件下的气体摩尔体积为23.8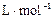 ,结果保留到小数点后三位)。
,结果保留到小数点后三位)。
参考答案:

本题解析:略
本题难度:一般
5、选择题 在某稀硝酸的溶液中,加入5.6g铁粉充分反应后,铁粉全部溶解,放出NO气体,溶液质量增加3.2g,所得溶液中Fe2+和Fe3+物质的量之比为(?)
A.1:1
B.3:2
C.2:1
D.4:1
参考答案:B
本题解析:设生成的NO的质量为5.6―3.2=2.4g,物质的量为 =0.08mol
=0.08mol
设溶液中Fe2+和Fe3+物质的量分别为a、b
两者的总物质的量为a+b= =0.1
=0.1
由电子的得失守恒可知2a+3b=0.08×3
可知a=0.06mol? b=0.04mol
故答案为B
本题难度:一般