微信搜索关注"91考试网"公众号,领30元,获取公务员、事业编、教师等考试资料40G!
1、选择题 下列叙述中错误的是
[? ]
A.钠原子和氯原子作用生成NaCl后,其结构的稳定性增强
B.在氯化钠中,除氯离子和钠离子的静电吸引力作用外,还存在电子与电子、原子核与原子核之间的排斥作用
C.任何离子键在形成的过程中必定有电子的得与失
D.钠与氯气反应生成氯化钠后,体系能量降低
参考答案:C
本题解析:
本题难度:简单
2、选择题 某短周期元素最外层只有2个电子,则该元素一定是( )
A.第1、2或3周期元素
B.最高正化合价为+2
C.IIA族元素
D.金属元素
参考答案:短周期元素最外层只有2个电子,则该元素可能为He元素或ⅡA族元素,则:
A、该元素可能是He元素、Be元素或Mg元素,故可以是第1、2或3周期元素,故A正确;
B、若该元素为He,主要化合价为0价,故B错误;
C、若该元素为He,为零族元素,故C错误;
D、若该元素为He,不是金属元素,故D错误;
故选A.
本题解析:
本题难度:一般
3、选择题 某元素原子核外L层电子数比K层电子数多3,则此元素在周期表中位于( )
A.第二周期第ⅤA族
B.第二周期第ⅦA族
C.第三周期第ⅤA族
D.第三周期第ⅦA族
参考答案:某元素原子核外L层电子数比K层电子数多3,K层电子数是2,L层电子数比K层电子数多3,则L层电子数是5,则该元素是N元素,该元素核外有2个电子层,所以在第二周期,其最外层电子数是5,则为第VA族,所以该元素位于第二周期第VA族,故选A.
本题解析:
本题难度:简单
4、选择题 化学科学需要借助化学专用语言来描述,下列有关化学用语正确的是( )
A.CO2的电子式:
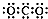
B.质量数为37的氯原子:
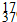
Cl
C.NH4Cl的电子式:
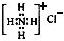
D.原子核内有10个中子的氧原子:
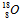
参考答案:D
本题解析:
本题难度:简单
5、填空题 下表为周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)表中属于d区的元素是 (填编号)。?
(2)元素⑥形成的最高价含氧酸根的立体构型是 ,其中心原子的杂化轨道类型是 。
(3)元素②的一种氢化物是重要的化工原料,常把该氢化物的产量作为衡量石油化工发展水平的标志。有关该氢化物分子的说法正确的是 。
A.分子中含有氢键
B.属于非极性分子
C.含有4个σ键和1个π键
D.该氢化物分子中,②原子采用sp2杂化
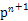 ,该元素原子的核外最外层电子的孤电子对数为 ;该元素与元素①形成的分子X构形为 ;X在①与③形成的分子Y中的溶解度很大,其主要原因是?。
,该元素原子的核外最外层电子的孤电子对数为 ;该元素与元素①形成的分子X构形为 ;X在①与③形成的分子Y中的溶解度很大,其主要原因是?。